Цинк-воздушные батареи — прорыв в области хранения энергии?
Электрохимические технологии хранения энергии быстро развиваются. Компания NantEnergy предлагает бюджетный цинково-воздушный аккумулятор энергии.

Компания NantEnergy, возглавляемая калифорнийским миллиардером Патриком Сун-Шионгом (Patrick Soon-Shiong), представила цинково-воздушный аккумулятор энергии (Zinc-Air Battery), стоимость которого существенно ниже литий-ионных аналогов.
Цинково-воздушный аккумулятор энергии
Батарея, «защищённая сотней патентов», предназначена для использования в системах хранения энергии в энергетике. По утверждению NantEnergy, её стоимость ниже ста долларов за киловатт-час.
Устройство цинково-воздушной батареи отличается простотой. При зарядке электричество преобразует оксид цинка в цинк и кислород. В фазе разряда в ячейке цинк окисляется воздухом. Одна батарея, заключённая в пластиковый корпус, по размерам ненамного больше, чем портфель для бумаг.
Цинк не является редким металлом, и проблемы ограниченности ресурсов, обсуждаемые в связи с литий-ионными аккумуляторами, цинк-воздушные батареи не затрагивают. Кроме того, последние практически не содержат вредных для окружающей среды элементов, и цинк очень легко перерабатывается для вторичного использования.
Важно отметить, что устройство NantEnergy — это не прототип, а серийная модель, которая испытывалась в течение последних шести лет «в тысячах разных мест». Эти батареи обеспечивали энергией «более 200 тысяч жителей Азии и Африки и использовались в более чем 1000 башен сотовой связи по всему миру».
Столь низкая стоимость системы хранения энергии позволит «превратить электрическую сеть в работающую круглосуточно полностью безуглеродную систему», то есть основанную полностью на возобновляемых источниках энергии.
Цинк-воздушные батареи — это не новинка, они изобретены еще в XIX веке и широко применяются с 30-х годов прошлого века. Основная сфера применения этих источников питания — слуховые аппараты, портативные радиостанции, фототехника… Определенной научно-технической проблемой, обусловленной химическими свойствами цинка, являлось создание перезаряжаемых аккумуляторов. Судя по всему, данная проблема сегодня в значительной степени преодолены. NantEnergy достигла того, что батарея может повторять цикл заряда и разряда более 1000 раз без ухудшения характеристик.
В числе прочих параметров, указываемых компанией: 72 часа автономии и 20-летний срок службы системы.
К количеству циклов и прочим характеристикам, конечно, есть вопросы, которые надо уточнять. Впрочем, некоторые эксперты в области накопителей энергии верят в технологию. По результатам опроса GTM, проведённого в декабре прошлого года, восемь процентов респондентов указали на цинковые батареи, как на технологию, способную заменить литий-ион в системах хранения энергии.
Ранее, глава Tesla, Илон Маск сообщал, что стоимость литий-ионных элементов (cells), выпускаемых его компанией, может упасть ниже $100/кВт*ч в текущем году.
Часто приходится слышать, что распространение вариабельных ВИЭ, солнечной и ветровой энергетики, якобы тормозится (будет тормозиться) по причине отсутствия дешевых технологий хранения энергии.
Это, разумеется, не так, поскольку накопители энергии — лишь один из инструментов повышения маневренности (гибкости) энергосистемы, но не единственный инструмент. К тому же, как мы видим, электрохимические технологии хранения энергии развиваются высокими темпами. опубликовано econet.ru
Подписывайтесь на наш канал Яндекс Дзен!
Если у вас возникли вопросы по этой теме, задайте их специалистам и читателям нашего проекта здесь.
P.S. И помните, всего лишь изменяя свое потребление — мы вместе изменяем мир! © econet
Воздушно-цинковый элемент — Домашнему мастеру — Сборник — Познавательный Интернет-журнал «Умеха
Мы уже рассказывали, как самим сделать газовый аккумулятор и свинцово-поташный аккумулятор. Предлагаем еще один тип источника тока — воздушно-цинковый элемент. Этот элемент не требует зарядки в процессе эксплуатации, что является весьма важным преимуществом перед аккумуляторами.
Воздушно-цинковый элемент сейчас — наиболее совершенный источник тока, так так он обладает сравнительно высокой удельной энергией (110—180 Вт-ч/кг), прост в изготовлении и эксплуатации и наиболее перспективен в смысле увеличения его удельных характеристик. Теоретически рассчитанная удельная мощность воздушно-цинкового элемента может достигать 880 Вт-ч/кг. Если будет достигнута хотя бы половина этой мощности, элемент станет весьма серьезным соперником двигателя внутреннего сгорания.
Очень важное преимущество воздушно-цинкового элемента — малое изменение напряжения при нагрузке по мере его разряда. Кроме того, такой элемент обладает значительной прочностью, так как его сосуд может быть изготовлен из стали.
Принцип работы воздушно-цинковых элементов основан на использовании электрохимической системы: цинк — раствор едкого калия — активированный уголь, адсорбирующий кислород воздуха. Подбирая составы электролита, активной массы электродов и выбирая оптимальную конструкцию элемента, можно значительно увеличить его удельную мощность.
Конструкция и технологический процесс изготовления воздушно-цинкового элемента почти ничем не отличаются от газового и свинцово-поташного. Устройство его показано на рисунке. В сосуде 1 размещены отрицательный цинковый электрод 2 и положительные электроды 5 из активированного угля. Положительные электроды — мешочного типа. По центру мешочка 4 вставляется стержень 9 из гальванического угля. Мешочек плотно заполняется активированным углем, верхняя часть завязывается вокруг стержня. Отрицательный электрод 2 представляет собой цинковую пластину толщиной 6—10 мм, в верхнем торце которой просверлено отверстие и нарезана резьба, куда заворачивается стальной стержень 6, имеющий на своем конце соответствующую резьбу. На все стержни электродов надеты клеммы 8, обеспечивающие надежный контакт. Между стенками сосуда и электродами проложены сепараторы 3 из гофрированного мипора или мипласта. которые можно взять из выбракованных мотоциклетных или автомобильных аккумуляторов, вымочить в течение 4—6 часов, после чего хорошо промыть проточной водой. В качестве сепараторов можно использовать сукно, тонкий войлок от валенок или стеклоткань.
Сверху элемент закрывается крышкой 7, в которой имеются сквозные пробки 10, через них пропускаются стержни электродов, а также глухая пробка 11 для заливки электролита.
Во время работы аккумулятора цинк постепенно растворяется электролитом. После полного разряда, когда израсходуется весь цинк, положительные электроды сохраняют свою работоспособность, и достаточно заменить отрицательный электрод, как аккумулятор вновь готов к работе.
В качестве электролита применяется 20-процентный раствор едкого калия в дистиллированной воде.
Электролит можно сохранять долго, если залить его в бутылку под самую пробку и стараться не взбалтывать.
Элемент можно неограниченно долго хранить в сухом состоянии, если при его изготовлении на дно заложить необходимое количество едкого калия и герметически закрыть пробкой 11. Чтобы привести такой элемент в действие, достаточно залить в отверстие дистиллированной воды так, чтобы она покрыла электроды.
Для увеличения срока службы цинковой пластины ее можно покрыть амальгамой ртути. В какую-либо фаянсовую или фарфоровую посуду налейте 20—30 г пятипроцентного раствора серной кислоты и капните несколько капель ртути. На дно посуды положите цинковую пластину и небольшим куском суконки или зубной щеткой втирайте ртуть в цинк до тех пор, пока ее поверхность не станет блестящей. Такой способ позволяет продлить срок службы отрицательной пластины в 10-20 раз. Работать с ртутью необходимо в вытяжном шкафу или на открытом воздухе, так как пары ее ядовиты.
Для разборки элемента достаточно со стержней электродов снять клеммы 8, вынуть сквозные пробки 10, после чего легко снимается крышка 7 и можно заменить израсходованную цинковую пластину. При разборке элемента электролит должен быть удален, а внутренняя часть сосуда промыта проточной водой.
Емкость элемента можно значительно увеличить, если отрицательный электрод изготовить из пористого цинка.
Источник тока из алюминия своими руками

Приветствую, Самоделкины!
Из года в год добыча нефти становится все более сложной и топливо, получаемое из нее, становится все более дорогим. В странах евросоюза так вообще грозятся перестать выпускать бензиновые двигатели, хотят заменить весь транспорт на электромобили. Но вот литиевые батареи до сих пор далеко не идеальные и к слову, идеальными становиться совсем не торопятся. В лучшем случае на одном заряде литиевой батареи получится преодолеть дистанцию максимум в 700 км, после чего придется заряжать аккумулятор примерно неделю, а если использовать для зарядки обыкновенную розетку, то это вообще займет просто уйму времени. И вы только представьте, что произойдет, если все начнут постоянно заряжать свои электромобили, какие будут огромные нагрузки на электросеть и как сильно будет просаживаться напряжение. В общем, будущее литиевых аккумуляторов пока видится довольно туманно и с каждым годом все больше и больше исследований посвящается поискам новых вариантов аккумуляторных батарей.
Как известно, самым энергоемким металлом является алюминий. Уже в наше время на некоторых опытных образцах алюминиевых батарей можно проехать без подзарядки порядка 2000 км, причем перезарядка аккумуляторных батарей данного типа происходит всего за 15 минут, после чего можно ехать дальше еще около 2000 км.
Перезарядка алюминиевых батарей отличается от зарядки аккумуляторов на основе лития. Но тем не менее в ней нет ничего сложного, просто нужно вставить новый алюминий, вылить электролит и налить новый электролит, все — по сути, то же самое, что и бензиновый автомобиль, только это уже электромобиль, и нет никаких нагрузок на электросети. К тому же не нужно плодить огромное количество розеток с проводами с огромным сечением, чтобы все эти электромобили зарядить.
Но тут не все так гладко. Достать электричество из алюминия оказывается совсем не так просто, как хотелось бы. Сперва давайте разберемся в чем заключается принцип алюминий-воздушной батареи.
Чтобы такая батарея начала работать понадобятся 2 электрода: один естественно из алюминия, а второй — из графита. Оба эти электрода находятся в растворе электролита.

В качестве электролита можно использовать поваренную соль (NaCl), но с ней можно поднять напряжение примерно до 0,7В. Щелочным электролитом (NaOH) напряжение можно поднять уже больше, примерно до 1В.
В ходе химической реакции алюминий покрывается слоем гидроксида алюминия (Al(OH)3), который плавно опускается на дно емкости. А на поверхности электрода из графита образуются пузырьки водорода, которые в свою очередь приводят к повышению сопротивления и падению напряжения, этот процесс называется поляризацией.
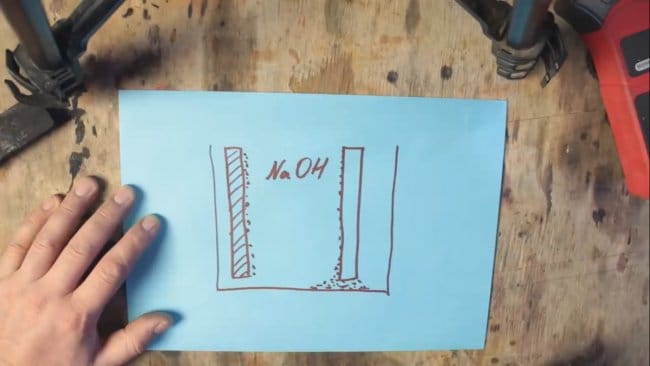
Первую проблему с выпадением осадка гидроксида алюминия можно избавиться простым увеличением емкости, куда будет оседать отработанный продукт, а вот от второй проблемы может помочь деполяризующая масса на основе оксида марганца, который в процессе работы будет превращаться в гидроксид марганца.
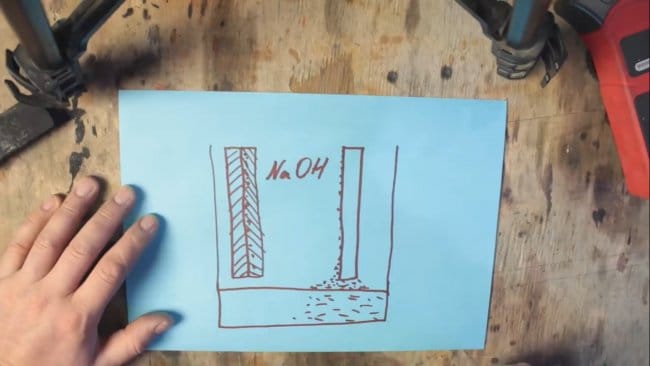
По сути мы получили обыкновенную щелочную батарейку, но только очень большую. Но возникает новая проблема. Дело в том, что оксид марганца тоже расходуются и его тоже придется менять. А нам необходимо добиться чтобы расходовался только алюминий. Для этого придется взять кислород из окружающего воздуха. Вот тут-то и начинается алюминий-воздушная батарея. Одну из стенок просто нужно заменить газопроницаемой мембраной, а графитовый электрод нужно заменить смесью графита и оксида марганца с наночастицами платины или серебра.
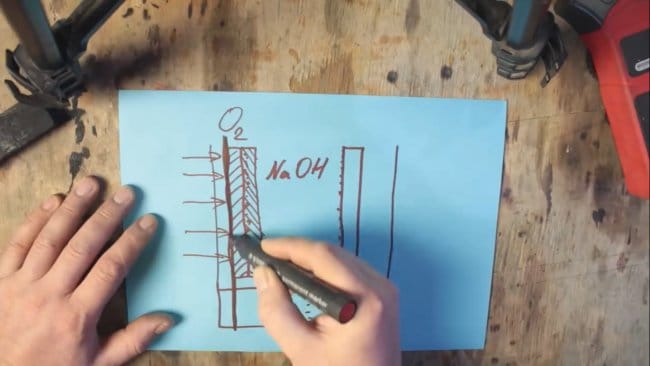
Оксид марганца с наночастицами благородного металла не вступает в реакцию, а действуют как катализатор, благодаря чему водород из электролита окисляется кислородом находящемся в воздухе.

Технологиями получения оксида марганца с включениями наночастиц серебра в принципе не сложна и его можно попробовать получить в кустарных условиях. Но в данной статье мы разберем как сделать максимально бюджетный вариант батареи, получающей энергию из алюминия. Дальнейшая инструкция взята с YouTube канала «Огненное ТВ». Более подробно в оригинальном видеоролике автора:
Максимально бюджетный вариант графита — это летние контактные вставки для троллейбусов. Их можно найти абсолютно бесплатно на конечных троллейбусных остановках, а можно и купить, стоят они не дорога, автор нашёл их в продаже по 22 рубля за штуку.

Далее нам потребуется щелочь. Вот такое средство для чистки труб в своем составе содержит стопроцентную натриевую щелочь.

Для запуска реакции щёлочи нам понадобится совсем чуть-чуть, будет достаточно 1г щёлочи на 0,5л воды.
Первым делом давайте проверим действительно ли в данной батареи нужно использовать графитовый электрод. Для опыта возьмем вот такой вот электрод из нержавеющей стали.

Теперь помещаем алюминиевую пластину и электрод из нержавейки в щелочь, подключаем мультиметр и смотрим сколько вольт получится.

Как видим, получилось примерно 1,4В. Теперь давайте проверим ток короткого замыкания.
Ток КЗ получился в районе 20мА. Какие можно сделать выводы: теоретически в экстремальных условиях возможно собрать батарею из нержавеющих кружек и алюминиевой фольги.

Следующий у нас будет медный электрод, выполненный из электротехнической меди.

Как можем наблюдать напряжение получилось чуть выше чем 1,4В, а вот ток короткого замыкания поначалу было высоким, но потом начал достаточно быстро проседать и медь к тому же начала покрываться темным налетом, скорее всего такой эффект вызвали примеси в воде, так как воду для этого эксперимента автор взял водопроводную, из-под крана.

Теперь погружаем в раствор электролита графитовый электрод.


С данным электродом получилось напряжение 1,3В, ток короткого замыкания остановился в районе 17мА. На первый взгляд кажется, что электрод из нержавеющей стали более эффективен, но площадь поверхности нержавеющего электрода больше, так что пока неизвестно что лучше графит или нержавейка.
Так как графит имеет достаточно большое сопротивление, нужно с ним как-то бороться. Необходимо изготовить электроды из хорошо проводящего ток материала, а графит должен быть только на его поверхности. Было решено просверлить графит насквозь, и в получившихся отверстиях нарезать резьбу под болты м6.
В итоге получился стальной электрод с графитовой оболочкой.

Сопротивление не просверленного графита составляет примерно 4.5Ом, а просверленного графита примерно 1,7 Ома.


На лицо уменьшение сопротивления, а, следовательно — эффективность конструкции возрастет. В дальнейших экспериментах будем использовать дистиллированную воду.
Первый эксперимент с электролитом, в котором 4г щелочи на 1л воды.


Ток короткого замыкания получился 150мА. Следующий электролит имеет концентрацию 6г щелочи на 1 литр. Ну и так далее, каждый раз будем увеличивать концентрацию на 2г пока не дойдем до концентрации, при которой ток не будет расти.


Даже несмотря на то, что у такая простая батарея обладает не большой отдачей по току, но зато такая батарея может работать очень долго, а в качестве электродов можно использовать любой алюминий, который легко переплавить в электроды любой формы, например, алюминиевые банки из-под различных алкогольных и безалкогольных напитков, фольга от шоколада и т.п.
В итоге, после всех проделанных экспериментах с различной концентрацией электролита, становится понятно, что при такой конструкции батареи не имеет смысла добавлять более 12г щелочи на 1 литр воды, то есть у нас получается примерно 1% раствор.


Затем автор собрал еще одну обойму, состоящую из 3-ех электродов.


Две батареи дают более высокое напряжение и потери меньше, поэтому и результат лучше.
А теперь возьмем ведро электролита, большой кусок алюминия и 2 электрода из нержавейки.
В ведре электролит концентрации 10г/1л. Пиковый ток 1,3А, просел он до 520мА. При всей огромной площади нержавейки с графитом она не сравнилась, потому что с графитом получилось 600мА. Кстати, в ходе реакции выделяется водород, который также можно собирать и использовать как источник энергии. Короче, есть куда расти. На этом пока все. Благодарю за внимание. До новых встреч!
Источник
 Доставка новых самоделок на почту
Доставка новых самоделок на почтуПолучайте на почту подборку новых самоделок. Никакого спама, только полезные идеи!
*Заполняя форму вы соглашаетесь на обработку персональных данных
Становитесь автором сайта, публикуйте собственные статьи, описания самоделок с оплатой за текст. Подробнее здесь.Воздушно-цинковый элемент — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 17 августа 2014; проверки требуют 18 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 17 августа 2014; проверки требуют 18 правок.| Воздушно-цинковый элемент | |
|---|---|
 Воздушно-цинковые элементы с цветовым кодированием | |
| Удельная энергоёмкость | 1350 Вт/ч/кг |
| Удельная энергоплотность | более 450 Вт/л |
| Удельная мощность | 5000 Вт/кг |
| Саморазряд | большой |
| Электродвижущая сила | 1,65 В |
| Рабочая температура | -20…+35 °С |
Воздушно-цинковый элемент — гальванический элемент, в котором в качестве анода используется — газовый (воздушный электрод), электролит — водный раствор гидроксида калия (либо растворы хлорида цинка), катод — цинк. Отличается весьма высокой удельной энергоёмкостью (выше чем у литий-ионных аккумуляторов[1]). Широкому распространению препятствует короткий срок эксплуатации, связанный с высыханием электролита, однако ведутся работы по устранению этого недостатка.
- Теоретическая энергоёмкость: 1350 Вт·ч/кг[2]
- Удельная энергоёмкость: более 450 Вт·ч/кг[3][4]
- Удельная энергоплотность(Вт·ч/дм³):
- Максимальная мощность: 5000 Вт/кг[5]
- ЭДС: 1.4-1.45 В [5]
- Рабочая температура: — 20…+35 °C.
| диаметр, мм | высота, мм | МЭК-код | Renata | Varta | Rayovac | Panasonic |
|---|---|---|---|---|---|---|
| 11,6 | 5,4 | PR44 | ZA675 | V675A | DA675 | PR675 |
| 7,9 | 5,4 | PR48 | ZA13 | V13A | DA13 | PR13 |
| 7,9 | 3,6 | PR41 | ZA312 | V312A | DA312 | PR312 |
| 5,9 | 3,6 | PR70 | ZA10 | V10 | DA230 | PR230 |
На катоде происходит реакция электровосстановления кислорода, продуктами которой являются отрицательно заряженные гидроксид-ионы:
O2 + 2H2O + 4e → 4OH–.
Гидроксид-ионы движутся в электролите к цинковому аноду, где происходит реакция окисления цинка с высвобождением электронов, которые через внешнюю цепь возвращаются на катод:
Zn + 4OH– → Zn(OH)42– + 2e.
Zn(OH)42– → ZnO + 2OH– + H2O.
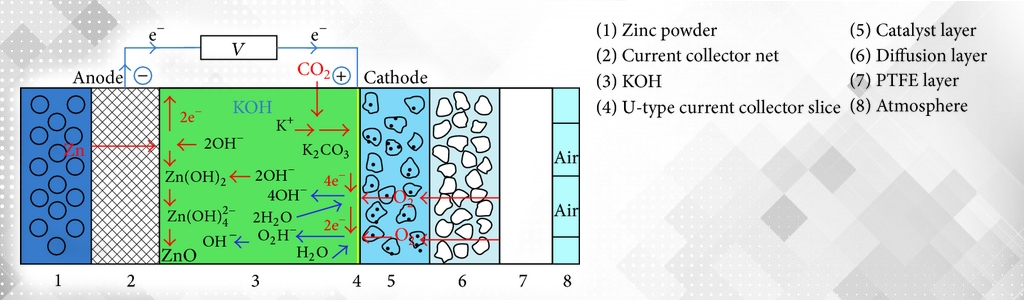
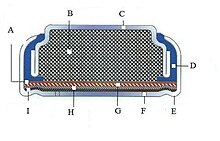 Схема поперечного сечения воздушно-цинкового элемента: A — сепаратор, B — анод (цинковый порошок), C — защитный кожух анода, D — изолятор, E — защитный кожух катода, F — отверстие для воздуха, G — катодный катализатор и коллектор тока, H — слой распределения воздуха, I — полупроницаемая мембрана
Схема поперечного сечения воздушно-цинкового элемента: A — сепаратор, B — анод (цинковый порошок), C — защитный кожух анода, D — изолятор, E — защитный кожух катода, F — отверстие для воздуха, G — катодный катализатор и коллектор тока, H — слой распределения воздуха, I — полупроницаемая мембранаКонструкция ячейки воздушно-цинкового элемента включает катод и анод, разделённые щелочным электролитом и механическими сепараторами. В качестве катода используется газодиффузный электрод (gas diffusion electrode, GDE), водопроницаемая мембрана которого позволяет получать кислород из циркулирующего через неё атмосферного воздуха. «Топливом» является цинковый анод, окисляющийся в процессе работы элемента, а окислителем — кислород, получаемый из поступающего через «дыхательные отверстия» атмосферного воздуха.
Одна из особенностей воздушно-цинкового элемента — относительно большой саморазряд. Однако воздушно-цинковый элемент не разряжается, пока катод не наполнится воздухом. Поэтому при хранении вентиляционное отверстие элементов закрывается герметизирующей наклейкой. На полную мощность элемент выходит приблизительно через минуту после удаления наклейки.
Применяется для питания слуховых аппаратов.
Производители и типы производимых аккумуляторов[править | править код]
Воздушно-цинковые элементы (Zinc-Air) – возможная альтернатива литию
Долгое время область применения воздушно-цинковых элементов питания не выходила за рамки медицины. Высокая емкость и длительный срок службы (в неактивном состоянии) позволили им беспрепятственно занять нишу одноразовых батареек для слуховых аппаратов. Но в последние годы наблюдается большой рост интереса к этой технологии у автопроизводителей. Некоторые считают, что нашлась альтернативу литию. Так ли это?
Воздушно-цинковая батарея для электромобиля может быть устроена следующим образом: в разделенную на отсеки емкость вставлены электроды, на которых адсорбируется и восстанавливается кислород воздуха, а также специальные съемные кассеты, заполненные расходным материалом анода, в данном случае гранулами цинка. Между отрицательными и положительными электродами прокладывается сепаратор. В качестве электролита может использоваться водный раствор гидроксида калия, либо раствор хлорида цинка.
Поступающий извне воздух с помощью катализаторов образует в водном растворе электролита гидроксильные ионы, которые окисляют цинковый электрод. В ходе данной реакции высвобождаются электроны, образующие электрический ток.
Преимущества
Мировые запасы цинка по некоторым оценкам составляют примерно 1.9 гигатонн. Если начать мировое производство металлического цинка сейчас, то уже через пару лет можно будет обеспечить сборку миллиарда воздушно-цинковых аккумуляторов емкостью 10 кВт*ч каждый. К примеру, для создания такого же количества литий-ионных батарей при нынешних условиях добычи лития потребуется более 180 лет. Доступность цинка позволит еще и снизить цену на аккумуляторные батареи.
Очень важно и то, что воздушно-цинковые элементы, имея прозрачную схему рециклирования отработанного цинка, являются экологически чистыми изделиями. Используемые здесь материалы не отравляют окружающую среду и могут быть отработанны вторично. Продукт реакции воздушно-цинковых элементов питания (оксид цинка) также абсолютно безопасен для человека и его среды обитания. Не зря оксид цинка применяется в качестве основного компонента для детской присыпки.
Главным же преимуществом, благодаря которому электромобилестроители смотрят на эту технологию с надеждой, является высокая плотность энергии (в 2-3 раза выше, чем у li-ion). Уже сейчас энергоемкость Zinc-Air достигает 450 Вт*ч/кг, но теоретическая плотность может составлять 1350 Вт*ч/кг!
Недостатки
Раз мы не ездим на электромобилях с воздушно-цинковыми батареями, значит, есть и недостатки. Во-первых, такие элементы сложно сделать перезаряжаемыми с достаточным количеством циклов разряда/заряда. В ходе работы воздушно-цинковой батареи электролит попросту высыхает, либо проникает слишком глубоко в поры воздушного электрода. А поскольку осаждающийся цинк распределяется неравномерно, образуя разветвленную структуру, между электродами нередко происходят короткие замыкания.
Ученые пытаются найти выход. Американская компания ZAI решила эту проблему простой заменой электролита и добавлением свежих картриджей с цинком. Естественно, для этого потребуется развитая инфраструктура заправочных станций, на которых будет происходить смена окисленного активного материала в анодной кассете на свежий цинк.
И хотя экономическая составляющая проекта пока не проработана, производители утверждают, что стоимость такой «зарядки» будет существенно ниже заправки машины с ДВС. Кроме того, процесс смены активного материала потребует не более 10 минут. Даже сверхбыстрые аккумуляторы SCiB за это же время смогут восполнить только 50% своего потенциала. В прошлом году корейская компания Leo Motors уже продемонстрировала воздушно-цинковые батареи ZAI на своем электрическом грузовике.
Работает над усовершенствованием Zinc-Air батареи и технологическая фирма из Швейцарии ReVolt. Она предложила специальные гелеобразующие и вяжущие добавки, контролирующие влажность и форму цинкового электрода, а также новые катализаторы, которые существенно улучшают работу элементов.
Все же инженерам обеих компаний так и не удалось преодолеть рубеж в 200 циклов разряда/заряда Zinc-Air. Поэтому говорить о воздушно-цинковых элементах, как об электромобильных батареях, пока рано.
Рекомендуем также статью о литий-воздушном аккумуляторе.
Элемент питания — самодельная батарейка и содовый выпрямитель +САМОДЕЛЬНЫЙ МЕДНО-КУПОРОСНЫЙ ЭЛЕМЕНТ. / Мастерская / НеПропаду
Буэнос диас камрады, в особенности рукастые… На сайте както мелькала конструкция самодельной батарейки, но не совсем функциональной… А тут мне на глаза попалась книженция 1956го года (считавшаяся потерянной) так что спешу поделится парой конструкций…
САМОДЕЛЬНЫЙ УГОЛЬНО-ЦИНКОВЫЙ ЭЛЕМЕНТ
Простой элемент можно собрать в стеклянной пол-
литровой банке из-под консервов, внутри которой поме-
щают электроды — уголь и цинк. Положительный элект-
род такого элемента делают из угольного стержня
длиною .12 — 15 см, изготовленного из старого угля от
проекционного, или кинофонаря. В крайнем случае
можно применить уголь от старой батарейки для кар-
манного фонарика или любого старого угольно-цинко-
вого элемента.
К угольному стержню с помощью хомутика и винта
с гайкой прикрепляется гибкий провод. Угольный
электрод устанавливают в центре мешочка, напол-
ненного толченым углем, смешанным с перекисью
марганца и нашатыря. Их можно приобрести в
аптеке.
Смесь заливают водой так, чтобы получилась густая
кашица.
Кашицу плотно набивают в мешочек, сшитый из
плотной материи — бязи или холста. Диаметр мешочка
5- 5,5 см. Длина его на 1 см короче длины угольного
стержня.
Отрицательный электрод изготовляют в виде цин-
кового цилиндра без дна диаметром 6 —.6,5 см, рав-
ным длине мешочка. К цинковому электроду припаи-
вают гибкую проволоку длиною 15 — 20 см. Цилиндр.
опускают в стеклянную банку, туда.же опускают мешо-
чек. Чтобы мешочек не касался дна банки, на кото-.
ром будут осаждаться нерастворившиеся частички
-электролита, положите на дно банки прокладку, сде-
ланную из двух перекрещенных палочек, пропитанных
парафином. Между мешочком и цинком также вставьте
несколько деревянных палочек, покрытых парафином
или воском.
Теперь элемент можно залить электролитом. Для при-
готовления’ электролита 120 граммов кристаллического
нашатыря растворяют в 1 литре теплой воды. Остыв-
ший раствор заливают вбанку и дают ему время
(около полутора часов) впитаться в смесь мешочка,
после чего раствор доливают так, чтобы электро-
лит закрывал мешочек на1 — 1,5 см.
.Сверху банку, в которуюпомещен элемент, закройте
картонной или фанернойкрышкой. Для крышки вы-
режьте два кружочка: один по внутреннему и один по
внешнему диаметру банки и скрепите их- между со-
бой. В крышке шилом сде-лайте два отверстия для
вывода’ проводов (рис. 20).Вместо стеклянной банки
можно употребить глиняную или изготовить банку
из цинка, но тогда ей удоб-нее придать не круглую,
а четырехугольную форму.
Если место закрепления
хомутика будет окисляться, то следует снять хомутик,
очистить уголь, снова закрепить хомутик и покрыть
эту часть угля (вместе с хомутиком) воском или
парафином.

САМОДЕЛЬНЫЙ СОДОВЫЙ ВЫПРЯМИТЕЛЬ
Работа такого выпрямителя основана на односто-
ронней проводимости тока от железной пластинки
к алюминиевой, если их поместить в раствор соды.
Выпрямитель собирают в стеклянной банке из-под
консервов, в бутылке с широким горлышком или в гли-
няном сосуде. Электроды изготовляют из листового
железа и алюминия толщиною 0,5 — 1 мм.
Для железного электрода вырезают пластинку ши-
риною около 2,5 см и длиною — по высоте сосуда. Из
. алюминия вырезают пластинку такой же длины, но
шириною 1 см.
Пластинки прикрепляют к деревянной крышке, сде-
ланной из нетолстой дощечки или фанеры, Для крышки
вырезают две круглые дощечки: диаметр одной на 1—
1,5 см больше диаметра отверстия банки,, а другой,
наоборот, меньше на О,5 — 1 см, чем отверстие банки.
Обе~дощечки сколачивают гвоздиками. Края крышки
выравнивают напильником или наждачной бумагой
(шкуркой).
Посредине крышки на расстоянии 3 см друг от
друга ножом прорезают два отверстия, равные ширине
пластинок. В отверстия пропускают верхние концы
пластинок так, чтобы нижние не касались дна банки.
Выведенные наружу концы отгибают под прямым
углом в разные стороны. Предварительно в них ши-
лом или гвоздем пробивают по два отверстия для шу-
. рупов.
Каждую из пластинок прикрепляют к крышке двумя
шурупами. Ближний к сгибу шуруп, служащий для
крепления, сразу завинчивают до конца, а другой
предназначен для подключения соединительных прово-
дов, — под его головку нужно положить шайбу.
Теперь банку можно наполнить электролитом. Для
этого налейте в банку воду (если есть, лучше
дистиллированную) и приготовьте насыщенный раствор
питьевой соды.
При составлении электролита для лучшего раство-
рения соды рекомендуем воду все время мешать или
взбалтывать легким встряхиванием банки. Соду можно
приобрести в любой аптеке или аптекарском магазине.
Для раствора понадобится 20 — 25 граммов нормальной
питьевой соды.
После приготовления электролита крышку с при-
крепленными к. ней электродами надевают на банку, и
сборка выпрямителя закончена.
Для работы выпрямитель включают последовательно
с приборами, применяемыми для опыта. Как это сделать,
показано на рисунке- 28.
Выпрямитель хорошо работает при непродолжитель-
ных включениях по 10 — 15 минут, после чего требует
кратковременного перерыва — выключения на 5 — 7 ми-
нут. При продолжительных включениях без перерыва
электролит может нагреться и выпрямление прекратится.
При работе нужно учитывать, что ток; проходящий
через выпрямитель,.теряет примерно половину своего
первоначального напряжения,
При изготовлении выпрямителя в бутылке пластинки
(электроды) прижимают пробкой, а на выходящих на-
ружу концах укрепляют зажимы. Проследите за тем,
чтобы пластинки в таком выпрямителе не соприкасались
друг с другом.
ВЫПРЯМИТЕЛЬ-РЕОСТАТ
Электролитические выпрямители нашей конструкции
удобны и тем, что их можно использовать как реостат.
Сопротивление такого реостата для снятия тока боль-
шей или меньшей силы можно изменять, уменьшая или
увеличивая расстояние между электродами внутри
банки, или выдвигая одну из пластин наружу.
Добавлю копипаста…
САМОДЕЛЬНЫЙ МЕДНО-КУПОРОСНЫЙ ЭЛЕМЕНТ.

Ниже описана подробная информация по изготовлению самодельного медно-купоросного элемента, а моя сборка, это быстрая, грубая сборка, которая наглядно показывает работу медно-купоросного элемента.Как видно из фото элементы сделаны по ниже описанной схеме, но с грубыми нарушениями, но как показала практика, и такие элементы объединенные в батарею, способны питать светодиодные фонари и заряжать мобильные телефоны.В этой самодельной конструкции из-за недоступности чистого цинка, применён алюминиевый электрод, но э.д.с.алюминия ниже чем у цинка, составляет 0,6 В, то есть одна банка даёт 0,6 вольт, из-за этого прибор состоит не из 4-х банок, а из 6-ти, чтобы получить 3,6 вольт.
При испытании данного прибора не было никаких измерительных приборов, но как видно из фото, прибор свободно обеспечивает свечение 12-ти светодиодов-ток потребления 200мА, и заряжает мобильный телефон-ток потребления 400мА.
При испытании элемент зарядил батарею телефона ёмкостью 750мА за 1,40 минут.
Примерные технические характеристики батареи элементов, состоящей из 6-ти банок, емкостью 0,33л.: 3,7Вольт, ток замыкания около 500мА, ёмкость 25-30А/ч.
В ходе испытания батарея элементов стабильно проработала на одной столовой ложке купороса около 100 часов при токе разряда примерно 200мА/ч, сейчас прибор так-же работает, но сила тока значительно меньше и составляет около 80мА/ч, купорос практически истрачен, таким образом если посчитать, то можно определить, сколько времени вообще элементы проработают на определённом количестве купороса, питая определенные приборы.
ПОРЯДОК ИЗГОТОВЛЕНИЯ.





В ЭТОЙ КОНСТРУКЦИИ В КАЧЕСТВЕ АЛЮМИНИЕВОГО ЭЛЕКТРОДА ИСПОЛЬЗОВАЛИСЬ, АЛЮМИНИЕВЫЕ БАНКИ (ПИВНЫЕ), И ДРУГИЕ ИЗДЕЛИЯ ИЗ АЛЮМИНИЯ, ЕСЛИ БУДУТ ИСПОЛЬЗОВАТЬСЯ АЛЮМИНИЕВЫЕ БАНКИ, ТО ИХ НУЖНО ТЩАТЕЛЬНО ЗАЧИСТИТЬ ОТ ЗАЩИТНОГО, ВНУТРЕННЕГО СЛОЯ, И ВНЕШНИХ НАДПИСЕЙ, ТАК КАК ОНИ НЕ ПРОПУСКАЮТ ТОК.
МЕДНО-ЦИНКОВЫЕ ГАЛЬВАНИЧЕСКИЕ ЭЛЕМЕНТЫ С МЕДНЫМ КУПОРОСОМ.
Эти элементы чаще всего применялись для питания радиолюбительской аппаратуры, так как они наиболее просты в изготовлении, и обладают устойчивым напряжением по сравнению с другими химическими источниками питания, и практически почти не поляризуются.Кроме того они очень дёшевы и удобны в эксплуатации.Благодаря этим качествам они получили широкое распространение и применение в радиолюбительской среде прошлых лет.Сейчас же когда портативная электроника стала очень экономична, такие химические источники питания могут обеспечивать, как зарядку телефонов, фонарей, к примеру на даче, так и автономное, длительное питание КПК, телефонов, светодиодных фонарей, светильников.Простейшие медно-купоросные элементы собираются обычно в среклянных банках объемом в 0,5-1 литр.
ПОРЯДОК ИЗГОТОВЛЕНИЯ.
Сначала внутренняя поверхность банки обмазывается вазелином или салом на расстоянии 3-4 сантиметра от верхнего края банки, это делается для того чтобы предупредить выползание кристаллов солей из сосуда элемента.Далее из тонкого листа меди, или латуни или свинца изготавливается цилиндр по внутреннему диаметру и высоте банки.Далее в цилиндре надо с одной стороны сделать двойные прорези на глубину 4-5 мм., и получившиеся скобки загнуть наружу, для того что-бы цилиндр весел на них, на горлышке банки, не доходя до дна банки на 5 см., после изготовления припаять к нему медный провод, это и будет (+).Далее изготавливается диафрагма, диафрагма изготавливается из картона, делается цилиндр из картона по длине банки, или короче банки на 5 см., а потом к нему пришивается нитками картонное дно, так что-бы не оставалось щелей, а места сшивки пропитываются горячим парафином чтобы герметизировать дно от вытекания жидкости.Далее на цилиндр плотно наматывают несколько слоёв пергамента или газетной бумаги, предварительно вымоченного в солёном растворе, чтобы не оставалось воздушных прослоек, а после получившейся «стакан» плотно обшивается обёрнутой в несколько слоёв тканью, для механической прочности.Потом на верх диафрагмы наклеивают или пришивают кольцо, чтобы стакан не проваливался, и места крепления обмазывают горячим парафином, в кольце делают отверстие, через которое в банку наливается вода и вставляется мешалка для помешивания купороса.Потом в диафрагму надо налить раствор поваренной соли и оставить на несколько часов, правильно собранная диафрагма не должна подтекать, а её поверхность должна быть всего-лишь влажной.далее по внутреннему диаметру диафрагмы изготавливается из листа цинка цилиндр к нему припаивается медный провод который будет служить (-), цинковый цилиндр должен свободно входить в диафрагму, но при этом быть как можно ближе к её стенкам, то есть ближе к медному цилиндру, чтобы уменьшить внутренне сопротивление, и соответственно повысить эффективность.
СБОРКА ЭЛЕМЕНТА.
В чистую банку, если 0,5л., насыпают столовую ложку медного купороса, вставляют мешалку, а потом устанавливают диафрагму, наполненную раствором поваренной соли, после в то отверстие, которое для мешалки, в банку наливается вода, а за тем вставляется в диафрагму цинковый цилиндр, после сборки элемент полностью готов к работе, остаётся соединить элементы последовательно, как обычные батарейки, и питать и заряжать приборы.Применение пористой диафрагмы обусловлено разделением электролитов, тоесть разделением кристаллов купороса, и соляного раствора от смешивания, иначе купорос бурно вступает в реакцию и слишком быстро расходуется, даже когда элемент не используется, а через диафрагму расход купороса равномерен и экономичен, что обеспечивает долгую работу источника тока-гальванического элемента…
Удод за элементом заключается в периодической заправке купороса, смене электролита и очистке от окисления электродов. При потреблении тока около 600мА(сотовый телефон), батарея состоящая из 4-х пол-литровых элементов элементов проработает на одной заправке купороса(4 стол.л.) около месяца, при условии использования его каждый день около 6 часов..При падении мощности периодически мешалкой надо взбалтывать медный купорос.За время работы в течении месяца израсходуется около 100г.купороса, и 40г. цинка,
примечание.если заменить цинк на алюминий, то элементов надо не 4 или 5, а 6 или 7, соединенных последовательно, так как э.д.с. алюминия ниже чем у цинка, и состовляет 0,4-0,6V…
Взято отсюда.
soliaris2010.narod2.ru/dobicha_elektroenergii_-primitivnii_istochnik_.html
Воздушно-цинковый аккумулятор готовится к массовому

В MGX Minerals усовершенствовали аккумулятор на основе воздушно-цинкового топливного элемента (Zinc-air Fuel Cell), создав регенеративную батарею следующего поколения. Её главное преимущество — отсутствие высокозатратных материалов, таких как литий, ванадий и кобальт.
Проектом занимается дочернее предприятие MGX Minerals — ZincNyx Energy Solutions. Учёные предложили новые методы увеличения ёмкости аккумулятора. Более того, они уже готовы начать массовое производство. Для этого нужно провести ещё немного доработок под актуальные на рынке электронные устройства, включая электромобили и смартфоны.
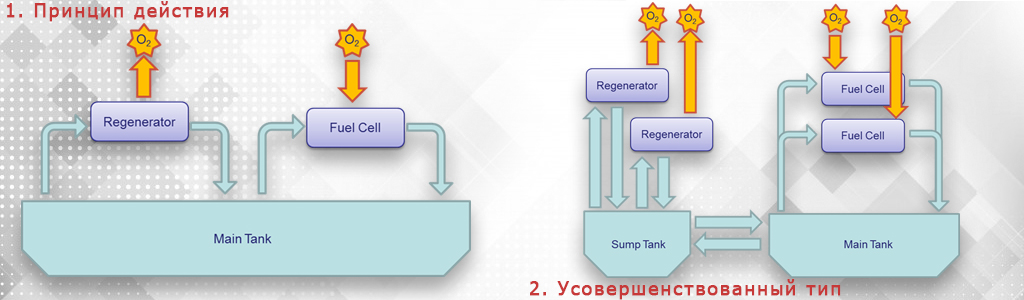
Что такое воздушно-цинковый аккумулятор ZincNyx?
Батарея нового типа использует поток цинкового воздуха. Она хранит энергию в виде частиц цинка, что позволяет избавиться от дорогостоящего лития в химическом составе ячейки. Производство подобных элементов будет намного дешевле.
В отличие от обычных батарей, которые имеют фиксированное соотношение ёмкости и мощности, технология ZincNyx использует систему по типу «топливного бака» c гибким сочетанием ёмкости и мощности.
Объем хранилища энергии напрямую зависит от размера топливного бака и количества перезаряжаемого цинкового топлива. Производители смогут выбирать наиболее подходящее для их электроники сочетание и масштабировать аккумулятор под разные цели.
Ещё одним важным преимуществом воздушно-цинковой батареи является способность заряжаться и разряжаться одновременно вне зависимости от типа зарядного устройства (быстрого, маломощного или постоянного). Каждая из схем, отвечающая за подзарядку и разгрузку ёмкости, размещены отдельно и независимо друг от друга.
Для сравнения, сегодняшние аккумуляторы обладают ограниченным максимальным зарядом и разрядом с учётом общего количества ячеек — у нихе нет разделения компонентов заряда, разряда и хранения энергии.
Как работает воздушно-циновый аккумулятор?
Процесс подробно показан на видео в разделе технологий ZincNyx здесь. Базовая система включает в себя несколько компонентов.
Из чего состоит воздушно-цинковая батарея?
• Регенератор
• Основная ёмкость (бак)
• Топливный элемента
Когда система перезаряжается, электрическая мощность используется в блоке регенератора для получения мелких частиц цинка внутри электролита-носителя. Пока система продолжает заряжаться, частицы цинка собираются в главный резервуар, окруженный общим электролитом. В результате кислород высвобождается.
Cистема генерирует энергию, и частицы цинка доставляются из основного бака в топливный элемент в электролите канала-носителя. Частицы цинка объединены с кислородом, выведенным из воздуха, и электрическая мощность подаётся в нагрузку.
Опытные образцы новой батареи сперва появятся в Северной Америке. Точные сроки пока не называются — MGX Minerals пока ещё работает с инвесторами для подготовки к массовому производство. Но до тех пор традиционные аккумуляторы останутся единственным практичным вариантом для телефонов, планшетов, ноутбуков и других устройств. На них распространяется гарантия 12 месяцев — позвоните по бесплатному телефону для поиска интересующей вас батареи: 8 800 555-86-57 (круглосуточно) или оставьте заявку в нашем интернет-магазине.



