Галогены — это… Что такое Галогены?
 | В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 14 декабря 2011. |
| Группа → | 17 (VIIA) | ||||||
|---|---|---|---|---|---|---|---|
| ↓ Период | |||||||
| 2 | |||||||
| 3 | |||||||
| 4 | |||||||
| 5 | |||||||
| 6 |
| ||||||
| 7 |
| ||||||
Галоге́ны (от греч. ἁλός — соль и γένος — рождение, происхождение; иногда употребляется устаревшее название гало́иды) — химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева (по устаревшей классификации — элементы главной подгруппы VII группы)[1].
Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители, поэтому встречаются в природе только в виде соединений. С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F
К галогенам относятся фтор F, хлор Cl, бром Br, иод I, астат At, а также (формально) искусственный элемент унунсептий Uus.
| Фтор F | Хлор Cl | Бром Br | Иод I |
|---|---|---|---|
 |  |  |
Все галогены — неметаллы. На внешнем энергетическом уровне 7 электронов, являются сильными окислителями. При взаимодействии с металлами возникает ионная связь, и образуются соли. Галогены, (кроме F) при взаимодействии с более электроотрицательными элементами, могут проявлять и восстановительные свойства вплоть до высшей степени окисления +7.
Распространённость элементов и получение простых веществ
Как уже было сказано выше, галогены имеют высокую реакционную способность, поэтому встречаются в природе обычно в виде соединений.
Их распространённость в земной коре уменьшается при увеличении атомного радиуса от фтора к иоду. Количество астата в земной коре измеряется граммами, а унунсептий в природе отсутствует. Фтор, хлор, бром и иод производятся в промышленных масштабах, причем хлор производится в гораздо больших количествах.
В природе эти элементы встречаются в основном в виде галогенидов (за исключением иода, который также встречается в виде иодата натрия или калия в месторождениях нитратов щелочных металлов). Поскольку многие хлориды, бромиды и иодиды растворимы в воде, то эти анионы присутствуют в океане и природных рассолах. Основным источником фтора является фторид кальция, который очень малорастворим и находится в осадочных породах (как флюорит CaF2).
Основным способом получения простых веществ является окисление галогенидов. Высокие положительные стандартные электродные потенциалы E
В промышленности хлор в основном получают электролизом водного раствора хлорида натрия в специальных электролизёрах. При этом протекают следующие реакции:
полуреакция на аноде:
полуреакция на катоде:
Окисление воды на аноде подавляется использованием такого материала электрода, который имеет более высокое перенапряжение по отношению к O2, чем к Cl2 (таким материалом оказался катодное и анодное пространства разделены полимерной ионообменной мембраной. Мембрана позволяет катионам Na+ переходить из анодного пространства в катодное. Переход катионов поддерживает электронейтральность в обеих частях электролизёра, так как в течение электролиза отрицательные ионы удаляются от анода (превращение 2Cl
Бром получают химическим окислением бромид-иона, находящегося в морской воде. Подобный процесс используется и для получения иода из природных рассолов, богатых I−. В качестве окислителя в обоих случаях используют хлор, обладающий более сильными окислительными свойствами, а образующиеся Br2 и I2 удаляются из раствора потоком воздуха.
Физические свойства галогенов
Фтор является трудносжижаемым, а хлор легкосжижаемым газом с удушливым резким запахом. Энергия связи галогенов сверху вниз по ряду изменяется не равномерно. Фтор имеет аномально низкую энергию связи (151 кДж/моль), это объясняется тем, что фтор не имеет
| Простое вещество | Температура плавления, °C | Температура кипения, °C |
| F | −220 | −188 |
| Cl2 | −101 | −34 |
| Br2 | −7 | 58 |
| I2 | 113,5 | 184,885 |
| At2 | 244 | 309[2] |
Химические свойства галогенов
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к астату. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например:
- 2Al + 3F2 = 2AlF3 + 2989 кДж,
- 2Fe + 3F
Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р) — все реакции при этом сильно экзотермические, например:
- Н2 + F2 = 2HF + 547 кДж,
- Si + 2F2 = SiF4(г) + 1615 кДж.
При нагревании фтор окисляет все другие галогены по схеме
- Hal2 + F2 = 2НalF
где Hal = Cl, Br, I, At, причем в соединениях HalF степени окисления хлора, брома, иода и астата равны +1.
Наконец, при облучении фтор реагирует даже с инертными (благородными) газами:
- Хе + F2 = XeF2 + 152 кДж.
Взаимодействие фтора со сложными веществами также протекает очень энергично. Так, он окисляет воду, при этом реакция носит взрывной характер:
- 3F2 + ЗН2О = OF2↑ + 4HF + Н2О2.
Свободный хлор также очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов. Для сравнения приведем уравнения реакций хлора с теми же простыми веществами, что и для фтора:
- 2Al + 3Cl2 = 2AlCl3(кр) + 1405 кДж,
- 2Fe + ЗCl2 = 2FeCl3(кр) + 804 кДж,
- Si + 2Cl2 = SiCl4(Ж) + 662 кДж,
- Н2 + Cl2 = 2HCl(г)+185кДж.
Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует с водородом, тогда как при нагревании или при освещении (например, на прямом солнечном свету) эта реакция протекает со взрывом по приведенному ниже цепному механизму:
- Cl2 + hν → 2Cl,
- Cl + Н2 → HCl + Н,
- Н + Cl2 → HCl + Cl,
- Cl + Н2 → HCl + Н и т. д.
Возбуждение этой реакции происходит под действием фотонов (hν), которые вызывают диссоциацию молекул Cl2 на атомы — при этом возникает цепь последовательных реакций, в каждой из которых появляется частица, инициирующая начало последующей стадии.
Реакция между Н2 и Cl2 послужила одним из первых объектов исследования цепных фотохимических реакций. Наибольший вклад в развитие представлений о цепных реакциях внёс русский учёный, лауреат Нобелевской премии (1956 год) Н. Н. Семёнов.
Хлор вступает в реакцию со многими сложными веществами, например замещения и присоединения с углеводородами:
- СН3-СН3 + Cl2 → СН3-СН2Cl + HCl,
- СН2=СН2 + Cl2 → СН2Cl — СН2Cl.
Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
- Cl2 + 2HBr = 2HCl + Br2,
- Cl2 + 2HI = 2HCl + I2,
- Cl2 + 2KBr = 2KCl + Br2,
а также обратимо реагирует с водой:
- Cl2 + Н2О = HCl + HClO — 25 кДж.
Хлор, растворяясь в воде и частично реагируя с ней, как это показано выше, образует равновесную смесь веществ, называемую хлорной водой.
Заметим также, что хлор в левой части последнего уравнения имеет степень окисления 0. В результате реакции у одних атомов хлора степень окисления стала −1 (в HCl), у других +1 (в хлорноватистой кислоте HOCl). Такая реакция — пример реакции самоокисления-самовосстановления, или диспропорционирования.
Хлор может таким же образом реагировать (диспропорционировать) со щелочами:
- Cl2 + 2NaOH = NaCl + NaClO + Н2О (на холоде),
- 3Cl2 + 6КОН = 5KCl + KClO3 + 3Н2О (при нагревании).
Химическая активность брома меньше, чем у фтора и хлора, но все же достаточно велика в связи с тем, что бром обычно используют в жидком состоянии и поэтому его исходные концентрации при прочих равных условиях больше, чем у хлора.
Для примера приведем реакции взаимодействия брома с кремнием и водородом:
- Si + 2Br2 = SiBr4(ж) + 433 кДж,
- Н2 + Br2 = 2HBr(г) + 73 кДж.
Являясь более «мягким» реагентом, бром находит широкое применение в органической химии.
Отметим, что бром, так же, как и хлор, растворяется в воде, и, частично реагируя с ней, образует так называемую «бромную воду», тогда как иод практически в воде не растворим и не способен её окислять даже при нагревании; по этой причине не существует «иодной воды». Но иод способен растворяться в растворах иодидов с образованием комплексных анионов:
- I2 + I− → I−3.
Образующийся раствор называется раствором Люголя.
Иод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании. Взаимодействие же иода с водородом происходит только при сильном нагревании, реакция является эндотермической и сильно обратимой:
Н2 + I2 = 2HI — 53 кДж.
Таким образом, химическая активность галогенов последовательно уменьшается от фтора к астату. Каждый галоген в ряду F — At может вытеснять последующий из его соединений с водородом или металлами, то есть каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов. Астат ещё менее реакционноспособен, чем иод. Но и он реагирует с металлами (например с литием):
- 2Li + At2 = 2LiAt — астатид лития.
А при диссоциации образуются не только протоны, но и ионы At+:HAt диссоц. на:2HAt=H++At—+H—+At+.
Примечания
- ↑ Таблица Менделеева на сайте ИЮПАК
- ↑ Редкол.:Кнунянц И. Л. (гл. ред.) Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1988. — Т. 1. — С. 211. — 623 с. — 100 000 экз.
Общая характеристика галогенов — урок. Химия, 8–9 класс.
Общая характеристика элементов
Галогены — элементы \(VIIA\) группы периодической системы: фтор F, хлор Cl, бром Br, иод I и астат At.
Астат является радиоактивным элементом и встречается в природе редко.
Все галогены относятся к неметаллам.
В атомах галогенов на внешнем энергетическом уровне находится по \(7\) электронов:
F +9)2)7
Cl +17)2)8)7
Br +35)2)8)18)7
I +53)2)8)18)18)7
Валентные электроны галогенов образуют три электронные пары, а один электрон внешнего энергетического уровня остаётся неспаренным.
С возрастанием порядкового номера от фтора к иоду увеличиваются радиусы атомов, снижается их электроотрицательность. Значит, неметаллические свойства галогенов по группе сверху вниз ослабевают.
До завершения внешнего электронного слоя атомам галогенов не хватает только одного электрона, поэтому им наиболее характерна степень окисления \(–1\).
У фтора электроотрицательность больше, чем у остальных элементов, и поэтому степень окисления \(–1\) — его единственная возможная степень окисления в соединениях.
Атомы других галогенов способны также и отдавать валентные электроны, проявляя при этом положительные степени окисления \(+1\), \(+3\), \(+5\), \(+7\). Так, положительные степени окисления атомы хлора проявляют в соединениях с более электроотрицательными фтором, кислородом и азотом.
Галогены образуют с металлами соединения с ионной связью, а с другими неметаллами — соединения с ковалентной полярной связью.
Общая характеристика простых веществ
Атомы галогенов соединяются попарно и образуют двухатомные молекулы: F2, Cl2, Br2, I2.
Связь в молекулах ковалентная неполярная, одинарная. Кристаллическая решётка — молекулярная. Поэтому у галогенов невысокие температуры кипения и плавления.
При обычных условиях фтор представляет собой светло-жёлтый газ, хлор — жёлто-зелёный газ, бром — красно-коричневую жидкость, иод — тёмно-фиолетовые кристаллы.
Фтор

Хлор

Бром
Иод
Твёрдый иод при нагревании легко возгоняется (переходит в газообразное состояние и обратно в твёрдое, не превращаясь в жидкость).
Возгонка иода
У всех галогенов — резкий неприятный запах, и они очень токсичны.
В ряду галогенов с увеличением относительной молекулярной массы возрастают температуры кипения и плавления, увеличивается плотность, более интенсивной становится окраска.
В воде галогены растворяются слабо.
Фтор с водой вступает в химическую реакцию и вытесняет из неё кислород:
2F2+2h3O=4HF+O2↑.
Хлор — Википедия
| Хлор | |
|---|---|
| ← Сера | Аргон → | |
 Жидкий хлор в запаянном сосуде | |
| Название, символ, номер | Хлор / Chlorum (Cl), 17 |
| Атомная масса (молярная масса) | [35,446; 35,457][комм 1][1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ne] 3s2 3p5 |
| Радиус атома | 99 пм |
| Ковалентный радиус | 102±4 пм |
| Радиус иона | (+7e)27 (-1e)181 пм |
| Электроотрицательность | 3,16 (шкала Полинга) |
| Электродный потенциал | 0 |
| Степени окисления | 7, 6, 5, 4, 3, 1, 0, −1 |
| Энергия ионизации (первый электрон) | 1254,9(13,01) кДж/моль (эВ) |
| Плотность (при н. у.) | 3,21 г/л; (жид. при −35 °C) 1,557 г/см3; (тв. при −105 °C) 1,9 г/см³ |
| Температура плавления | 172,2К; −100,95 °C |
| Температура кипения | 238,6К; −34,55 °C |
| Критическая точка | 416,9 К, 7,991 МПа |
| Уд. теплота плавления | 6,41 кДж/моль |
| Уд. теплота испарения | 20,41 кДж/моль |
| Молярная теплоёмкость | 21,838[2] Дж/(K·моль) |
| Молярный объём | 18,7 см³/моль |
| Структура решётки | орторомбическая |
| Параметры решётки | a=6,29 b=4,50 c=8,21 Å |
| Теплопроводность | (300 K) 0,009 Вт/(м·К) |
| Номер CAS | 7782-50-5 |
 | |
Хлор (от греч. χλωρός — «жёлто-зелёный») — химический элемент с атомным номером 17[3]. Принадлежит к 17-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA), находится в третьем периоде таблицы. Атомная масса элемента 35,446…35,457 а. е. м.[1] [комм 1]. Обозначается символом Cl (от лат. Chlorum). Химически активный неметалл. Входит в группу галогенов.
Простое вещество хлор при нормальных условиях — ядовитый газ желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом. Молекула хлора двухатомная (формула Cl2).
Соединение с водородом — газообразный хлороводород — был впервые получен Джозефом Пристли в 1772 г. Хлор был получен в 1774 г. шведским химиком Карлом Вильгельмом Шееле, описавшим его выделение при взаимодействии пиролюзита с соляной кислотой в своём трактате о пиролюзите:
- 4HCl+MnO2→MnCl2+Cl2↑+2h3O{\displaystyle {\mathsf {4HCl+MnO_{2}\rightarrow MnCl_{2}+Cl_{2}\uparrow +2H_{2}O}}}
Шееле отметил запах хлора, схожий с запахом царской водки, его способность взаимодействовать с золотом и киноварью, а также его отбеливающие свойства. Однако Шееле, в соответствии с господствовавшей в химии того времени теорией флогистона, предположил, что хлор представляет собой дефлогистированную муриевую (соляную) кислоту. Бертолле и Лавуазье в рамках кислородной теории кислот обосновали, что новое вещество должно быть оксидом гипотетического элемента мурия. Однако попытки его выделения оставались безуспешными вплоть до работ Г. Дэви, которому электролизом удалось разложить поваренную соль на натрий и хлор, доказав элементарную природу последнего.
В 1811 г. Дэви предложил для нового элемента название «хлорин» (chlorine). Спустя год Ж. Гей-Люссак «сократил» название до хлора (chlore). В том же 1811 г. немецкий физик Иоганн Швейгер предложил для хлора название «галоген» (дословно солерод), однако впоследствии этот термин закрепился за всей 17-й (VIIA) группой элементов, в которую входит и хлор[4].
В 1826 году атомная масса хлора была с высокой точностью определена шведским химиком Йёнсом Якобом Берцелиусом (отличается от современных данных не более, чем на 0,1 %)[5].
В природе встречаются два изотопа хлора 35Cl и 37Cl. В земной коре хлор самый распространённый галоген. Хлор очень активен — он непосредственно соединяется почти со всеми элементами периодической системы. Поэтому в природе он встречается только в виде соединений в составе минералов: галита NaCl, сильвина KCl, сильвинита KCl·NaCl, бишофита MgCl2·6Н2О, карналлита KCl·MgCl2·6Н2O, каинита KCl·MgSO4·3Н2О. Самые большие запасы хлора содержатся в составе солей вод морей и океанов (содержание в морской воде 19 г/л[6]). На долю хлора приходится 0,025 % от общего числа атомов земной коры; кларковое число хлора — 0,017 %. Человеческий организм содержит 0,25 % ионов хлора по массе. В организме человека и животных хлор содержится в основном в межклеточных жидкостях (в том числе в крови) и играет важную роль в регуляции осмотических процессов, а также в процессах, связанных с работой нервных клеток.
В природе встречаются 2 стабильных изотопа хлора: с массовым числом 35 и 37. Доли их содержания соответственно равны 75,78 % и 24,22 %[7]. Свойства стабильных и некоторых радиоактивных изотопов хлора перечислены в таблице:
| Изотоп | Относительная масса, а. е. м. | Период полураспада | Тип распада | Ядерный спин |
|---|---|---|---|---|
| 35Cl | 34,968852721 | Стабилен | — | 3/2 |
| 36Cl | 35,9683069 | 301 тыс. лет | β-распад в 36Ar | 0 |
| 37Cl | 36,96590262 | Стабилен | — | 3/2 |
| 38Cl | 37,9680106 | 37,2 минуты | β-распад в 38Ar | 2 |
| 39Cl | 38,968009 | 55,6 минуты | β-распад в 39Ar | 3/2 |
| 40Cl | 39,97042 | 1,38 минуты | β-распад в 40Ar | 2 |
| 41Cl | 40,9707 | 34 c | β-распад в 41Ar | |
| 42Cl | 41,9732 | 46,8 c | β-распад в 42Ar | |
| 43Cl | 42,9742 | 3,3 c | β-распад в 43Ar |

При нормальных условиях хлор — жёлто-зелёный газ с удушающим запахом. Некоторые его физические свойства представлены в таблице.
| Свойство | Значение[8] |
|---|---|
| Цвет (газ) | Жёлто-зелёный |
| Температура кипения | −34 °C |
| Температура плавления | −100 °C |
| Температура разложения (диссоциации на атомы) | ~1400 °C |
| Плотность (газ, н.у.) | 3,214 г/л |
| Сродство к электрону атома | 3,65 эВ |
| Первая энергия ионизации | 12,97 эВ |
| Теплоёмкость (298 К, газ) | 34,94 Дж/(моль·K) |
| Критическая температура | 144 °C |
| Критическое давление | 76 атм |
| Стандартная энтальпия образования (298 К, газ) | 0 кДж/моль |
| Стандартная энтропия образования (298 К, газ) | 222,9 Дж/(моль·K) |
| Энтальпия плавления | 6,406 кДж/моль |
| Энтальпия кипения | 20,41 кДж/моль |
| Энергия гомолитического разрыва связи Х—Х | 243 кДж/моль |
| Энергия гетеролитического разрыва связи Х—Х | 1150 кДж/моль |
| Энергия ионизации | 1255 кДж/моль |
| Энергия сродства к электрону | 349 кДж/моль |
| Атомный радиус | 0,073 нм |
| Электроотрицательность по Полингу | 3,20 |
| Электроотрицательность по Оллреду — Рохову | 2,83 |
| Устойчивые степени окисления | −1, 0, +1, +3, (+4), +5, (+6), +7 |
Газообразный хлор относительно легко сжижается. Начиная с давления в 0,8 МПа (8 атмосфер), хлор будет жидким уже при комнатной температуре. При охлаждении до температуры в −34 °C хлор тоже становится жидким при нормальном атмосферном давлении. Жидкий хлор — жёлто-зелёная жидкость, обладающая очень высоким коррозионным действием (за счёт высокой концентрации молекул). Повышая давление, можно добиться существования жидкого хлора вплоть до температуры в +144 °C (критической температуры) при критическом давлении в 7,6 МПа.
При температуре ниже −101 °C жидкий хлор кристаллизуется в орторомбическую решётку с пространственной группой Cmca и параметрами a = 6,29 Å, b = 4,50 Å, c = 8,21 Å[9]. Ниже 100 К орторомбическая модификация кристаллического хлора переходит в тетрагональную, имеющую пространственную группу P42/ncm и параметры решётки a = 8,56 Å и c = 6,12 Å[9].
Растворимость[править | править код]
| Растворитель | Растворимость г/100 г |
|---|---|
| Бензол | Растворим |
| Вода[10] (0 °C) | 1,48 |
| Вода (20 °C) | 0,96 |
| Вода (25 °C) | 0,65 |
| Вода (40 °C) | 0,46 |
| Вода (60 °C) | 0,38 |
| Вода (80 °C) | 0,22 |
| Тетрахлорметан (0 °C) | 31,4 |
| Тетрахлорметан (19 °C) | 17,61 |
| Тетрахлорметан (40 °C) | 11 |
| Хлороформ | Хорошо растворим |
| TiCl4, SiCl4, SnCl4 | Растворим |
Степень диссоциации молекулы хлора Cl2 → 2Cl при 1000 К равна 2,07⋅10−4%, а при 2500 К — 0,909 %.
Порог восприятия запаха в воздухе равен 2—3 мг/м³.
По электропроводности жидкий хлор занимает место среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода, и в 1022 раз хуже серебра. Скорость звука в газообразном хлоре примерно в полтора раза меньше, чем в воздухе.
Строение электронной оболочки[править | править код]
На валентном уровне атома хлора содержится 1 неспаренный электрон: 1s2 2s2 2p6 3s2 3p5, поэтому валентность, равная 1 для атома хлора, очень стабильна. За счёт присутствия в атоме хлора незанятой орбитали d-подуровня атом хлора может проявлять и другие степени окисления. Схема образования возбуждённых состояний атома:
Также известны соединения хлора, в которых атом хлора формально проявляет валентности IV и VI, например, ClO2 и Cl2O6. Однако оксид хлора(IV) является радикалом, то есть у него есть один неспаренный электрон, а оксид хлора(VI) содержит два атома хлора, имеющих степени окисления +5 и +7.
Взаимодействие с металлами[править | править код]
Хлор непосредственно реагирует почти со всеми металлами (с некоторыми только в присутствии влаги или при нагревании):
- 2Na+Cl2→2NaCl{\displaystyle {\mathsf {2Na+Cl_{2}\rightarrow 2NaCl}}}
- 2Sb+3Cl2→2SbCl3{\displaystyle {\mathsf {2Sb+3Cl_{2}\rightarrow 2SbCl_{3}}}}
- 2Fe+3Cl2→2FeCl3{\displaystyle {\mathsf {2Fe+3Cl_{2}\rightarrow 2FeCl_{3}}}}
Взаимодействие с неметаллами[править | править код]
C неметаллами (кроме углерода, азота, фтора, кислорода и инертных газов) образует соответствующие хлориды.
- 5Cl2+2P→2PCl5,{\displaystyle {\mathsf {5Cl_{2}+2P\rightarrow 2PCl_{5}}},}
- 2S+Cl2→S2Cl2{\displaystyle {\mathsf {2S+Cl_{2}\rightarrow S_{2}Cl_{2}}}}
или
- S+Cl2→SCl2.{\displaystyle {\mathsf {S+Cl_{2}\rightarrow SCl_{2}}}.}
На свету или при нагревании активно реагирует (иногда со взрывом) с водородом по радикально-цепному механизму. Смеси хлора с водородом, содержащие от 5,8 до 88,3 % водорода, взрываются при облучении с образованием хлороводорода. Смесь хлора с водородом в небольших концентрациях горит бесцветным[11] или жёлто-зелёным пламенем. Максимальная температура водородно-хлорного пламени 2200 °C.
- h3+Cl2→2HCl.{\displaystyle {\mathsf {H_{2}+Cl_{2}\rightarrow 2HCl}}.}
С кислородом хлор образует оксиды (см. статью Оксиды хлора), в которых он проявляет степень окисления от +1 до +7: Cl2O, ClO2, Cl2O5, Cl2O7. Они имеют резкий запах, термически и фотохимически нестабильны, склонны к взрывному распаду. Напрямую хлор с кислородом не реагирует. При реакции с фтором образуется не хлорид, а фториды:
- Cl2+F2→2ClF,{\displaystyle {\mathsf {Cl_{2}+F_{2}\rightarrow 2ClF}},}
- Cl2+3F2→2ClF3,{\displaystyle {\mathsf {Cl_{2}+3F_{2}\rightarrow 2ClF_{3}}},}
- Cl2+5F2→2ClF5.{\displaystyle {\mathsf {Cl_{2}+5F_{2}\rightarrow 2ClF_{5}}}.}
Известны фторид хлора(I), фторид хлора(III) и фторид хлора(V) (ClF, ClF3 и ClF5), Могут быть синтезированы из элементов, степень окисления хлора меняется в зависимости от условий синтеза. Все они представляют собой при комнатной температуре бесцветные ядовитые тяжёлые газы с сильным раздражающим запахом. Сильные окислители, реагируют с водой и стеклом. Используются как фторирующие агенты.
Другие свойства[править | править код]
Хлор вытесняет бром и иод из их соединений с водородом и металлами:
- Cl2+2HBr→Br2+2HCl{\displaystyle {\mathsf {Cl_{2}+2HBr\rightarrow Br_{2}+2HCl}}}
- Cl2+2NaI→I2+2NaCl{\displaystyle {\mathsf {Cl_{2}+2NaI\rightarrow I_{2}+2NaCl}}}
При реакции с монооксидом углерода образуется фосген:
- Cl2+CO→COCl2{\displaystyle {\mathsf {Cl_{2}+CO\rightarrow COCl_{2}}}}
При растворении в воде или щелочах, хлор диспропорционирует, образуя хлорноватистую (а при нагревании хлорноватую) и соляную кислоты, либо их соли:
- Cl2+h3O⇄HCl+HClO{\displaystyle {\mathsf {Cl_{2}+H_{2}O\rightleftarrows HCl+HClO}}}
- Cl2+2NaOH→NaCl+NaClO+h3O{\displaystyle {\mathsf {Cl_{2}+2NaOH\rightarrow NaCl+NaClO+H_{2}O}}}
- 3Cl2+6NaOH→5NaCl+NaClO3+3h3O{\displaystyle {\mathsf {3Cl_{2}+6NaOH\rightarrow 5NaCl+NaClO_{3}+3H_{2}O}}} (при нагревании)
Хлорированием сухого гидроксида кальция получают хлорную известь:
- Cl2+Ca(OH)2→CaCl(OCl)+h3O{\displaystyle {\mathsf {Cl_{2}+Ca(OH)_{2}\rightarrow CaCl(OCl)+H_{2}O}}}
Действием хлора на аммиак можно получить трихлорид азота:
- 4Nh4+3Cl2→NCl3+3Nh5Cl{\displaystyle {\mathsf {4NH_{3}+3Cl_{2}\rightarrow NCl_{3}+3NH_{4}Cl}}}
Окислительные свойства хлора[править | править код]
Хлор — очень сильный окислитель:
- Cl2+h3S→2HCl+S{\displaystyle {\mathsf {Cl_{2}+H_{2}S\rightarrow 2HCl+S}}}
Раствор хлора в воде используется для отбеливания тканей и бумаги.
Реакции с органическими веществами[править | править код]
С насыщенными соединениями:
- Ch4-Ch4+Cl2→C2H5Cl+HCl{\displaystyle {\mathsf {CH_{3}{\text{-}}CH_{3}+Cl_{2}\rightarrow C_{2}H_{5}Cl+HCl}}}
- Ch5+Cl2→Ch4Cl+HCl
Галогены, подготовка к ЕГЭ по химии
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.

Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
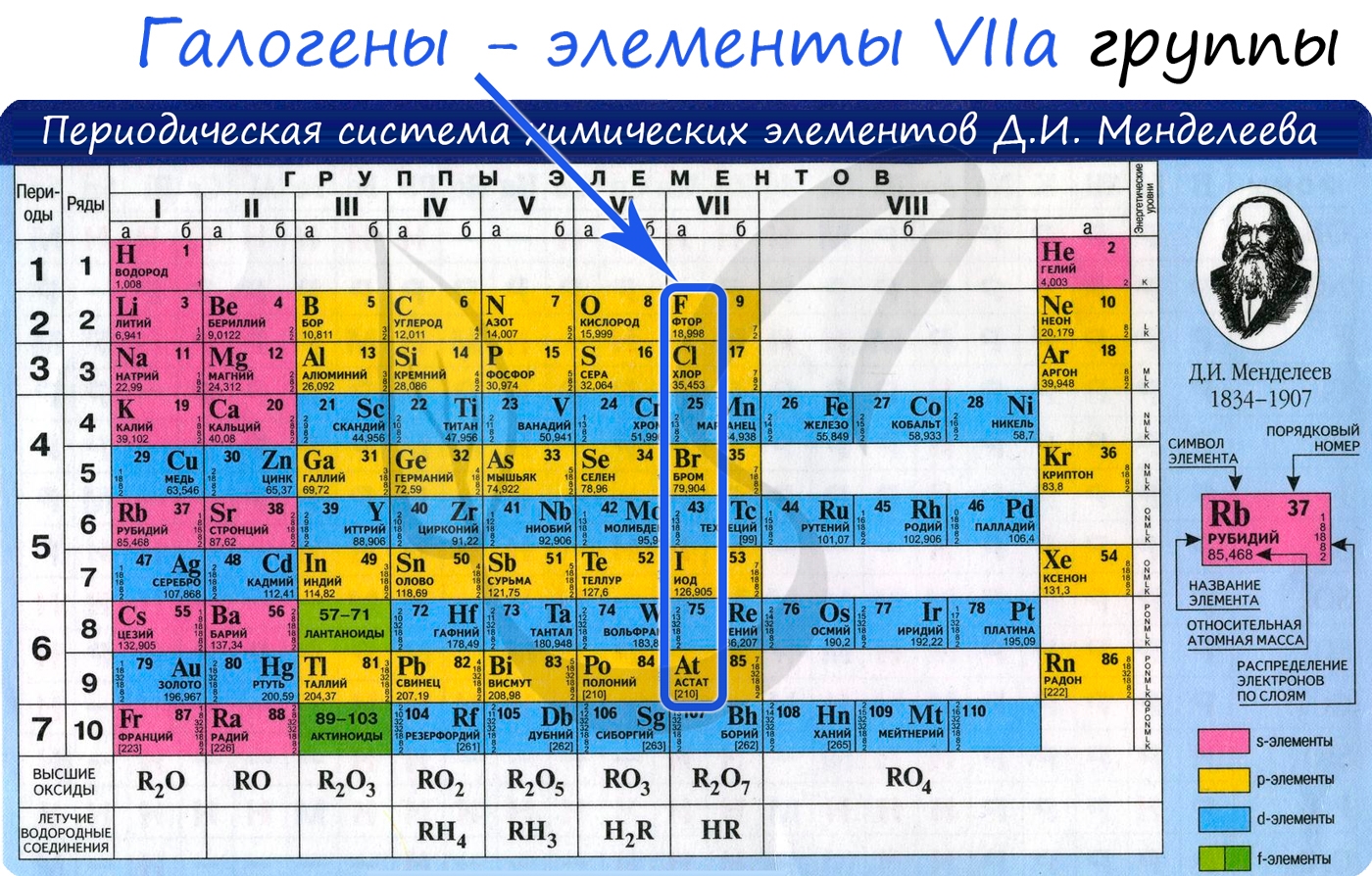
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np5:
- F — 2s22p5
- Cl — 3s23p5
- Br — 4s24p5
- I — 5s25p5
- At — 6s26p5
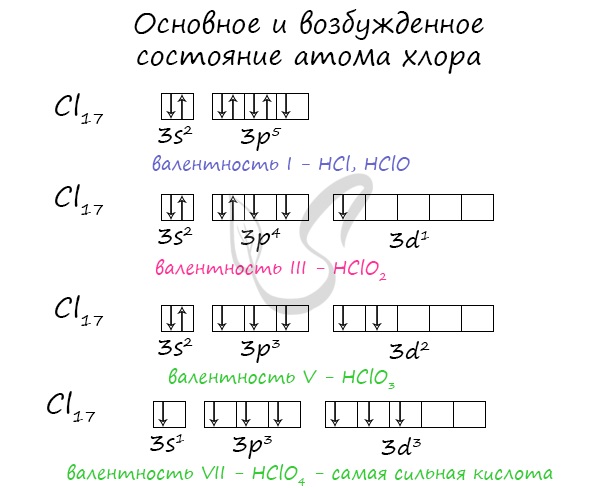
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.
Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит

Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
NaCl + H2O → (электролиз) NaOH + H2↑ + Cl2↑
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
HF → F2 + H2
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
Cl2 + KBr → Br2 + KCl
Cl2 + KI → I2 + KCl

В лабораторных условиях галогены могут быть получены следующими реакциями.
HCl + MnO2 → MnCl2 + Cl2 + H2O
HCl + KMnO4 → MnCl2 + Cl2 + KCl + H2O
Химические свойства
- Реакции с металлами
- Реакции с неметаллами
- Реакции с водой
- Реакции с щелочами
- Окислительные способности
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Al + F2 → AlF3
Cu + Cl2 → CuCl2
Na + Br2 → NaBr
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
Cl2 + Si → SiCl4
Cl2 + H2 → HCl (на свету)

F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность ;)
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F—)
Br2 + I2 → BrI3 (бром более электроотрицателен, чем йод — I—)
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
H2O + F2 → HF + O2
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Cl2 + H2O → HCl + HClO
H2O + Br2 → HBr + HBrO

Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при нагревании.
Cl2 + NaOH → NaCl + NaClO + H2O
Cl2 + NaOH → (t) NaCl + NaClO3 + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KCl + F2 → KF + Cl2
KBr + Cl2 → KCl + Br2
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
Получение
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
H2 + Cl2 → HCl
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
NaCl + H2SO4 → NaHSO4 + HCl↑
CaF2 + H2SO4 → CaSO4 + HF
PBr3 + H2O → HBr↑ + H3PO3
H2S + I2 → S + HI
Химические свойства
- Кислотные свойства
- С солями
- Восстановительные свойства
- Реакция с оксидом кремния
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Mg + HBr → MgBr2 + H2↑
Zn + HCl → ZnCl2 + H2↑

Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
Na2O + HCl → NaCl + H2O
ZnO + HI → ZnI2 + H2O
KOH + HCl → KCl + H2O (реакция нейтрализации)

Cr(OH)3 + HCl → CrCl3 + H2O
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
AgNO3 + HCl → AgCl + HNO3
Li2CO3 + HBr → LiBr + H2CO3
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
HI + MnO2 → I2 + MnI2 + H2O
HI + H2SO4 → I2 + H2S + H2O
HI + O2 → H2O + I2
HI + Br2 → HBr + I2
HCl + H2SO4 → Cl2 + SO2 + H2O

В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
SiO2 + HF → SiF4 + H2O
©Беллевич Юрий Сергеевич
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Химические свойства галогенов — урок. Химия, 8–9 класс.
Галогены относятся к химически активным веществам. В реакциях с металлами и большинством неметаллов, а также со сложными веществами галогены проявляют сильные окислительные свойства. Наиболее активен в химических реакциях фтор. С увеличением молекулярной массы активность галогенов снижается.
Взаимодействие с металлами
При взаимодействии галогенов с металлами образуются соли: фториды, хлориды, бромиды, иодиды.
Фтор реагирует со всеми металлами (даже с золотом и платиной), с большинством — при обычных условиях:
Ca+F2=CaF2,
2Au+3F2=t2AuF3.
Остальные галогены реагируют с металлами при нагревании:
2Fe+3Cl2=t2FeCl3,
Cu+Br2=tCuBr2,
2Al+3I2=t2AlI3.
Взаимодействие с водородом
В реакциях галогенов с водородом образуются газообразные галогеноводороды.
Фтор взаимодействует с водородом со взрывом с образованием фтороводорода:
h3+F2=2HF.
Смесь хлора с водородом взрывается только при поджигании или освещении. В результате реакции образуется хлороводород:
h3+Cl2=t2HCl.
Бром начинает реагировать с водородом только при нагревании, и реакция происходит без взрыва. Продукт реакции — бромоводород:
h3+Br2=t2HBr.
Реакция иода с водородом идёт медленно даже при нагревании. Иод с водородом образуют газ иодоводород:
h3+I2=t2HI.
На примере этих реакций прослеживается снижение химической активности веществ в ряду: фтор — хлор — бром — иод.
Все галогеноводороды хорошо растворяются в воде. Их растворы представляют собой кислоты:
HF — плавиковая, HCl — соляная, HBr — бромоводородная, HI — иодоводородная.
Сила кислот в этом ряду увеличивается. Самая слабая из них — плавиковая кислота, самая сильная — иодоводородная.
Вытеснение галогенов друг другом из солей
В реакциях галогенов с галогенидами проявляется следующая закономерность: более активный галоген вытесняет менее активный из его солей. Так, хлор взаимодействует с водными растворами бромидов и иодидов, выступая в этих реакциях окислителем:
2KBr−1+Cl02=Br02+2KCl−1,
2NaI−1+Cl02=I02+2NaCl−1.
Бром способен вытеснить иод из иодидов, а с хлоридами не реагирует:
2KI−1+Br02=I02+2KBr−1.
У иода способность вытеснять другие галогены отсутствует, так как его окислительные свойства в ряду галогенов самые слабые.
Реакции фтора с водными растворами солей невозможны по причине его взаимодействия с водой.
Галогены. Общая характеристика. Хлор. | Советы тут
 Сегодня разберем урок химии 16 — Галогены. Общая характеристика. Хлор. Получение свойства и применение хлора и его соединений.
Сегодня разберем урок химии 16 — Галогены. Общая характеристика. Хлор. Получение свойства и применение хлора и его соединений.
Но сначала, проверим ответы на урок химии 15 – тестовые задания к урокам химии 10-14:
1-3, 2-4, 3-3, 4-4, 5-1, 6-4, 7-1, 8-1, 9-4, 10-1, 11-1, 12-1, 13-1, 14-1, 15-1, 16-3, 17-3, 18-4, 19-3, 20-1, 21-3, 22-4, 23-3, 24-2, 25-4, 26-3, 27-2, 28-2, 29-2, 30-3.
Галогены составляют главную подгруппу седьмой группы периодической таблицы. К ним относятся элементы фтор F, хлор Cl, бром Br, йод I, астат Аt. На внешнем уровне у них имеется по семь электронов: nS2nP5. Фтор является самым электроотрицательным элементом, проявляет степень окисления F-1. Другие галогены проявляют степени окисления от (-1) до (+7). В свободном состоянии молекулы галогенов двухатомны (F2), (Cl2), (Br2), (I2) и являются типичными неметаллическими простыми веществами. Фтор и хлор являются газами, бром – жидкость, йод и астат – твердые вещества. Окислительная способность галогенов при переходе от фтора к астату уменьшается, галоген с меньшим порядковым номером всегда вытесняет галоген с большим порядковым номером из бескислородных солей: F2 + 2KBr → 2KF + Br2.
Хлор Сl2. При обычных условиях ядовитый газ зеленовато-желтого цвета. В лабораторных условиях получают по реакциям:
- MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
- 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
- KClO3 + 6HCl → KCl + 3Cl2↑ + 3H2O
В промышленности хлор получают электролизом раствора хлорида натрия: 2NaCl + 2H2O → 2NaOH + Cl2↑ + H2↑
Химические свойства. Хлор реагирует со многими веществами:
- с металлами: 2Fe + 3Cl2 → 2FeCl3
- с неметаллами: 2Р + 5Сl2 → 2PCl5
- с водородом: Н2 + Сl2 → 2HCl
- с водой: Cl2 + H2O → HCl + HClO Смесь соляной и хлорноватистой кислот (HClO) кислот называют хлорной водой.
- При взаимодействии хлора с щелочами на холоду образуются смеси хлоридов и гипохлоридов:
Сl2 + 2KOH → KCl + KClO + H2O
- В горячем растворе щелочи протекает реакция:
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
- Хлор реагирует со многими органическими веществами, например с предельными углеводородами: СН4 + Cl2 → CH3Cl + HCl
- C непредельными углеводородами: С2Н2 + 2Cl2 → C2H2Cl4
Хлор относится к продуктам основного органического синтеза и находит широкое применение в различных отраслях промышленности: для получения брома и иода, хлоридов и кислородсодержащих производных, для отбеливания бумаги, обеззараживания питьевой воды, получения хлороводорода. Хлороводород НСl– бесцветный газ с сильным запахом. Хорошо растворяется в воде, водные растворы называют хлороводородной кислотой, а дымяшие концентрированные растворы – соляной кислотой. Получают по реакциям: Н2 + Сl2 → 2HCl, NaCl + H2SO4 → NaHSO4 + HCl (при обычной температуре). При нагревании
реакция протекает по второй стадии: 2NaCl + H2SO4 → Na2SO4 + 2HCl. Хлороводородная является сильной минеральной кислотой и обладает всеми свойствами кислот. Наиболее важными кислородсодержащими соединениями хлора являются: HClO – хлорноватистая кислота, ее соли – гипохлориты.
HClO2 – хлористая кислота, соли – хлориты.
HClO3 – хлорноватая кислота, соли – хлораты.
HClO4 – хлорная кислота, соли – перхлораты.
Из солей кислородсодержащих кислот хлора наибольшее значение имеют бертолетова соль (хлорат калия, КClO3) и хлорная известь – СаОСl2.
Бертолетову соль используют для получения кислорода в лабораторных условиях, а хлорную известь как отбеливающее и дезинфицирующее средство.
Это был урок химии 16 — Галогены. Общая характеристика. Хлор. Получение свойства и применение хлора и его соединений.
Friend me:
к нашему сайту.
Галогены ⚗️ электронная конфигурация элементов, общая характеристика, химические и физические свойства, способы получения и применения, взаимодействие с другими веществами
Не все знают, что под пугающим названием «галогены» зачастую скрываются распространенные в быту вещества. Не в чистом виде, но все-таки. Отдельными представителями «семейства» ежедневно пользуется каждый человек.
Приведём примеры:
-
На упаковке любой зубной пасты имеется словосочетание со словом «фтор». Полезен для зубной эмали.
-
Хлор знаком любой домохозяйке и сотруднику клининговой компании. А уж его запах знают все, кто посещал бассейн или лечебные учреждения России. Не пустой звук для советских школьников. Даже не из курса химии, а из уроков химзащиты в рамках начальной военной подготовки (НВП).
-
Про «бром» ходили легенды среди военнослужащих СССР. Насколько сведения достоверны – неизвестно.
-
Темно-коричневая бутылочка с «йодом» – постоянный спутник любителя поиграть с котенком и непоседливого ребенка. Распространенный антисептик.
Что такое галогены
Определяют, как элементы 17-ой группы таблицы Менделеева. Сторонники «старой школы» выразились бы: «главной подгруппы VII группы».
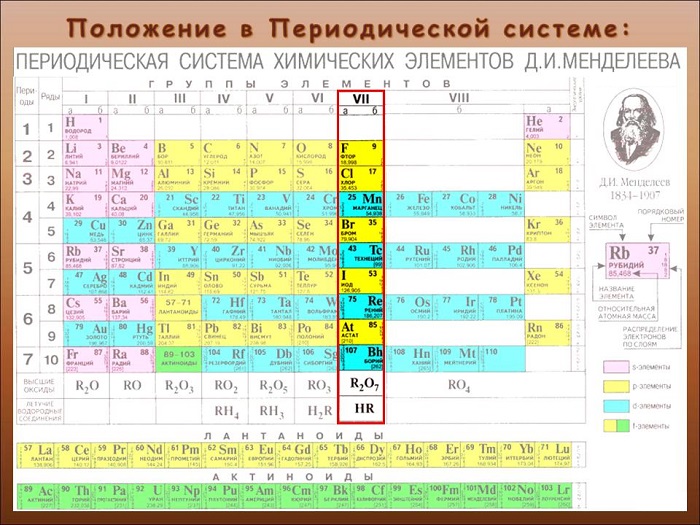
Название представляет собой компиляцию греческих слов. Означает приблизительно «солерождающий». Такое определение было дано в XIX веке британским ученым Гэмфри Дэви.
Перечень и общая характеристика галогенов

С первыми четырьмя элементами из списка некоторое знакомство имеется. Надо заметить, что вещества хоть и достаточно распространенные, но в чистом виде в природе не встречаются. Только в составе соединений.
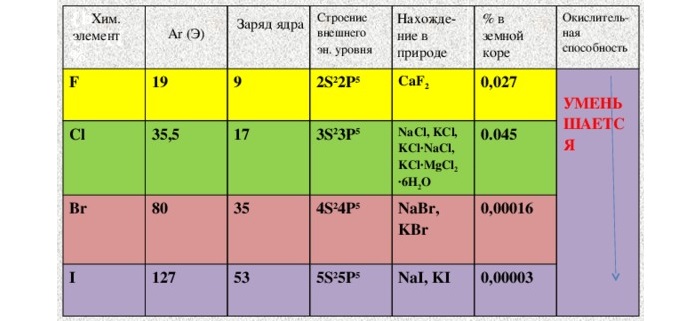
Астат – элемент не просто редкий, а самый редкий из всех встречающихся на планете. Его «запасы» оцениваются в 1 г. Свойства доподлинно не известны. Так как из-за радиоактивности и мизерной «продолжительности жизни» в достаточных количествах выделить не получилось.
Теннессин существует скорее теоретически. На Земле, по крайней мере, не нашли. Рекордное зафиксированное (и признанное) в лаборатории количество – 6 ядер. Включая изотоп.
Зато точно известен общий принцип построения наружного энергетического уровня: ns2np5. Под «n» понимается период расположения элемента.
Легко заметить, что до «идеальных» инертов не хватает всего-то электрончика. А так хочется. Не удивительно, что так агрессивны.
Физические свойства
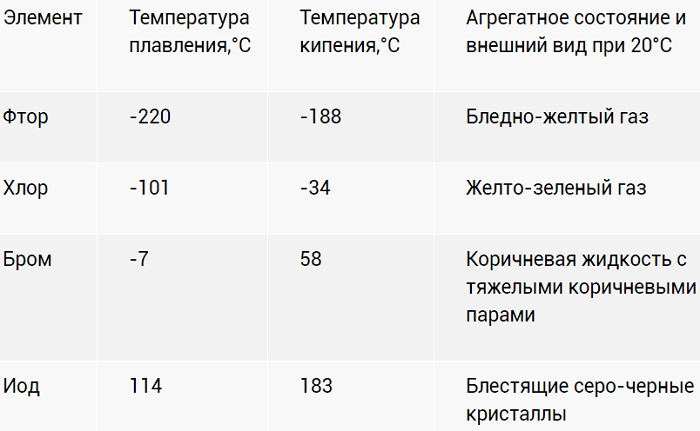
Галогены – ярко выраженные неметаллы. Летучи, с характерно едким «ароматом». Причем для йода (I2) жидкое агрегатное состояние вообще не характерно. При разогреве просто испаряется фиолетовым дымком.
Хлор – настоящее боевое отравляющее вещество. И применялось в таком качестве. Попадая в незащищенные глаза и органы, образует кислоты. С соответствующими последствиями. Для летального исхода достаточно концентрации в воздухе 2 мг/л.
Насыщенность цветов с «утяжелением» ядер возрастает. Активность, напротив, падает.
В воде растворимость ограничена. Лучше ведёт себя с органическими растворителями. Растворы оригинально окрашены: от слабо желтого до фиолетового.
Химические свойства галогенов
Галогены (Hal) — мощные окислители, а фтор агрессивен настолько, что вступает в реакцию с собратьями. Происходит это при подогреве. Степень окисления «пострадавших» оказывается +1.
Общее уравнение:
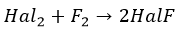
Можно сказать, что F реагирует со всеми простыми субстанциями, кроме отдельных благородных газов. А так (с облучением):
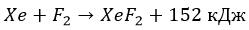
Остальные элементы ряда не взаимодействуют с:
С неметаллами
Водород окисляет фтор при любых условиях, со взрывом. Cl с подсветкой УФ или подогревом. Но тоже громко. Остальные только с нагреванием. Но уравнение едино:
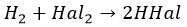
С фосфором взаимодействуют совершенно по-разному:
∗ F до получения пентафторида. Единственный, без нагревания:
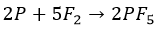
∗ хлор и бром, в зависимости от концентрации:
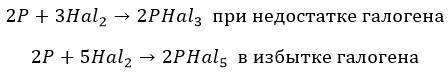
∗ йод – недостаточно мощный окислитель:
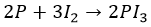
∗ с серой также не все очевидно. Но только не с фтором. Окисление максимально, но с нагревом:
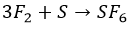
∗ бром и хлор реагируют нетипично и «неохотно»:
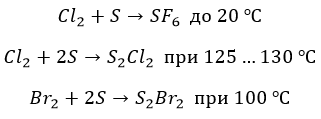
С металлами
Перед фтором ничто не устоит. Даже благородный класс, хоть и с нагревом:
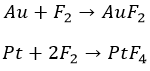
Остальные металлы прочим галогенам по силам. Не без подогрева:
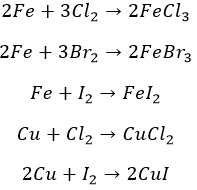
Реакции замещения
Агрессивные вытесняют «тяжелых» соседей по группе:
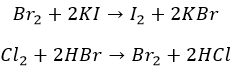
И с неметаллами не церемонятся:
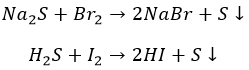
Хлор, как более активный, ведет себя несколько по-другому:
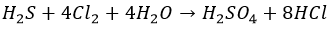
С водой
Фтор в своем репертуаре. Вода будет пылать синим пламенем и норовить плюнуть плавиковой кислотой:
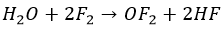
Хлор с бромом гораздо спокойнее. Да и процессы нестабильны, обратимы:
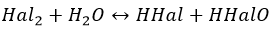
Йод с водой в видимые взаимодействия не вступает.
С растворами щелочей
И в этом случае фтор проявляется как резкий окислитель:
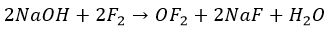
Остальные ведут себя, как с водой. Но процесс при разных температурах проходит по разным сценариям:
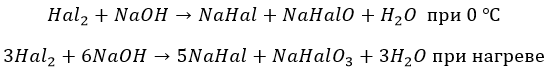
Йод реагирует только по второму варианту.
Получение
Выделить вещество настолько активное, что норовит прореагировать со всем окружающим, не так просто.
Фтор
Обычно получают из сложных солей. При интенсивном нагреве (термолиз) провоцируется распад на более простые и нужный газ.

Или электролизом KF*3HF. Аналогичный метод применяется в промышленности.
Хлор
Из соляной кислоты. Неприятно и опасно даже в условиях лаборатории:
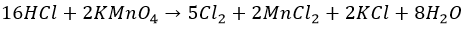
Индустриально добывают из распространенной поваренной соли при помощи электролиза:
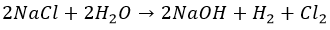
Бром и йод
«На коленке» – из солей. Окислителями, в кислом же окружении:
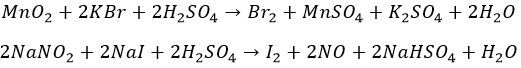
Химзаводам за сырьем ходить не надо. Морская вода, скважные жидкости. Остатки сожженных океанских/морских водорослей – настоящая йодная руда.
Применение галогенов
Как уже упоминалось, фтор применяется в лечебных и профилактических средствах. Соединения необходимы для изготовления алюминия.

Основная часть производимого хлора используется для синтеза соляной кислоты. Необходим в химической индустрии. Для сельскохозяйственных, бытовых ядохимикатов, чистящих средств, отбеливателей. Для очистителей воды.
Бром и йод применяются для медикаментов и в химической отрасли.
Заключение
О свойствах галогенов можно писать бесконечно. В данной статье не затрагивались темы взаимодействий с органическими веществами, например.
А ведь без них невозможен, скажем, фотосинтез. Одна из основ жизни. Без соляной кислоты невозможно пищеварение высших животных. Об этом мы расскажем в следующих публикациях.



