Производство и добыча водорода как источника водородной энергии
Со школьных уроков химии и физики известно, что энергия водорода сосредоточенная в этом газе довольно значительна. Искры достаточно, чтобы воспламенить смесь нормального воздуха и водорода полученного в результате опыта на школьных уроках.
В отличие от многих других процессов горения, продукт реакции абсолютно безвреден с экологической точки зрения, поэтому люди изучают промышленное производство и энергию водорода.
Так как человечеству необходимы все больше энергии чистая водородная энергия пришлась бы кстати.
Топливные элементы могут генерировать столь востребованную электроэнергию из этого газа. Неудивительно, что многие люди с видением глобальной водородной экономики видят в этом решение наших текущих климатических проблем.
Энергия водорода может в то же время помочь нам избавиться от загрязнения воздуха, кислотных дождей и других экологических проблем, вызванных другими источниками.
Жюль Верн увидел потенциал энергии водорода еще в 1874 году в романе «Таинственный остров», и вопрос в том, почему процветающая водородная промышленность еще не развилась.
Ответ прост: этот газ не встречается в природе в чистом виде и нужно преобразование энергии. Энергетика и комплекс технических процессов необходим прежде чем его можно выделить и использовать как водородную энергию.
Отделение до чистого водорода делает его дорогим, а некоторые производственные процессы даже приводят к высоким выбросам парниковых газов.Но даже если водородная промышленность еще только на чертежной доске, вторичная энергия водорода все еще интересна как альтернативный источник для некоторых областей применения.
Что представляет первый элемент периодической системы
Водород – самый маленький и легкий атом. Как чрезвычайно легкий газ, он был использован для наполнения газовых баллонов дирижаблей жесткой формы как Цеппелины, в течение первой половины девятнадцатого века. Катастрофа в Гинденбурге в США в 1937 году, где предположительно произошел электростатический заряд который вызвал возгорание, положил трагический конец перспективам использования водорода в дирижаблях.
Основное применение водорода сегодня находится в химической промышленности. В качестве источника энергия водорода в настоящее время широко используется, в основном, в авиационном и космическом секторе.
Водород как источник энергии используется для привода реактивных двигателей самолетов.
В космических полетах жидкий водород используется в качестве ракетного топлива. Например, запуск космического челнока потребляет около 1,4 млн литров жидкого водорода весом более 100 тонн создавая температуру горения до 3200° C.
Производство
Водородная энергетика использует несколько способов производства водорода.
Газ сначала должен быть получен в чистом виде, прежде чем энергия из него может быть получена. Это требует легкодоступного недорогого сырья, содержащего этот химический элемент. Кроме воды (H2O), которая состоит из водорода (H) и кислорода (O) могут быть применены смеси углерода. Это в первую очередь природный газ или метан (CH4). Мазут и уголь также состоят из водорода (H) и углерода (C), но имеют гораздо более высокую долю углерода, чем природный газ.
Из углеводородов
Современные промышленные методы получения водорода почти исключительно используют ископаемые топливо, как природный газ, сырую нефть или уголь, как сырье. Такие методы, как паровой риформинг или частичное окисление паром для получения водорода из ископаемых углеводородов. Этот процесс химически отделяет углерод который после этого превращается в окись углерода (CO). Эти методы добычи водорода не являются идеальным вариантом с целью активной защиты климата. 

В основном, упомянутый способ производства водорода из ископаемых источников работает при высоких температурах обработки. Это требует большого количества внешних ресурсов.
Поэтому для получения водорода необходимы другие методы, с тем чтобы он был экологически чистым и безопасным. Идеальным способом является электролиз.
Методом электролиза
Немецкий химик Иоганн Вильгельм Риттер впервые использовал электролиз для получения водорода еще в 1800 году. С помощью электрической энергии, электролиз разлагает воду на водород и кислород. 

Особенностью электролиза может быть то, что если электроэнергия добыта из возобновляемых источников, то производство водорода во всем цикле может выделять только углекислый газ.
С помощью этого метода два электрода погружают в проводящий водный электролит. Это может быть смесь воды и серная кислота или гидроксид калия (KOH). Аноды и катоды проводят постоянный ток в электролитах и на них образуются газы водород и кислород. Хотя электролиз уже достиг высокого уровня технического развития, как экологически совместимый вариант производства кислорода, другие альтернативные методы также разрабатываются.
Термохимический метод
При температуре выше 1700° C вода непосредственно разлагается на водород и кислород. 
 Однако эти температуры требуют дорогостоящих термостойких средств. Необходимую температуру можно уменьшить ниже чем 1000° С через различные сопряженные химические реакции.
Однако эти температуры требуют дорогостоящих термостойких средств. Необходимую температуру можно уменьшить ниже чем 1000° С через различные сопряженные химические реакции.Биологическое получение
Другие методы включают фотобиологическое производство водорода. Суть этого метода в том, что некоторые водоросли во время роста при нехватке серы производят водород. 

Хранение и транспортировка
После получения водорода он должен храниться и транспортироваться потребителю. В принципе, мы знакомы с хранением и транспортировкой горючих газов.
Водород – очень легкий газ с очень минимальной плотностью, но имеет относительно высокое значение энергоемкости. При сравнении с природным газом то он требует гораздо больших объемов хранения, хотя накопленный водород намного легче.
Произведенный водород можно сохранить под высоким давлением и сжать для того чтобы уменьшить необходимые объемы хранения. При нормальном давлении этот газ конденсируется, но до тех пор, пока он не достигнет чрезвычайно низких температур минус 253° C.
Для достижения таких низких температур требуется определенное количество энергии. От 20 до 40% энергии, хранящейся в водороде, используется для его сжижения.
В принципе, те же технологии, которые используются в секторе природного газа могут быть использованы для сжижения, транспортировки и хранения. Этот первый элемент периодической системы можно транспортировать либо в трубопроводах, либо на специальных танкерах и грузовых судах. В то время как трубопроводы, как правило, транспортируют газообразную форму, танкеры предпочтительны для жидкого водорода. В отличие от водорода, природный газ уже становится жидким при минус 162 ° C. Опыт работы в газовой отрасли может быть использован для хранения и транспортировки водородной энергии.
Будущее применение
Топливные элементы считаются ключом к будущему использованию энергии водорода, поскольку они могут преобразовывать его непосредственно в электрическую энергию. Теоретически это приводит к более высокой эффективности, чем при сжигании в обычных тепловых электростанциях.
Принцип работы топливных элементов известен уже очень давно.
Есть некоторые споры о том, кто на самом деле изобрел топливный элемент:
- Немецко-швейцарский химик Кристиан Фридрих провел первые тесты в технологии топливных элементов в 1838 году.
- Английский физик сэр Уильям Роберт Гроув построил первый топливный элемент в 1839 году.
- Впоследствии такие известные ученые, как Анри Беккерель и Томас Эдисон, стали участвовать в их дальнейшем развитии. Однако это была довольно слабо продвинутая стадия развития.
- Наконец, в середине двадцатого века была достигнута задача, позволившая применение и основное использование топливных элементов.
Топливные элементы, в основном, предполагают реверсирование электролиза. Топливный элемент всегда содержит два электрода. В зависимости от типа топливного элемента, чистый водород (H2) или топливо содержащее углеводороды подают через анод и чистый кислород (О2 ) или воздух в качестве окислительного материала через катод. Электролит отделяет анод и катод. Электроны текут по большой цепи и создают электрическую энергию.
С 1990-х годов разработка топливных элементов идет полным ходом. Автомобильные производители и энергокомпании приняли технологию и ищут способ получить прибыль от положительного применения водорода как источника энергии.
Урок 26. Получение водорода и его применение – HIMI4KA
В уроке 26 «Получение водорода и его применение» из курса «Химия для чайников» узнаем о получении водорода в лабораториях и в промышленности, а также выясним в каких отраслях промышленности его применяют.


Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:


Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:


Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
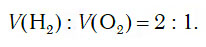
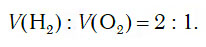
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
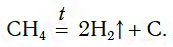
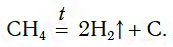
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
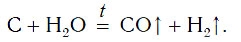
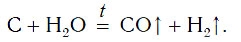
Существуют и другие промышленные способы получения водорода.
Применение водорода
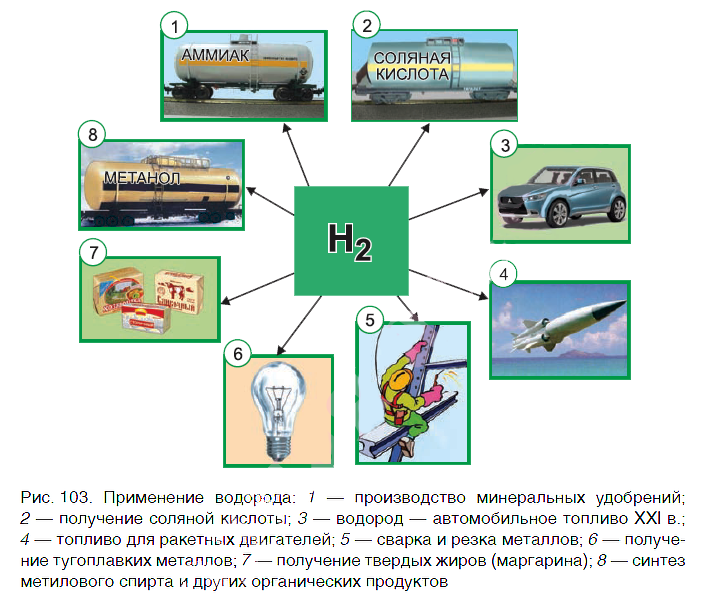
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 оС. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.

В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
- В лаборатории водород получают действием кислот на металлы.
- В промышленности для получения водорода используют доступное и дешевое сырье — природный газ, воду.
- Водород — это перспективный источник энергии XXI в.
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
как работают водородные автомобили и когда они появятся на дорогах / Habr
В Испании, где я сейчас живу, довольно много электромобилей — встречаю их практически каждый день, как на дорогах, так и на станциях для зарядки. И каждый год электрокаров становится все больше (не только в Испании, конечно). Но есть и альтернатива — автомобили на водородном топливе, которые тоже не загрязняют природу, поскольку их выхлоп — вода. Тема сегодняшней справочной — водородные машины, принцип их работы и перспективы.
Когда появились первые автомобили на водороде?
Изобрел двигатель внутреннего сгорания, работающий на водороде, Франсуа Исаак де Ривас (François Isaac de Rivaz) в 1806 году. Водород он получал с помощью электролиза воды. Поршневой двигатель, который создал изобретатель, называют машиной де Риваса (De Rivaz engine).
Зажигание было искровым, двигатель имел шатунно-поршневую систему работы. Ну а цилиндр приводился в движение детонацией смеси водорода и кислорода электрической искрой — ее приходилось генерировать вручную в момент опускания поршня. Через два года этот же изобретатель построил уже самодвижущееся устройство с водородным двигателем.
Но более-менее широко применять водород для работы автомобильных двигателей стали много лет спустя. В 1941 году в блокадном Ленинграде автомобильные двигатели ГАЗ-АА были модифицированы инженер-лейтенантом Б. И. Шелищем. Движки управляли лебедками аэростатов заграждения (их заправляли водородом, и запасов газа в Ленинграде было много), но это были автомобильные двигатели. Кроме того, были модифицированы и несколько сотен движков в автомобилях.
Начиная с 1980-х сразу в нескольких странах, включая США, Японию, Германию, СССР и Канаду стартовало экспериментальное производство по созданию автомобилей, работающих на водороде, бензин-водородных смесях и смесях водорода с природным газом.
В 1982 году нефтеперерабатывающий завод «Квант» и завод РАФ разработали первый в мире экспериментальный водородный микроавтобус «Квант-РАФ» с комбинированной энергоустановкой на основе водородо-воздушного топливного элемента мощностью 2 кВт и никель-цинковой аккумуляторной батареи емкостью 5 кВт*ч.
На протяжении многих лет такие автомобили разрабатывали в разных странах по большей части в качестве эксперимента. После того, как концепция «зеленого» автомобиля стала популярной, автомобилями на водороде заинтересовались крупные корпорации вроде Toyota. Начиная с 2000-х, автомобильные компании стали разрабатывать концепты коммерческих авто.
А где брать водород?
Водород можно получать разными методами:
- паровая конверсия метана и природного газа;
- газификация угля;
- электролиз воды;
- пиролиз;
- биотехнологии.
Наиболее экономичным способом производства водорода сейчас считается паровая конверсия. Так называют получение водорода из легких углеводородов (метан, пропан-бутановая фракция) с использованием парового риформинга. Риформингом называют процесс каталитической конверсии углеводородов в присутствии водяного пара. Водяной пар смешивается с метаном при высокой температуре (700–1000 Сº) и большом давлении с использованием катализатора.
При паровой конверсии водород получать дешевле, чем используя любые другие методы, включая электролиз.
Наиболее безвредный способ производства водорода — электролиз — получение водорода из воды с использованием электрического тока. Чистота выхода водорода близка к 100%. Если не считать загрязнение для получения электричества, такие установки почти безвредны для окружающей среды, поскольку в процессе работы выделяются только водород и кислород.
Еще один безопасный для окружающей среды способ получения водорода — реактор с биомассой.
Источник
Производить водород можно и на крупной фабрике, и на относительно небольшом предприятии. Чем масштабнее производство — тем ниже себестоимость газа. Но зато в первом случае увеличиваются расходы на доставку водорода к местам заправки машин.
Как работает топливная система и какие есть варианты?
Лучше всего рассмотреть принцип работы такой системы на примере серийных водородных авто Toyota Mirai. Основа — топливный элемент, электрохимическая система, преобразующая частицы водорода и кислорода в воду. Внутри такого элемента — протонпроводящая полимерная мембрана, которая разделяет анод и катод. Обычно это угольные пластины с нанесенным катализатором.
На катализаторе анода молекулярный водород теряет электроны, катионы проводятся через мембрану к катоду, а электроны отдаются во внешнюю цепь. На катализаторе катода молекулы кислорода соединяются с электроном и протоном, образуя воду. Пар или жидкость — это единственный продукт реакции.
Преимущество топливных ячеек на основе протонообменных мембран — высокая удельная мощность и относительно низкая рабочая температура. Они быстро греются и почти сразу после старта начинают производить энергию.
В Mirai используются топливные элементы с высокой удельной мощностью на единицу объема (3,2 кВт/л), максимальная их мощность 124 кВт. Произведенный топливным элементом постоянный ток преобразуется в переменный с одновременным повышением напряжения до 650 В. Электричество поступает в литий-ионный аккумулятор. Для движения машина расходует запасенную в нем энергию.
Водород в топливный элемент Mirai поступает из баллонов высокого давления (около 700 атм). Блок управления в автомобиле контролирует режим работы топливного элемента и зарядку/разрядку аккумулятора.
По данным Toyota на 100 км пути Mirai требуется до 750 граммов водорода. Владельцы Mirai говорят о примерно килограмме водорода на 100 км пути.
Такие автомобили опасны? Почему?
Поскольку водород — горючий газ, то транспортировать и хранить его нужно осторожно. Нужны высокочувствительные газоанализаторы, которые смогут дать сигнал в случае утечки. Правда, водород очень летучий газ (ведь это самый легкий химический элемент) и при попадании в атмосферу водород быстро поднимается вверх.
Сгорает он очень быстро. Дирижабль «Гинденбург» горел всего 32 секунды. Благодаря скоротечности пожара погибли далеко не все пассажиры, выжили 62 человека из 97, находившихся в гондоле дирижабля.
Тем не менее, если автомобилей на водороде станет много, то потребуются новые меры безопасности движения на дорогах. Машины с ДВС тоже опасны — в случае аварии и пробоя бака бензин или дизельное топливо вытекают на дорогу и могут воспламениться. Если будет пробит бак с водородом, газ очень быстро улетучится. Но если близко будет источник открытого огня или искр, водород может загореться.
В Mirai и других моделях водородных авто используются очень прочные баки для водорода. Toyota сделала свои баки пуленепробиваемыми, их стенки из сверхпрочного волокна выдерживают выстрелы из крупнокалиберного оружия. Для тестов компания наняла снайперов и пробить бак смогла только пуля калибром .50 после двойного попадания в одно и тоже место.
Если соблюдать меры безопасности, водородные автомобили не опаснее машин с ДВС.
Какой срок службы у топливных ячеек?
Пока что такая информация есть лишь для Mirai. Toyota заявляет, что одна ячейка гарантированно будет работать на протяжении 250 000 км. Затем, если работа ячейки ухудшается, ее можно заменить в сервисном центре.
Какие компании уже выпускают или собираются выпускать автомобили на водороде?
Водородные машины разрабатывают Honda, Toyota, Mercedes-Benz и Hyundai — у этих компаний уже есть готовые транспортные средства. Другие показывают пока лишь концепты (впрочем, рабочие) или просто красиво отрендеренные картинки. К числу первых можно отнести Audi и Ford, к числу вторых — BMW (справедливости ради нужно сказать, что в 2007 году BMW выпустила партию из 100 экспериментальных «водородных» моделей, которые так и остались экспериментом) и Lexus.
В серию запущены пока лишь Toyota Mirai и Honda Clarity. Их можно приобрести в США и Европе.
Сколько это стоит?
В настоящий момент водородные автомобили немного дороже обычных в плане эксплуатации. Так, при поездке в Европе протяженностью 480 км затраты на горючее для владельца обычной машины составят примерно $45, а вот владелец Mirai заплатит около $57. И это при том, что правительство некоторых стран субсидирует производство водорода для машин. Стоимость 1 кг водорода составляет в среднем $11.45.
Чем водородные авто лучше электромобилей?
Собственно, вопрос не совсем корректный. Дело в том, что и автомобиль на водороде, с топливной ячейкой, и «чистый» электрокар — это электромобили. Просто в одном случае машину заправляют водородом, во втором — электричеством.
Если сравнивать стоимость большинства электромобилей и Toyota Mirai, то они сравнимы, это несколько десятков тысяч долларов США. Стоимость Hyundai ix35 Fuel Cell составляет около $53 тыс., Toyota Mirai — $57 тыс., Honda Clarity — $59 тыс. Стоимость электрокаров Tesla начинается с $45 тыс. (базовая комплектация с прайсом в $35 тыс. пока доступна лишь для предзаказа). Электромобили от BMW стоят около $50 тыс.
Водородные автомобили быстро заправляются — на это уходит всего 3–5 минут, в отличие от электромобилей, где нужно от получаса до нескольких часов для подзарядки.
Основное достоинство водородного транспорта в том, что топливные ячейки служат много лет и практически не нуждаются в обслуживании. Если взять «чистый» электромобиль с его огромной батареей, то ее срок службы всего 1–1,5 тыс. циклов, то есть 3-5 лет. Причем водородный автомобиль без проблем будет работать на морозе (заводиться в том числе), а вот аккумулятор электромобиля потеряет заряд.
Какие перспективы у водородных машин и когда их можно будет увидеть на дорогах?
Водородные автомобили уже колесят по дорогам Европы и США (возможно, единичные экземпляры есть и в других регионах). Но их немного — несколько тысяч, что нельзя назвать массовым внедрением.
Проблема, которая сейчас мешает распространению водородных транспортных средств — отсутствие инфраструктуры (всего несколько лет назад аналогичная проблема была актуальной и для электромобилей). Нужны специализированные фабрики по производству водорода, транспортные системы для водорода и заправки.
Водородные АЗС в 2019 году(источник)
Кроме того, водород получается довольно дорогим, так что если электромобили покупают, в частности, для экономии на топливе, то в случае водородной машины — это не вариант. При массовом появлении фабрик по производству водорода для машин, а также сервисной инфраструктуры можно ожидать выхода гораздо большего числа транспортных средств на водороде на дороги общего пользования.
Но нет гарантии, что это вообще случится ли это или нет — пока неясно. Автопроизводители вроде Toyota активно продвигают свои машины и преимущества водорода в транспортной сфере. Но конкуренция слишком велика, как среди обычных машин с ДВС, так и среди электромобилей.
Получение водорода. Установки получения (производства) водорода.
Общее описание
- Генератор водорода
- Установка оборудована 2 пакетами элементов для производства водорода 30 нм³/ч
- Контейнер модернизирован и подготовлен для увеличения производительности в будущем до 45 нм³/ч. Так же если в будущем потребуется дополнительно увеличить мощность, то контейнер рассчитан на увеличение до 60 нм³/ч.
- Модуль хранения объемом 50 м³ по воде для хранения 450 нм³ водорода при 10 бар.
Предложенная нами система включает стандартные встроенные системы безопасности, стандартное заводское приемочное испытание и комплект технической документации.
Услуги на месте включают: пуск системы, ввод в эксплуатацию и обучение на месте. Строительные работы и подготовка площадки, выполняемые на месте, осуществляются заказчиком в соответствии с требованиями.
Энергоисточники (вода, электричество, азот, воздух КИП,…) должны быть доступны на месте.
Характеристики электролизера:
- Полностью автоматическая работа
- Полный контроль получения водорода
- Производство под давлением (10 бар изб.) без установки компрессора
- Высокая эффективность и надежность
- Очень низкие затраты на техническое обслуживание (ограниченное число подвижных деталей, без насоса для электролита)
- Водород не содержит углерода – без вредных выбросов
- Производственный процесс сертифицирован по ISO 9001, 14001
- Услуги по пуску и пост-продажному обслуживанию
Введение
Установка производства водорода в контейнерном исполнении для установки снаружи представляет собой комплексную установку производства водорода с производительностью по водороду 60 нм³/ч при чистоте 99,998% и давлении 10 бар (изб.)
Разработан модифицированный ISO контейнер повышенной вместимости для размещения генератора водорода и всего его питающего оборудования.
Ввод оборудования для наружного размещения в эксплуатацию на площадке заказчика тем самым значительно облегчен по сравнению с установкой в существующее помещение генератора на базе скида.
Надежность
Используя принцип внедрения технологического уровня эксплуатационной безопасности оборудования каждая установка помимо прочего обладает следующими характеристиками:
- минимальное присутствие газа в системе
- определение минимального давления для предотвращения попадания воздуха
- система непрерывного мониторинга/обнаружения водорода в атмосфере
- система защитной вентиляции зона II (только с кожухом или корпусом (каркасом) для наружного размещения)
- надежная логическая схема для всех параметров
- Система бесперебойного питания, обеспечивающая безопасное отключение в случае аварийного отключения питания
- Система постоянного мониторинга, чистота производства О2 газа
- Системы множественного / параллельного управления
- Многократное резервирование параметров, которые являются критичными в рамках безопасности системы
Автоматизация
Надежность – это одно из наиболее значимых требований для наших заказчиков. Установка разработана для полностью непрерывной эксплуатации с минимальной потребностью в присутствии оператора, обеспечивая константный поток водорода.
- Система контроля давления: Человеко-машинный интерфейс на панели управления позволяет операторы выбрать требуемое давление газа (между 8 и 10 бар изб.). Установка автоматически регулирует свою производительность с тем, чтобы обеспечить установленное давление.
- Автоматизация охлаждения: охлаждающая вода поступает в теплообменники через клапан, регулируемый ПЛК. При повышении температуры клапан открывается, тем самым подавая большее количество охлаждающей воды в контур. В результате этого – стабильная производственная температура.
- Автоматическая продувка азотом: следуя принципам системы, продувка азотом требуется перед запуском установки при внутреннем давлении ниже 15 кПа. Процесс продувки регулируется ПЛК системы путем активации клапана в последовательном процессе.
- Удаленный I/O: используя современное соединение PROFIBUS, мы значительно уменьшили количество соединительных кабелей и соответственно время, необходимое на установку. Внедрение прокола в комбинации с безопасным ПЛК и безопасным I/O позволяет системе полностью соответствовать самым строгим актуальным нормам и стандартам безопасности. ПЛК автоматически диагностирует любые ошибки передачи данных, не только делая систему безопаснее, но также сокращая время и силы на устранения неполадок.
Объем поставки
Сенсорный экран с человеко-машинным интерфейсом (HMI)
Экран HMI расположен на панели управления и позволяет оператору контролировать и эксплуатировать электролизер либо с экрана, либо с удаленного соединения, через защищенное соединение VPN. Система мониторинга включает в себя запись данных на компактную флэш карту. Она также позволяет нашим техническим специалистам подключаться к электролизеру, для диагностики и исправления случаев неисправностей и тревожной сигнализации при необходимости.
Исполнение контейнера
ISO 40’ футовый контейнер спроектирован и модифицирован для размещения водородной установки 60 нм³/ч и включает:
- изолированные стенки и перекрытия
- пол из металлических листов
- запираемые двери во внешних стенках
- Освещение во всех отсеках
- Все устройства полностью оснащены и установлены на место вкл. трубную обвязку и кабели, что значительно сокращает время и затраты на установку / межсоединения на месте.
- Два вытяжных вентилятора, которые вытягивают воздух через технологическое помещение из помещения общего назначения. Первый обеспечивает минимальный поток и работает постоянно. Поток проверяется между помещением общего назначения и технологическим помещением и подается аварийный сигнал, если минимум не достигнут.
Второй вентилятор активируется, когда температура окружающего воздуха в технологическом помещении находится вне пределов спецификации или когда обнаружен водород.
Технологический скид
Ключевым компонентов электролизного скида является пакет биполярных ячеек для электролиза воды под давлением. Пакет ячеек состоит из кольцевых электролизных ячеек, в каждой из которых содержатся два электрода и одна щелочная неорганическая ионообменная мембрана.
Генерация H2 и O2 происходит при подаче тока на пакет ячеек. Газы затем направляются на газовый сепаратор, который представляет собой двойной сосуд под давление из нержавеющей стали, после которого они промываются в специально спроектированном напорном сосуде, расположенном над газосепаратором.
Технологическая часть поставляется как полностью собранный скид, в который включено оборудование, например:
- Пакеты ячеек
- Газосепарторы, установка промывки газообразного водорода и коалесцирующие фильтры
- Теплообменники для электролита и системы газового охлаждения
- Лоток детектора утечек с реле уровня
- Детектор водорода , панель анализатора для водорода в кислороде
- Приборы кип и распределительные коробки: датчики, трансмиттеры, реле и т.д.
- Клапаны и вентиляционные коллекторы (H2 и O2)
Блок управления
Шкаф панели управления включает в себя ПЛК и все соответствующее оборудования для обеспечения автоматической и надежной эксплуатации установки. Панель управления с помощью кабелей будет подсоединена как к технологической части, так и к силовой стойке. Характеристики:
- Утвержденный электрический кожух с 2 запираемыми дверцами
- Вентиляторы охлаждения + система фильтрации воздуха
- ПЛК (Siemens S-7 программное обеспечение)
- Снаружи: терминал с дисплеем для визуализации и HMI
- Аварийный останов на дверце кожуха
- Блок бесперебойного питания для безопасного отключения
- Источник питания 24 В пост. тока
- Автоматические выключатели и трансформаторы
- Печатные платы и звуковая сигнализация
Блок питания

Блок питания конвертирует входящей 3х фазный переменный ток в стабилизированный постоянный ток, требуемый для процесса электролиза.
Каждый блок питания может питать до 2 пакетов элементов и состоит из:
- Кожух с запираемой дверцей
- Охлаждающие вентиляторы + система фильтрации воздуха
- Защитная блокировка дверного переключателя
- ПЛК контролируется тиристорами
- Трансформатор
- Выпрямительный диод
- Автоматические выключатели, контакторы
- Измерительный пакет элементов на дверце амперметр и вольтметр
- Устройство проверки фазы
Система очистки водорода

Система очистки водорода спроектирована для дальнейшей очистки водорода до минимального уровня в размере 99.998%. Данная чистота достигается в 2 этапа:
Этап 1. Деоксидизация: для уменьшения содержания O2 в потоке газообразного H2 с помощью каталитической реакции. Выход O2 в H2 составляет менее 10 ppm или опционально менее 2 ppm.
Этап 2. Осушка: для удаления влажности в 2 колоннах осушки. Одна колонна находится в работе, в то время как вторая находится в режиме резерва / регенерации. Водород на выходе будет иметь атмосферную точку росы менее -60 °C или опционально менее -75 °C.
Система очистка водорода сконструирована на скиде и располагается в технологическом помещении. Система очистки водорода управляется с помощью центрального ПЛК в панели управления и имеет следующие особенности:
- Сосуд деокисидзации с катализатором для удаления О2 в H2 (с обогревом и изоляцией)
- Теплообменник
- Коалесцирующий фильтр
- Система дренажного сосуда для удаления воды
- Оборудование КИП
- Две колонны осушки с молекулярным ситом (с обогревом и изоляцией) (с временной регенерацией)
- Соединения до контура охлаждения газа
- Соединение до вентиляционных коллекторов технологической части (H2 и O2)
Холодильник (охлаждение газа)

Холодильник подает охлаждающую воду низкой температуры в замкнутый контур газообразного водорода и кислорода в сторону теплообменников при температуре 15 °C, вне зависимости от температуры окружающей среды. Охлажденная вода охлаждает газообразный водород и кислород, превращая водяной пар, появляющийся в процессе электролиза, в конденсат. Затем он фильтруется и удаляется из потока газа. Холодильник устанавливается внутри кожуха для применения внутри помещения и включает насос и расширительный бак.
Спецификация на чиллер
Система охлаждения электролита

Данная система охлаждения, включающая в себя насосный скид и сухой охладитель, выводит тепло в окружающий воздух.
Охлаждающая вода, как правило, водный раствор этиленгликоль, циркулирует в закрытом контуре, через высокопроизводительный теплообменник по типу «электролит-вода», установленный в технологической части установки производства водорода.
Благодаря системе охлаждения закрытого цикла гарантируется полная выходная способность установки по водороду в диапазоне температуры окружающей среды от -40 до +40°C. Сухой охладитель и насосный скид регулируются с помощью центрального ПЛК в панели управления.
Спецификация на сухой охладитель
Система подготовки питательной воды

Система подготовки питательной воды превращает водопроводную воду в чистую деминерализованную воду, необходимую для процесса электролиза. Осуществляется постоянный мониторинг за качеством воды, прежде чем она сможет поступить в процесс. Размеры ВхШхГ – 1,5х1,0х0,5 м
Система включает в себя такие фильтрационные очистные этапы как:
- Мембрана обратного осмоса
- Ионообменная система смешанного типа со смолой (2 резервуара, наполненные смолой)
- Система смягчения воды с цифровым дозирующим насосом (анти-накипь)
- Измеритель электропроводности
- Активированный уголь и предварительные фильтры для улавливания частиц
- Указатели давления и реле
Спецификация на питательную воду
Техническая спецификация
Вышеуказанные данные представлены только для информации и не могут быть использованы для гарантийных целей.
Общий вид
Дополнительные опции (по запросу)
Улучшение чистоты -75 °C 2ppm O2
Данная опция снижает атмосферную точку росы произведенного H2 с -60 °C до -75 °C, а содержание О2 в произведенном H2 с 10ppm до 2 ppm.
Уменьшенное содержание N2 – распылительный разбрызгиватель
Распылительный разбрызгиватель – это устройство, устанавливаемое на входе деминерализованной воды установки производства водорода для уменьшения содержания N2 менее 2 ppm произведенного H2.
Замер чистоты в режиме реального времени
Производится непрерывный мониторинг произведенного H2 в реальном времени как по содержанию воды («точка росы»), так и по содержанию кислорода. Данная опция может быть выбрана только в сочетании с системой очистки водорода.
Спускной клапан (только в комбинации с системой замера чистоты в режиме реального времени)
Данное устройство автоматически выпускает H2 в атмосферу, в случае если его качество не соответствует спецификации. Данная опция может быть выбрана только в комбинации с системой замера чистоты H2 в режиме реального времени.
Использование кислорода
Стандартно О2 сбрасывается в атмосферу. Производитель может обеспечить опциональную систему для очистки О2 и его подготовки для дальнейшего использования / очистки со стороны заказчика.
Система кондиционирования воздуха на панели управления
Это модульная установка кондиционирования воздуха, устанавливаемая на электропанелях. Данное устройство рекомендовано для систем, часто эксплуатируемых в температурах окруж. среды более +40 °C
Массовый расходомер
Массовый расходомер – это непосредственный замер объема H2, идущего в линию заказчика.
Содержание кислорода в детекторе атмосферы
Трансмиттер кислорода в атмосфере может быть реализован в технологическом помещении для непрерывного мониторинга уровня O2 в атмосфере технологического помещения. Система сигнализации срабатывает, если уровень кислорода падает ниже или поднимается выше безопасных предельных значений.
Автоматический перезапуск
Данная функция позволяет установке непрерывно определять актуальное давление в линии заказчика. Если установка находится в резервном режиме, то с помощью данной функции установка может быть автоматически повторно запущена, как только давление линии заказчика окажется ниже заданного порогового значения.
Опции по каркасу для наружной установки
Низкотемпературная опция:
Будут предприняты специальные действия, чтобы допустить работу при температуре окружающей среды до -40 °C. Например, адоптированная система охлаждения с закрытым контуром и усиленная система обогрева.
Аварийные огни:
В случае отключения сетевого питания аварийные огни в помещении с приборами управления будут светить до 30 минут.
Внешние огни:
Огни снаружи контейнера при входе в помещение с приборами управления / для инженерного оборудования и технологического помещения.
Вентиляционные трубы:
Две трубы из высококачественной нержавеющей стали с колпачками от дождя для безопасной вентиляции H2 и О2. Длина данных вентиляционных труб соответствует спецификации, для каркаса для наружного размещения, который установлен в зоне без прилегающих конструкций. Вентиляционные трубы должны быть вертикально соединены на месте к специально определенным фланцам на боковой стороне контейнера. Кабели обогрева для защиты труб от нулевых температур (точка замерзания) включены в данный объем.
Границы объема поставки
Границей установка электролиза является каркас для наружного размещения. На внешних стенках каркаса для наружного размещения имеются металлические пластины, которые включают следующие соединения:
- Пользователь водородного газа
- Вход питательной воды
- Вход воздуха КИП
- Вентиляционное отверстие кислорода (вентиляционная линия не включена)
- Вентиляционное отверстие водорода (вентиляционная линия не включена)
- Соединение дренажа конденсата
- Вход инертного газа (азот)
- Электрические межсоединения: включены внутри контейнера
- Механические межсоединения: включены внутри контейнера
- Энергопитание: автоматический прерыватель на стороне электролиза.
- Охлаждающая вода (2 контура):
Сухой охладитель (охлаждение электролита)
- Сухой охладитель поставляется в отдельной коробке. Он спроектирован для установки на крыше каркаса для наружного размещения, а объем поставки включает технические условия на крыше контейнера для их установки.
- Трубка обвязки и кабели для соединения контейнера к внутренней части контейнера включены, но монтаж сухого охладителя на крыше и осуществление соединений на месте осуществляются заказчиком.
Холодильник (охлаждение газа):
- Холодильник поставляется с полностью выполненными соединениями в каркасе для наружного размещения
Установка водоподготовки:
- Установка водоподготовки поставляется с полностью выполненными соединениями в каркасе для наружного размещения.
Водородная энергетика: начало большого пути
Водородная энергетика — одна из самых перспективных отраслей. узнаем самые продвинутые и известные водородные технологии.
C ростом числа электротранспорта городам потребуется больше электричества, которое зачастую получают экологически небезопасными способами. К счастью, сегодня мир научился получать энергию при помощи ветра, солнца и даже водорода. Новый материал мы решили посвятить последнему из источников и рассказать об особенностях водородной энергетики.
Водородная энергетика
- Водородные топливные элементы
- Проблемы добычи
- Водородное будущее
На первый взгляд, водород — идеальное топливо. Во-первых, он является самым распространенным элементом во Вселенной, во-вторых, при его сгорании высвобождается большое количество энергии и образуется вода без выделения каких-либо вредных газов. Преимущества водородной энергетики человечество осознало уже давно, однако применять ее в больших промышленных масштабах пока не спешит.
Водородные топливные элементы
Первый водородный топливный элемент был сконструирован английским ученым Уильямом Гроувом в 30-х годах XIX века. Гроув пытался осадить медь из водного раствора сульфата меди на железную поверхность и заметил, что под действием электрического тока вода распадается на водород и кислород. После этого открытия Гроув и работавший параллельно с ним Кристиан Шенбейн продемонстрировали возможность производства энергии в водородно-кислородном топливном элементе с использованием кислотного электролита.
Позже, в 1959 году, Фрэнсис Т. Бэкон из Кембриджа добавил в водородный топливный элемент ионообменную мембрану для облегчения транспорта гидроксид-ионов. Изобретением Бэкона сразу заинтересовалось правительство США и NASA, обновленный топливный элемент стал использоваться на космических аппаратах «Аполлон» в качестве главного источника энергии во время их полетов.
Водородный топливный элемент из сервисного модуля «Аполлонов», вырабатывающий электричество, тепло и воду для астронавтов.
Сейчас топливный элемент на водороде напоминает традиционный гальванический элемент с одной лишь разницей: вещество для реакции не хранится в элементе, а постоянно поставляется извне. Просачиваясь через пористый анод, водород теряет электроны, которые уходят в электрическую цепь, а сквозь мембрану проходят катионы водорода. Далее на катоде кислород ловит протон и внешний электрон, в результате чего образуется вода.
Принцип работы водородного топливного элемента. 
С одной топливной ячейки снимается напряжение порядка 0,7 В, поэтому ячейки объединяют в массивные топливные элементы с приемлемым выходным напряжением и током. Теоретическое напряжение с водородного элемента может достигать 1,23 В, но часть энергии уходит в тепло.
С точки зрения «зеленой» энергетики у водородных топливных элементов крайне высокий КПД — 60%. Для сравнения: КПД лучших двигателей внутреннего сгорания составляет 35-40%. Для солнечных электростанций коэффициент составляет всего 15-20%, но сильно зависит от погодных условий. КПД лучших крыльчатых ветряных электростанций доходит до 40%, что сравнимо с парогенераторами, но ветряки также требуют подходящих погодных условий и дорогого обслуживания.
Как мы видим, по этому параметру водородная энергетика является наиболее привлекательным источником энергии, но все же существует ряд проблем, мешающих ее массовому применению. Самая главная из них — процесс добычи водорода.
Проблемы добычи
Водородная энергетика экологична, но не автономна. Для работы топливному элементу нужен водород, который не встречается на Земле в чистом виде. Водород нужно получать, но все существующие сейчас способы либо очень затратны, либо малоэффективны.
Самым эффективным с точки зрения объёма полученного водорода на единицу затраченной энергии считается метод паровой конверсии природного газа. Метан соединяют с водяным паром при давлении 2 МПа (около 19 атмосфер, т. е. давление на глубине около 190 м) и температуре около 800 градусов, в результате чего получается конвертированный газ с содержанием водорода 55-75%. Для паровой конверсии необходимы огромные установки, которые могут быть применимы лишь на производстве.
Трубчатая печь для паровой конверсии метана — не самый эргономичный способ добычи водорода.
Более удобный и простой метод — электролиз воды. При прохождении электрического тока через обрабатываемую воду происходит серия электрохимических реакций, в результате которых образуется водород. Существенный недостаток этого способа — большие энергозатраты, необходимые для проведения реакции. То есть получается несколько странная ситуация: для получения водородной энергии нужна… энергия. Во избежание возникновения при электролизе ненужных затрат и сохранения ценных ресурсов некоторые компании стремятся разработать системы полного цикла «электричество — водород— электричество», в которых получение энергии становится возможным без внешней подпитки. Примером такой системы является разработка Toshiba h3One.
Мобильная электростанция Toshiba h3One
Мы разработали мобильную мини-электростанцию h3One, преобразующую воду в водород, а водород в энергию. Для поддержания электролиза в ней используются солнечные батареи, а излишки энергии накапливаются в аккумуляторах и обеспечивают работу системы в отсутствие солнечного света. Полученный водород либо напрямую подается на топливные ячейки, либо отправляется на хранение во встроенный бак. За час электролизер h3One генерирует до 2 м3 водорода, а на выходе обеспечивает мощность до 55 кВт. Для производства 1 м3 водорода станции требуется до 2,5 м3 воды.
Пока станция h3One не способна обеспечить электричеством крупное предприятие или целый город, но для функционирования небольших районов или организаций ее энергии будет вполне достаточно. Благодаря своей мобильности она может использоваться также как и временное решение в условиях стихийных бедствий или экстренного отключения электричества. К тому же, в отличие от дизельного генератора, которому для нормального функционирования необходимо топливо, водородной электростанции достаточно лишь воды.
Сейчас Toshiba h3One используется лишь в нескольких городах в Японии — к примеру, она снабжает электричеством и горячей водой железнодорожную станцию в городе Кавасаки.
Монтаж системы h3One в городе Кавасаки
Водородное будущее
Сейчас водородные топливные элементы обеспечивают энергией и портативные пауэр-банки, и городские автобусы с автомобилями, и железнодорожный транспорт (более подробно об использовании водорода в автоиндустрии мы расскажем в нашем следующем посте). Водородные топливные элементы неожиданно оказались отличным решением для квадрокоптеров — при аналогичной с аккумулятором массе запас водорода обеспечивает до пяти раз большее время полета. При этом мороз никак не влияет на эффективность. Экспериментальные дроны на топливных элементах производства российской компании AT Energy применялись для съемок на Олимпиаде в Сочи.
Стало известно, что на грядущих Олимпийских играх в Токио водород будет использоваться в автомобилях, при производстве электричества и тепла, а также станет главным источником энергии для олимпийской деревни. Для этого по заказу Toshiba Energy Systems & Solutions Corp. в японском городе Намиэ строится одна из крупнейших в мире станций по производству водорода. Станция будет потреблять до 10 МВт энергии, полученной из «зеленых» источников, генерируя электролизом до 900 тонн водорода в год.
Водородная энергетика — это наш «запас на будущее», когда от ископаемого топлива придется окончательно отказаться, а возобновляемые источники энергии не смогут покрывать нужды человечества. Согласно прогнозу Markets&Markets объем мирового производства водорода, который сейчас составляет $115 млрд, к 2022 году вырастет до $154 млрд.
Но в ближайшем будущем массовое внедрение технологии вряд ли произойдет, необходимо еще решить ряд проблем, связанных с производством и эксплуатацией специальных энергоустановок, снизить их стоимость. Когда технологические барьеры будут преодолены, водородная энергетика выйдет на новый уровень и, возможно, будет так же распространена, как сегодня традиционная или гидроэнергетика. опубликовано econet.ru
Подписывайтесь на наш канал Яндекс Дзен!
P.S. И помните, всего лишь изменяя свое потребление — мы вместе изменяем мир! © econet
Металлический водород — Википедия

Металли́ческий водоро́д — совокупность фазовых состояний водорода, находящегося при крайне высоком давлении и претерпевшего фазовый переход. Металлический водород представляет собой вырожденное состояние вещества и, по некоторым предположениям, может обладать некоторыми специфическими свойствами — высокотемпературной сверхпроводимостью и высокой удельной теплотой фазового перехода.
Предсказан теоретически в 1935 году.
В 1930-х годах британский ученый Джон Бернал предположил, что атомарный водород, состоящий из одного протона и одного электрона и представляющий собой полный аналог щелочных металлов, может оказаться стабильным при высоких давлениях[1]. В 1935 году Юджин Вигнер и X. Б. Хантингтон провели соответствующие расчёты. Гипотеза Бернала нашла подтверждение — согласно полученным расчётам, молекулярный водород переходит в атомарную металлическую фазу при давлении около 250 тыс. атмосфер (25 ГПа) со значительным увеличением плотности[2]. В дальнейшем оценка давления, требуемого для фазового перехода, была повышена, но условия перехода всё же считаются потенциально достижимыми. Предсказание свойств металлического водорода ведётся теоретически. Попытки получения, начатые в 1970-х годах, привели к возможным эпизодам водорода в 1996, 2008 и 2011 году, пока, наконец, в 2017 году профессор Айзек Сильвера и его коллега Ранга Диас не добились получения стабильного образца при давлении 5 млн атмосфер[3][4][1], однако камера, где хранился образец, под давлением разрушилась, и образец был потерян.
Связь с другими областями физики[править | править код]
- Астрофизика
Считается, что большие количества металлического водорода присутствуют в ядрах планет-гигантов — Юпитера, Сатурна — и крупных экзопланет. Благодаря гравитационному сжатию под газовым слоем должно находиться ядро из металлического водорода.
Переход в металлическую фазу[править | править код]
При увеличении внешнего давления до десятков ГПа коллектив атомов водорода начинает проявлять металлические свойства. Ядра водорода (протоны) сближаются друг с другом существенно ближе боровского радиуса, на расстояние, сравнимое с длиной волны де Бройля электронов. Таким образом, сила связи электрона с ядром становится нелокализованной, электроны слабо связываются с протонами и формируют свободный электронный газ так же, как в металлах.
Жидкий металлический водород[править | править код]
Жидкая фаза металлического водорода отличается от твердой фазы отсутствием дальнего порядка. Имеется дискуссия о допустимом диапазоне существования жидкого металлического водорода. В отличие от гелия-4, жидкого при температуре ниже 4,2 K и нормальном давлении благодаря нулевой энергии нулевых колебаний, массив плотно упакованных протонов обладает значительной энергией нулевых колебаний. Соответственно, переход от кристаллической фазы к неупорядоченной ожидается при ещё более высоких давлениях. Исследование, проведенное Н. Ашкрофтом, допускает область жидкого металлического водорода при давлении около 400 ГПа и низких температурах[5][6]. В других работах Е. Бабаев предполагает, что металлический водород может представлять собой металлическую сверхтекучую жидкость.[7][8]
Сверхпроводимость[править | править код]
В 1968 году Нейл Ашкрофт предположил, что металлический водород может обладать сверхпроводимостью при сравнительно высоких температурах.[9]
Более точные расчёты[10] (Н. А. Кудряшов, А. А. Кутуков, Е. А. Мазур, Письма ЖЭТФ, т. 104, вып. 7, 2016, с. 488) показали, что критическая температура металлического водорода в фазе I41/AMD, той самой, которая изучалась[3] Рангой Диас и Иcааком Сильверой при давлении в 5 миллионов атмосфер, дает величину температуры перехода в сверхпроводящее состояние 215 кельвинов, то есть −58 градусов по Цельсию.
Экспериментальные попытки получения[править | править код]
Металлизация водорода ударным сжатием в 1996 году[править | править код]
В 1996 году Ливерморская национальная лаборатория сообщила, что в ходе исследований были созданы условия для металлизации водорода и получены первые свидетельства его возможного существования[11]. Кратковременно (около 1 мс) было достигнуто давление более 100 ГПа (106{\displaystyle 10^{6}} атм.), температура порядка тысяч кельвинов при плотности вещества около 600 кг/м3[12]. Поскольку предыдущие опыты по сжатию твердого водорода в ячейке с алмазными наковальнями до 250 ГПа не дали результата, целью эксперимента не было получение металлического водорода, а только изучение проводимости образца под давлением. Однако, по достижении 140 ГПа электрическое сопротивление практически исчезло. Ширина запрещенной зоны водорода под давлением составила 0.3 эВ, что оказалось сравнимо с тепловой энергией kT{\displaystyle kT}, соответствующей 3000 К и что свидетельствует о переходе «полупроводник — металл».
Исследования после 1996 года[править | править код]
Продолжались попытки перевести водород в металлическое состояние статическим сдавливанием при низких температурах. А. Руофф и Ч. Нараяна (Корнеллский университет, 1998)[13], П. Лоувьер и Р. Летуле (2002) последовательно приближались к давлениям, наблюдаемым в центре Земли (324—345 ГПа), но все же не наблюдали фазового перехода.
Эксперименты 2008 года[править | править код]
Теоретически предсказанный максимум кривой плавления на фазовой диаграмме, указывающий на жидкую металлическую фазу водорода, был экспериментально обнаружен Ш. Деемьяд и И. Сильвера[14]. Группа М. Ереметца заявила о переходе силана в металлическое состояние и проявление сверхпроводимости[15], но результаты не были повторены.[16][17]
Эксперименты 2011 года[править | править код]
В 2011 году было сообщено о наблюдении жидкой металлической фазы водорода и дейтерия при статическом давлении 260—300 ГПа. [18], что вновь вызвало вопросы в научном сообществе[19].
Эксперименты 2015 года[править | править код]
26 июня 2015 году в журнале Science была опубликована статья, в которой описан успешный эксперимент группы исследователей из Сандийских национальных лабораторий (США) совместно с группой из Ростокского университета (Германия) по сжатию жидкого дейтерия (тяжёлого водорода) с помощью Z-Машины до состояния, которое проявляет свойства металла[20].
Эксперименты 2016 года[править | править код]
В июле 2016 сообщалось, что физикам из Гарвардского университета удалось получить в лаборатории металлический водород. Они нагрели жидкий водород с помощью коротких вспышек лазера до температуры около 1900 градусов Цельсия и подвергли давлению в 1,1—1,7 мегабар[21].
Ожидается, что это вещество будет метастабильным, то есть при снятии давления останется металлом. Эксперимент физиков помогает объяснить, какие процессы могут происходить в недрах газовых гигантов. Учёные предполагают, что в будущем металлический водород может быть использован в качестве ракетного топлива или как сверхпроводник, способный существовать при комнатной температуре[22].
Научное сообщество скептически отнеслось к данной новости[23], ожидая повторного эксперимента[24].
- Топливные элементы
Метастабильные соединения металлического водорода перспективны как компактное, эффективное и чистое топливо. При переходе металлического водорода в обычную молекулярную фазу высвобождается в 20 раз больше энергии, чем при сжигании смеси кислорода и водорода — 216 МДж/кг[25].
- ↑ 1 2 Сергей Стишов. Практическое использование металлического водорода следует отнести к научной фантастике // Коммерсантъ Наука, № 1, 24 февраля 2017
- ↑ Wigner, E.; Huntington, H.B. On the possibility of a metallic modification of hydrogen (англ.) // Journal of Chemical Physics. — 1935. — Vol. 3, no. 12. — P. 764. — DOI:10.1063/1.1749590.
- ↑ 1 2 Ranga P. Dias, Isaac F. Silvera. Observation of the Wigner-Huntington transition to metallic hydrogen (англ.) // Science. — 2017-01-26. — P. eaal1579. — ISSN 1095-9203 0036-8075, 1095-9203. — DOI:10.1126/science.aal1579.
- ↑ In, Geology. Scientists Have Finally Created Metallic Hydrogen, Geology IN. Дата обращения 28 января 2017.
- ↑ Ashcroft N. W. The hydrogen liquids (англ.) // Journal of Physics: Condensed Matter. — 2000. — Vol. 12, no. 8A. — P. A129. — DOI:10.1088/0953-8984/12/8A/314.
- ↑ Bonev S.A., et al. A quantum fluid of metallic hydrogen suggested by first-principles calculations (англ.) // Nature. — 2004. — Vol. 431, no. 7009. — P. 669. — DOI:10.1038/nature02968. — arXiv:cond-mat/0410425.
- ↑ Babaev E., Ashcroft N. W. Violation of the London law and Onsager–Feynman quantization in multicomponent superconductors (англ.) // Nature Physics. — 2007. — Vol. 3, no. 8. — P. 530. — DOI:10.1038/nphys646. — arXiv:0706.2411.
- ↑ Babaev E., Sudbø A., Ashcroft N. W. A superconductor to superfluid phase transition in liquid metallic hydrogen (англ.) // Nature. — 2004. — Vol. 431, no. 7009. — P. 666. — DOI:10.1038/nature02910. — arXiv:cond-mat/0410408.
- ↑ Ashcroft, N.W. Metallic Hydrogen: A High-Temperature Superconductor? (англ.) // Physical Review Letters. — 1968. — Vol. 21, no. 26. — P. 1748. — DOI:10.1103/PhysRevLett.21.1748.
- ↑ N. A. Kudryashov, A. A. Kutukov, E. A. Mazur. Critical temperature of metallic hydrogen at a pressure of 500 GPa (англ.) // JETP Letters. — 2016-12-14. — Vol. 104, iss. 7. — P. 460–465. — DOI:10.1134/S0021364016190061.
- ↑ Weir S. T., Mitchell A. C., Nellis W. J. Metallization of fluid molecular hydrogen at 140 GPa (1.4 Mbar) (англ.) // Physical Review Letters. — 2004. — Vol. 76, no. 11. — P. 1860. — DOI:10.1103/PhysRevLett.76.1860.
- ↑ Nellis, W. J. Metastable Metallic Hydrogen Glass (неопр.). Lawrence Livermore Preprint UCRL-JC-142360 (2001). — «minimum electrical conductivity of a metal at 140 GPa, 0.6 g/cm3, and 3000 K».
- ↑ Ruoff A. L., et al. Solid hydrogen at 342 GPa: No evidence for an alkali metal (англ.) // Nature. — 1998. — Vol. 393, no. 6680. — P. 46. — DOI:10.1038/29949.
- ↑ Deemyad S., Silvera I. F. The melting line of hydrogen at high pressures (англ.) // Physical Review Letters. — 2008. — Vol. 100, no. 15. — DOI:10.1103/PhysRevLett.100.155701. — arXiv:0803.2321.
- ↑ Eremets M. I., et al. Superconductivity in hydrogen dominant materials: Silane (англ.) // Science. — 2008. — Vol. 319, no. 5869. — P. 1506–9. — DOI:10.1126/science.1153282.
- ↑ Degtyareva O. Formation of transition metal hydrides at high pressures (англ.) // Solid State Communications. — 2009. — Vol. 149, no. 39—40. — DOI:10.1016/j.ssc.2009.07.022. — arXiv:0907.2128v1.
- ↑ Hanfland M., Proctor J., Guillaume C. L., et al. High-Pressure Synthesis, Amorphization, and Decomposition of Silane (англ.) // Physical Review Letters. — 2011. — Vol. 106, no. 9. — DOI:10.1103/PhysRevLett.106.095503.
- ↑ Eremets M. I., Troyan I. A. Conductive dense hydrogen (англ.) // Nature Materials. — 2011. — No. 10. — P. 927–931. — DOI:10.1038/nmat3175.
- ↑ Nellis W. J., Ruoff A., Silvera I. F. Has Metallic Hydrogen Been Made in a Diamond Anvil Cell? (англ.) // arxiv.org. — 2012. — arXiv:http://arxiv.org/abs/1201.0407.
- ↑ M. D. Knudson, M. P. Desjarlais, A. Becker, R. W. Lemke, K. R. Cochrane, M. E. Savage, D. E. Bliss, T. R. Mattsson, R. Redmer. Direct observation of an abrupt insulator-to-metal transition in dense liquid deuterium (англ.) // Science. — 26 June 2015. — Vol. 348, no. 6242. — P. 1455—1460. — DOI:10.1126/science.aaa7471.
- ↑ Физики получили частицу Юпитера на Земле
- ↑ В США ученые провели эпохальный опыт. Они получили металлический водород // Независимая газета, 27.01.2017.
- ↑ Physicists doubt bold report of metallic hydrogen // Nature — News & Comment
- ↑ There’s Reason To Be Skeptical About Metallic Hydrogen // Форбс (англ.)
- ↑ Silvera, Isaac F. Metallic Hydrogen: A Game Changing Rocket Propellant (неопр.). NIAC SPRING SYMPOSIUM (27 марта 2012). — «Recombination of hydrogen atoms releases 216 MJ/kg Hydrogen/Oxygen combustion in the Shuttle releases 10 MJ/kg … density about 12-13 fold». Дата обращения 13 мая 2012.
Биоводород — Википедия
Материал из Википедии — свободной энциклопедии
 Производство водорода с помощью водорослей
Производство водорода с помощью водорослейБиоводород — водород, полученный из биомассы.
В настоящее время во всём мире ежегодно производится около 50 млн тонн водорода. Из них примерно 48 % производится из природного газа, 30 % из нефти, и 18 % из угля. При производстве водорода из углеводородов получается большое количество СО2, который является одной из причин глобального потепления. К тому же не все страны обладают собственными углеводородами. Решением этих проблем может стать производство водорода из биомассы.
Водород из биомассы получается термохимическим или биохимическим способом.
При термохимическом методе биомассу нагревают без доступа кислорода до температуры 500—800 °C (для отходов древесины), что намного ниже температуры процесса газификации угля. В результате процесса выделяется H2, CO и CH4.
Себестоимость процесса $5—7 за килограмм водорода. В будущем возможно снижение до $1,0—3,0.
В биохимическом процессе водород вырабатывают различные бактерии, например, Rodobacter speriodes, Enterobacter cloacae.
Возможно применение различных энзимов для ускорения производства водорода из полисахаридов (крахмал, целлюлоза), содержащихся в биомассе. Процесс проходит при температуре 30 °C и нормальном давлении. Себестоимость водорода около $2 за кг.
Учёные Калифорнийского университета в Беркли в 1999 году обнаружили, что если водорослям не хватает кислорода и серы, то процессы фотосинтеза у них резко ослабевают и начинается бурная выработка водорода.
Водород может производить группа зелёных водорослей, например, Chlamydomonas reinhardtii. Водоросли могут производить водород из морской воды, или канализационных стоков.
Водород может производиться риформингом биогаза или лэндфилл-газа.



