Теплота — Википедия
Внутренняя энергия термодинамической системы может изменяться двумя способами: посредством совершения работы над системой и посредством теплообмена с окружающей средой. Энергия, которую получает или теряет тело в процессе теплообмена с окружающей средой, называется коли́чеством теплоты́ или просто теплотой[1]. Теплота — это одна из основных термодинамических величин в классической феноменологической термодинамике. Количество теплоты входит в стандартные математические формулировки первого и второго начал термодинамики.
Для изменения внутренней энергии системы посредством теплообмена также необходимо совершить работу. Однако это не механическая работа, которая связана с перемещением границы макроскопической системы. На микроскопическом уровне эта работа осуществляется силами, действующими между молекулами на границе контакта более нагретого тела с менее нагретым. Фактически при теплообмене энергия передаётся посредством электромагнитного взаимодействия при столкновениях молекул. Поэтому с точки зрения молекулярно-кинетической теории различие между работой и теплотой проявляется только в том, что совершение механической работы требует упорядоченного движения молекул на макроскопических масштабах, а передача энергии от более нагретого тела менее нагретому этого не требует.
Энергия может также передаваться излучением от одного тела к другому и без их непосредственного контакта.
Количество теплоты не является функцией состояния, и количество теплоты, полученное системой в каком-либо процессе, зависит от способа, которым она была переведена из начального состояния в конечное.
Единица измерения в Международной системе единиц (СИ) — джоуль. Как единица измерения теплоты используется также калория. В Российской Федерации калория допущена к использованию в качестве внесистемной единицы без ограничения срока с областью применения «промышленность»
Количество теплоты входит в математическую формулировку первого начала термодинамики, которую можно записать как Q=A+ΔU{\displaystyle Q=A+\Delta U}. Здесь ΔU{\displaystyle \Delta U} — изменение внутренней энергии системы, Q{\displaystyle Q} — количество теплоты, переданное системе, а A{\displaystyle A} — работа, совершённая системой. Однако определение теплоты должно указывать способ её измерения безотносительно к первому началу. Так как теплота — это энергия переданная в ходе теплообмена, для измерения количества теплоты необходимо пробное калориметрическое тело. По изменению внутренней энергии пробного тела можно будет судить о количестве теплоты, переданном от системы пробному телу. Без использования пробного тела первое начало теряет смысл содержательного закона и превращается в бесполезное для расчётов определение количества теплоты.
Пусть в системе, состоящей из двух тел X{\displaystyle X} и Y{\displaystyle Y}, тело Y{\displaystyle Y} (пробное) заключено в жёсткую адиабатическую оболочку. Тогда оно не способно совершать макроскопическую работу, но может обмениваться энергией (то есть теплотой) с телом X{\displaystyle X}. Предположим, что тело X{\displaystyle X} также почти полностью заключено в адиабатическую, но не жёсткую оболочку, так что оно может совершать механическую работу, но обмениваться теплотой может лишь с Y{\displaystyle Y}.
Таким образом, вводимое в феноменологической термодинамике количество теплоты может быть измерено посредством калориметрического тела (об изменении внутренней энергии которого можно судить по показанию соответствующего макроскопического прибора). Из первого начала термодинамики следует корректность введённого определения количества теплоты, то есть независимость соответствующей величины от выбора пробного тела Y{\displaystyle Y} и способа теплообмена между телами. При таком определении количества теплоты первое начало становится содержательным законом, допускающим экспериментальную проверку, так как все три величины, входящие в выражение для первого начала, могут быть измерены независимо
Предположим, что рассматриваемое тело может обмениваться теплотой лишь с N{\displaystyle N} бесконечными тепловыми резервуарами, внутренняя энергия которых столь велика, что при рассматриваемом процессе температура каждого остаётся строго постоянной. Предположим, что над телом был совершён произвольный круговой процесс, то есть по окончании процесса оно находится абсолютно в том же состоянии, что и в начале. Пусть при этом за весь процесс оно заимствовало из i-го резервуара, находящегося при температуре Ti{\displaystyle T_{i}}, количество теплоты Qi{\displaystyle Q_{i}}. Тогда верно следующее неравенство Клаузиуса:
- ∘∑i=1NQiTi⩽0.{\displaystyle \circ \sum _{i=1}^{N}{\frac {Q_{i}}{T_{i}}}\leqslant 0.}
Здесь ∘{\displaystyle \circ } обозначает круговой процесс. В общем случае теплообмена со средой переменной температуры неравенство принимает вид
- ∮δQ(T)T⩽0.{\displaystyle \oint {\frac {\delta Q(T)}{T}}\leqslant 0.}
Здесь δQ(T){\displaystyle \delta Q(T)} — количество теплоты, переданное участком среды с (постоянной) температурой T{\displaystyle T}. Это неравенство применимо для любого процесса, совершаемого над телом. В частном случае квазистатического процесса оно переходит в равенство. Математически это означает, что для квазистатических процессов можно ввести функцию состояния, называемую энтропией, для которой
- S=∫δQ(T)T,{\displaystyle S=\int {\frac {\delta Q(T)}{T}},}
- dS=δQT.{\displaystyle dS={\frac {\delta Q}{T}}.}
Здесь T{\displaystyle T} — это абсолютная температура внешнего теплового резервуара. В этом смысле 1T{\displaystyle {\frac {1}{T}}} является интегрирующим множителем для количества теплоты, умножением на который получается полный дифференциал функции состояния.
Для неквазистатических процессов такое определение энтропии не работает. Например, при адиабатическом расширении газа в пустоту
- ∫δQ(T)T=0,{\displaystyle \int {\frac {\delta Q(T)}{T}}=0,}
однако энтропия при этом возрастает, в чём легко убедиться, переведя систему в начальное состояние квазистатически и воспользовавшись неравенством Клаузиуса. Кроме того, энтропия (в указанном смысле) не определена для неравновесных состояний системы, хотя во многих случаях систему можно считать локально равновесной и обладающей некоторым распределением энтропии.
Внутренняя энергия системы, в которой возможны фазовые переходы или химические реакции, может изменяться и без изменения температуры. Например, энергия, передаваемая в систему, где жидкая вода находится в равновесии со льдом при нуле градусов Цельсия, расходуется на плавление льда, но температура при этом остаётся постоянной, пока весь лёд не превратится в воду. Такой способ передачи энергии традиционно называется «скрытой» или изотермической теплотой[4] (англ. latent heat), в отличие от «явной», «ощущаемой» или неизотермической теплоты (англ. sensible heat), под которой подразумевается процесс передачи энергии в систему, в результате которого изменяется лишь температура системы, но не её состав.
Энергия, необходимая для фазового перехода единицы массы вещества, называется удельной теплотой фазового превращения[5]. В соответствии с физическим процессом, имеющим место при фазовом превращении, могут выделять теплоту плавления, теплоту испарения, теплоту сублимации (возгонки), теплоту перекристаллизации и т. д. Фазовые превращения идут со скачкообразным изменением энтропии, что сопровождается выделением или поглощением тепла, несмотря на постоянство температуры.
О терминах «теплота», «количество теплоты», «тепловая энергия»[править | править код]
Многие понятия термодинамики возникли в связи с устаревшей теорией теплорода, которая сошла со сцены после выяснения молекулярно-кинетических основ термодинамики. С тех пор они используются и в научном, и в повседневном языке. Хотя в строгом смысле теплота представляет собой один из способов передачи энергии, и физический смысл имеет лишь количество энергии, переданное системе, слово «тепло-» входит в такие устоявшиеся научные понятия, как поток тепла, теплоёмкость, теплота фазового перехода, теплота химической реакции, теплопроводность и пр. Поэтому там, где такое словоупотребление не вводит в заблуждение, понятия «теплота» и «количество теплоты» синонимичны[6]. Однако этими терминами можно пользоваться только при условии, что им дано точное определение, не связанное с представлениями теории теплорода, и ни в коем случае «количество теплоты» нельзя относить к числу первоначальных понятий, не требующих определения[7]. Поэтому некоторые авторы уточняют, что во избежание ошибок теории теплорода под понятием «теплота» следует понимать именно способ передачи энергии, а количество переданной этим способом энергии обозначают понятием «количество теплоты»[8]. Рекомендуется избегать такого термина, как «тепловая энергия», который по смыслу совпадает с внутренней энергией[9].
Выработка энергопредприятиями тепловой и электрической энергии[править | править код]
В связи с зависимостью выработки электроэнергии от выработки тепла паросиловыми установками выделяют несколько видов выработки тепла и электроэнергии.
- Раздельная выработка тепла и электроэнергии.
- Комбинированная выработка тепла и электроэнергии.
Последний тип получения тепловой и электроэнергии является основой теплофикации, и характеризуется как совершенный метод производства энергии.[10]
- ↑ Сивухин, 2005, с. 57.
- ↑ Положение о единицах величин, допускаемых к применению в Российской Федерации. Утверждено Постановлением Правительства РФ от 31 октября 2009 г. № 879. (неопр.) (недоступная ссылка). Дата обращения 16 февраля 2014. Архивировано 2 ноября 2013 года.
- ↑ Сивухин, 2005, с. 58.
- ↑ Путилов, 1971, с. 49.
- ↑ Сивухин, 2005, с. 442.
- ↑ Теплота / Мякишев Г. Я. // Струнино — Тихорецк. — М. : Советская энциклопедия, 1976. — (Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров ; 1969—1978, т. 25).
- ↑ Сивухин, 2005, с. 13.
- ↑ Базаров, 1991, с. 25.
- ↑ Сивухин, 2005, с. 61.
- ↑ Энергосбережение в теплоэнергетике и теплотехнологиях: учебное пособие / Л.И. Молодежникова; Томский политехнический университет. — Томск: Изд-во Томского политехнического университета, 2011. – С.43-45.
- Базаров И. П. Термодинамика. — М.: Высшая школа, 1991. — 376 с.
- Путилов К. А. Термодинамика. — М.: Наука, 1971. — 375 с.
- Сивухин Д. В. Общий курс физики. — Т. II. Термодинамика и молекулярная физика. — 5 изд., испр.. — М.: Физматлит, 2005. — 544 с. — ISBN 5-9221-0601-5.
Количество теплоты
Количество теплоты — энергия, которую получает или теряет тело при теплопередаче. Количество теплоты является одной из основных термодинамических величин. Количество теплоты является функцией процесса, а не функцией состояния, то есть количество теплоты, полученное системой, зависит от способа, которым она была приведена в текущее состояние.
Внутренняя энергия тела может изменяться за счет работы внешних сил. Для характеристики изменения внутренней энергии при теплообмене вводится величина, называемая количеством теплоты и обозначаемая Q. В международной системе единицей количества теплоты, также как работы и энергии, является джоуль: [Q] = [A] = [E] = 1 Дж. На практике еще иногда применяется внесистемная единица количества теплоты – калория. 1 кал. = 4,2 Дж.
Количество теплоты, передаваемое от одного тела к другому, может идти на нагревание тела, плавление, парообразование, либо выделяться при противоположных процессах – остывании тела, кристаллизации, конденсации. Теплота выделяется при сгорании топлива. Между массой вещества и количеством теплоты, необходимым для его нагревания, существует прямая пропорциональная зависимость.
- Количество теплоты, необходимое для нагревания тела или выделяющееся при его охлаждении, прямо пропорционально массе тела и изменению его температуры:
Q = cmΔT, где с — удельная теплоемкость [Дж/кг·К], m — масса тела [кг], ΔT — изменение температуры [К]
- Количество теплоты, необходимое для превращения жидкости в пар или выделяющееся при его конденсации, прямо пропорционально массе жидкости: Q = Lm, где L — удельная теплота парообразования [Дж/кг], m — масса тела [кг]
- Количество теплоты, необходимое для плавления тела или выделяющееся при его кристаллизации, прямо пропорционально массе этого тела:
- Количество теплоты, выделяющееся при сгорании топлива, прямо пропорционально его массе: Q = qm, где q — удельная теплота сгорания [Дж/кг], m — масса тела [кг]
Удельная теплоемкость вещества показывает, чему равно количество теплоты, необходимое для нагревания или выделяющееся при охлаждении 1 кг вещества на 1 К.
Удельные теплоты парообразования, плавления, сгорания показывают, какое количество теплоты требуется для парообразования, плавления или выделяется при конденсации, кристаллизации, сгорании
Другие заметки по физике
Формула количества теплоты в физике
Определение и формула количества теплоты
Внутреннюю энергию термодинамической системы можно изменить двумя способами:
- совершая над системой работу,
- при помощи теплового взаимодействия.
Передача тепла телу не связана с совершением над телом макроскопической работы. В данном случае изменение внутренней энергии вызвано тем, что отдельные молекулы тела с большей температурой совершают работу над некоторыми молекулами тела, которое имеет меньшую температуру. В этом случае тепловое взаимодействие реализуется за счет теплопроводности. Передача энергии также возможна при помощи излучения. Система микроскопических процессов (относящихся не ко всему телу, а к отдельным молекулам) называется теплопередачей. Количество энергии, которое передается от одного тела к другому в результате теплопередачи, определяется количеством теплоты, которое предано от одного тела другому.
Теплотой называют энергию, которая получается (или отдается) телом в процессе теплообмена с окружающими телами (средой). Обозначается теплота, обычно буквой Q.
Это одна из основных величин в термодинамике. Теплота включена в математические выражения первого и второго начал термодинамики. Говорят, что теплота – это энергия в форме молекулярного движения.
Теплота может сообщаться системе (телу), а может забираться от нее. Считают, что если тепло сообщается системе, то оно положительно.
Формула расчета теплоты при изменении температуры
Элементарное количество теплоты обозначим как . Обратим внимание, что элемент тепла, которое получает (отдает) система при малом изменении ее состояния не является полным дифференциалом. Причина этого состоит в том, что теплота является функцией процесса изменения состояния системы.
Элементарное количество тепла, которое сообщается системе, и температура при этом меняется от Tдо T+dT, равно:
где C – теплоемкость тела. Если рассматриваемое тело однородно, то формулу (1) для количества теплоты можно представить как:
где – удельная теплоемкость тела, m – масса тела, — молярная теплоемкость, – молярная масса вещества, – число молей вещества.
Если тело однородно, а теплоемкость считают независимой от температуры, то количество теплоты (), которое получа
Количество теплоты. Тепловой баланс. Видеоурок. Физика 8 Класс
Все тела состоят из атомов и молекул, которые непрерывно движутся и взаимодействуют между собой. Нас интересует суммарная энергия их движения (кинетическая) и взаимодействия (потенциальная) – внутренняя энергия тела.
Внутреннюю энергию можно изменить двумя способами: выполняя работу и с помощью теплообмена.
Про механическую работу мы уже говорили, в ответвлении подробнее рассмотрим, как это связано с изменением внутренней энергии.
Механическая работа и превращение энергии
В механике мы использовали закон сохранения механической энергии:
Полная механическая энергия системы, в которой действуют только консервативные силы, остается постоянной.
Под полной механической энергией мы понимаем сумму кинетической и потенциальной энергии. Значит, энергия превращается из кинетической в потенциальную, и наоборот, чтобы их сумма оставалась постоянной (см. рис. 1).

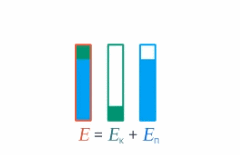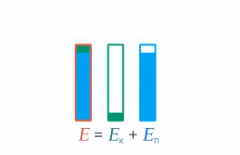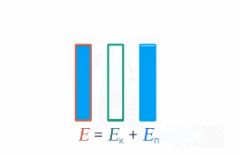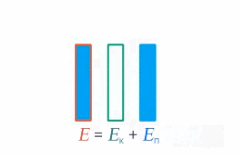
Рис. 1. Превращение кинетической и потенциальной энергий
Изменение кинетической энергии равно изменению потенциальной энергии со знаком минус – это значит, на сколько увеличилась кинетическая энергия, на столько же уменьшилась потенциальная. А работа консервативных сил равна этому изменению:
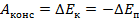
Что же происходит с энергией тела, если на него действуют неконсервативные силы, например сила трения? Механическая энергия не сохраняется, она превращается в другие виды энергии, в частности в тепловую (или внутреннюю энергию тела) (см. рис. 2).
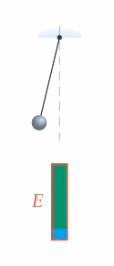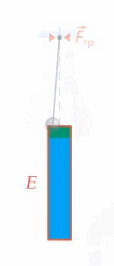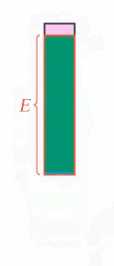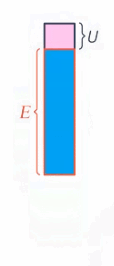
Рис. 2. Превращение механической энергии в тепловую
Работа неконсервативной силы равна изменению механической энергии (а оно равно изменению внутренней энергии со знаком минус, для превращения кинетической энергии в потенциальную мы записывали так же).
При изучении тепловых явлений нас как раз интересует изменение внутренней энергии.
Рассмотрим второй способ изменения внутренней энергии тела – это передача энергии от более теплого объекта к менее теплому. Назвали это теплопередачей и выделили виды теплопередачи: через излучение и через соударения молекул, назвав это теплопроводностью (см. рис. 3).
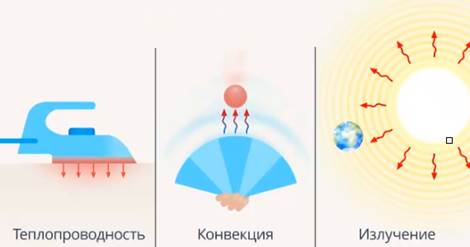
Рис. 3. Виды теплопередачи
Теплопередача может сопровождаться перемещением вещества, этот процесс мы назвали конвекцией.
Но для того чтобы количественно описывать тепловые процессы, нам недостаточно знать сам факт, что теплота передается.
Предположим, что в системе тел неконсервативные силы не совершают механическую работу. Рассмотрим энергию, которую передает или получает тело в результате теплообмена. Вследствие этого изменяется его внутренняя энергия. Эту полученную энергию, равную изменению внутренней энергии, назовем теплотой, а для ее количественного выражения часто будем употреблять название количество теплоты.
О терминах «теплота» и «количество теплоты»
Мы определили теплоту как энергию, которую передает или получает тело в процессе теплообмена. Это физическая величина, единицы измерения у нее те же, что и для энергии. То есть можно сказать «теплота равна 10 Дж» и т. д. Но в русском языке сложилась такая ситуация: если о многих других величинах можно сказать «какая масса?», «какая скорость?», то к теплоте более естественно применить вопрос «сколько?». То есть не «чему равна теплота?», а «сколько теплоты?», или, другими словами: «какое количество теплоты?». Это понятие, «количество теплоты», мы применяем наряду с понятием «теплота», но стоит помнить, что подразумевается одна и та же физическая величина. Просто иногда удобнее сказать «теплота передалась», а иногда «количество теплоты равно 10 Дж».
Обратите внимание: теплота равна изменению внутренней энергии тела. То есть мы не будем говорить об абсолютном количестве теплоты, а только о его изменении. То есть отвечать на вопрос: «Сколько теплоты получило или передало тело?». А привычные нам понятия «тепло/холодно» лучше всего описывает такая физическая величина, как температура.
Ощущаем ли мы температуру?
Касаясь чашки с горячим чаем, вы чувствуете ее тепло (см. рис. 4).

Рис. 4. Чашка с горячим чаем
Кажется, что мы определяем ее температуру и можем судить о внутренней энергии. А попробуйте провести следующий опыт: опустите одну руку в теплую воду, другую – в холодную, чтобы руки «привыкли» к температуре (см. рис. 5).

Рис. 5. Проведение эксперимента
А затем поместите их обе в воду комнатной температуры. Одной рукой вы почувствуете холод, другой – тепло. Получается, что наши ощущения связаны не с абсолютным значением температуры тела, а с разностью температур тела и нашей руки и с направлением теплообмена между ними.
Одна рука чувствует тепло, поскольку теплота передается от воды к руке. А вторая рука чувствует холод, поскольку тепло передается от руки к воде. При этом в случае холодной воды это не вода передает руке холод, а рука отдает воде тепло.
Конечно, мы иногда говорим «закрой дверь – холод напустишь» (как будто подразумеваем передачу именно холода), но это обывательский оборот, который закрепился в языке.
Например, при игре в пятнашки мы всегда двигаем сами «костяшки», но часто говорим о перемещении пустой клетки.
Мы говорим: «становится темно». Хотя темнота – это отсутствие света. Августин Блаженный говорил: «Нет зла, есть недостаток добра».
Так и с холодом – это отсутствие тепла. Нет передачи холода, есть теплопередача в том или ином направлении. Поэтому и лед, и чай, укутанные в шубу, будут некоторое время сохранять температуру, здесь у шубы одна и та же функция – теплоизоляция.
Обычно количество теплоты обозначается буквой Q. Количество теплоты – это изменение внутренней энергии при теплообмене, значит, эта величина измеряется, как и энергия, в джоулях: [Q] = Дж.
Обозначим внутреннюю энергию U. Тогда определение количества теплоты можно записать следующим образом:
Q = ΔU при равной нулю механической работе внешних сил (о чем мы договорились в начале урока).
Если тело получило 10 Дж теплоты и если тело потеряло 10 Дж теплоты – это не одно и то же (см. рис. 6).
Рис. 6. Получение и потеря теплоты
Как это обозначить? Для этого можем использовать удобный математический инструмент – отрицательные числа. Мы его уже использовали для обозначения направления движения. Если рассматривать прямолинейное движение вдоль одной прямой, удобно выбрать ось координат и одно направление считать положительным (см. рис. 7).
Рис. 7. Выбор положительного направления
В проекции на эту ось скорости тел 5 м/с и –5 м/с означают, что тела движутся со скоростью 5 м/с в противоположных направлениях.
Так и здесь: договоримся, что если тело получает теплоту (наши руки получили от теплой воды 10 Дж тепла), то Q положительно (запишем Q = 10 Дж), а если отдает – отрицательно, запишем Q = –10 Дж.
Остановимся пока на изучении тех случаев, когда агрегатное состояние вещества не меняется. Тогда если передать тепло телу, то оно нагреется, увеличится его температура (см. рис. 8)
. 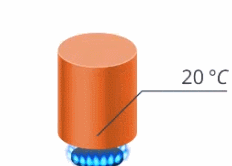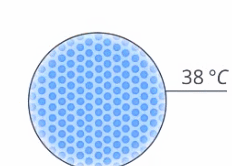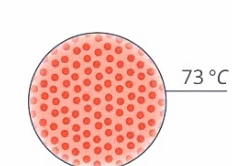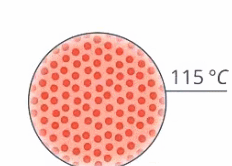
Рис. 8. Агрегатное состояние вещества не изменяется при получении теплоты
Разберемся, как количественно описать этот процесс.
Чайник закипит быстрее, если в него залить теплую воду, а не холодную (см. рис. 9).

Рис. 9. Закипание чайника с теплой и холодной водой
То есть чем большей разности конечной и начальной температур нужно достичь, тем больше нужно передать энергии. Полный чайник будет закипать дольше, чем почти пустой (см. рис. 10).
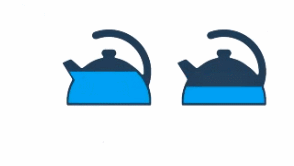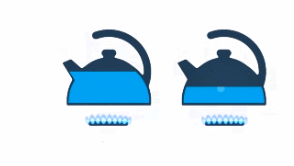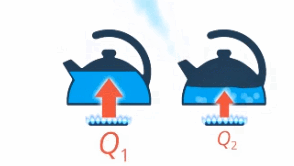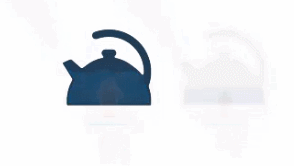
Рис. 10. Закипание полного чайника и полупустого
То есть чем больше масса воды, тем больше нужно передать энергии, чтобы ее нагреть. И наверняка есть разница, нагреть на одни и те же 10 градусов килограмм воды или килограмм железа – это тоже нужно учесть (см. рис. 11).

Рис. 11. Нагревание разных веществ
Можно провести эксперименты и установить более точные закономерности.
Оказывается, количество теплоты, которое необходимо передать телу, прямо пропорционально изменению температуры: 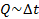 , где
, где 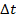 обозначает изменение температуры: конечная температура минус начальная
обозначает изменение температуры: конечная температура минус начальная  .
.
Если тело отдает тепло, то оно охлаждается. Конечная температура будет меньше начальной: 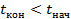 . Тогда
. Тогда 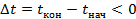 . Количество теплоты также будет
. Количество теплоты также будет 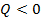 . Это согласуется с введенным понятием количества теплоты: если тело отдает тепло, то
. Это согласуется с введенным понятием количества теплоты: если тело отдает тепло, то 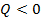 .
.
Экспериментально также было установлено, что:  (количество теплоты, которое необходимо передать телу, прямо пропорционально массе тела).
(количество теплоты, которое необходимо передать телу, прямо пропорционально массе тела).
Почему изменение внутренней энергии пропорционально массе?
Количество теплоты, которое получает тело, идет на увеличение его внутренней энергии. Внутренняя энергия – это суммарная энергия частиц вещества: атомов или молекул. Значит, изменение внутренней энергии должно быть пропорционально количеству частиц: 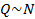 .
.
Однако таким параметром, как количество молекул, мы пользуемся редко. Более удобной характеристикой, эквивалентной количеству частиц данного вещества, является масса.
Масса вещества равна массе одной частицы (атома или молекулы), умноженной на количество частиц: 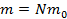 , тогда количество молекул равно
, тогда количество молекул равно 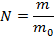 .
.
Получаем, что  или
или  , т. к. масса одной молекулы – величина постоянная для данного вещества и она будет заложена в коэффициенте пропорциональности, который определяется отдельно для каждого вещества и учитывает его параметры: массу молекул, связь между ними, связь кинетической энергии молекул и температуры и т. д.
, т. к. масса одной молекулы – величина постоянная для данного вещества и она будет заложена в коэффициенте пропорциональности, который определяется отдельно для каждого вещества и учитывает его параметры: массу молекул, связь между ними, связь кинетической энергии молекул и температуры и т. д.
Количество теплоты пропорционально массе тела и изменению его температуры:

Кроме того, количество теплоты, необходимое для нагревания данной массы на данную температуру, зависит от вещества: для спирта нужно меньше теплоты, чем для воды (см. рис. 12), а для золота – меньше, чем для железа (см. рис. 13).
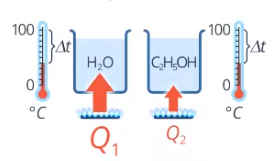
Рис. 12. Количество теплоты для нагревания воды и спирта

Рис. 13. Количество теплоты для нагревания железа и золота
Для данного вещества количество теплоты, которое нужно передать для нагревания данной m на данную 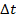 , оказалось постоянной величиной.
, оказалось постоянной величиной.
Отношение 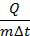 назвали удельной теплоемкостью, которую принято обозначать буквой c. Это количество теплоты, которое нужно передать 1 кг вещества, чтобы нагреть его на 1 °С (или 1 К, потому что мы говорим об изменении температуры, а цена деления этих двух шкал одинакова (см. рис. 14)).
назвали удельной теплоемкостью, которую принято обозначать буквой c. Это количество теплоты, которое нужно передать 1 кг вещества, чтобы нагреть его на 1 °С (или 1 К, потому что мы говорим об изменении температуры, а цена деления этих двух шкал одинакова (см. рис. 14)).

Рис. 14. Шкалы температур Цельсия и Кельвина
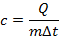
Для разных веществ это отношение отличается.
Единицы измерения удельной теплоемкости:
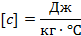
Различные вещества имеют различные удельные теплоемкости. Почему это так – поговорим в ответвлении.
c = const
Удельная теплоемкость с зависит от температуры t. Чтобы нагреть один и тот же железный шарик с 10 градусов до 11 и с 200 до 201 – нужно разное количество теплоты (см. рис. 15).
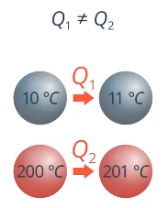
Рис. 15. Нагрев одного и того же шарика на 1 градус
Изменение удельной теплоемкости с изменением температуры достаточно мало, поэтому для решения задач мы можем считать, что с = const и зависимость 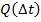 линейная (на участках, где не изменяется агрегатное состояние вещества (см. рис. 16)).
линейная (на участках, где не изменяется агрегатное состояние вещества (см. рис. 16)).

Рис. 16. Линейная зависимость  на участках, где не изменяется агрегатное состояние вещества
на участках, где не изменяется агрегатное состояние вещества
На самом деле, с, кроме температуры, зависит и от давления, но обычно мы будем решать задачи, в которых описаны процессы при нормальном атмосферном давлении, поэтому и здесь можно считать с = const.
Почему у веществ различные удельные теплоемкости
Почему для нагревания одной и той же массы на одну и ту же температуру для разных веществ нужно разное количество энергии?
Мы определили внутреннюю энергию тела как сумму кинетической и потенциальной энергии всех частиц тела. Когда теплота передается телу, часть ее идет на увеличение кинетической энергии (а значит, увеличение температуры), а часть – на увеличение потенциальной энергии частиц (см. рис. 17).
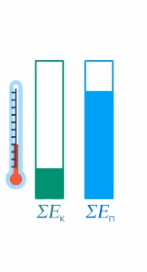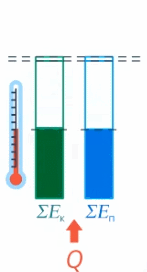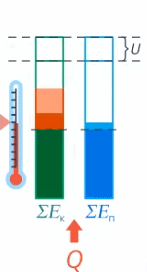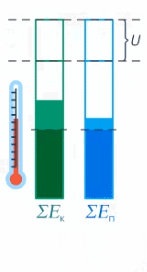
Рис. 17. Внутренняя энергия тела
У разных веществ соотношение этих частей разное.
Например, двум разным телам передали 100 Дж теплоты (см. рис. 18).

Рис. 18. Нагревание разных тел
У одного тела 40 Дж ушло в кинетическую энергию, а 60 – в потенциальную. У другого в кинетическую энергию перешло 20 Дж, 80 – в потенциальную. Итого тела получили одинаковое количество теплоты, но первое тело нагрелось больше, чем второе, т. к. кинетическая энергия его частиц увеличилась сильнее (40 Дж > 20 Дж). Это значит, что удельная теплоемкость второго вещества больше – ведь его труднее нагреть, чем первое.
Для разных веществ полученная энергия может распределяться по-разному – для нас это не ново.
Возьмем три мяча (см. рис. 19): хорошо накачанный, спущенный и деревянный.

Рис. 19. Опыт с тремя мячами
Если ударить по ним, сообщив одинаковую энергию, полетят они с разной скоростью. Часть переданной энергии пойдет на неупругую деформацию мяча и обуви бьющего, а часть – на увеличение кинетической энергии мяча. Для перечисленных мячей соотношение этих частей будет разное.
Значения удельных теплоемкостей различных веществ уже измерены, их можно найти в соответствующих таблицах.
Итак, на основе всего вышесказанного можно записать формулу для расчета количества теплоты, необходимого для нагревания тела:
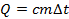
Процессы нагревания и охлаждения отличаются лишь знаком 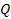 , так что формулу можно использовать и для расчета количества теплоты, которое выделяет тело при охлаждении.
, так что формулу можно использовать и для расчета количества теплоты, которое выделяет тело при охлаждении.
Для задач, которые мы будем решать в ближайшее время, нам достаточно такого очевидного утверждения: тепло передается от тела с большей температурой к телу с меньшей температурой до тех пор, пока температуры этих тел не уравняются (см. рис. 20).

Рис. 20. Теплообмен между телами с разной температурой
Более точно эта закономерность сформулирована в виде законов термодинамики, но их мы будем подробно изучать позже.
Мы сейчас рассматриваем изменение внутренней энергии тел через передачу теплоты. Если выделить систему тел, которые будем рассматривать вместе в рамках решения конкретной задачи, то возможны два варианта.
Первый – энергия может быть получена извне этой системы (см. рис. 21)

Рис. 21. Теплообмен с другими телами вне системы
(например, теплообмен с другими телами вне системы, превращение механической энергии в тепловую и т. д.). Второй вариант – считаем, что энергия передается посредством теплообмена только внутри системы, тогда суммарная энергия системы не меняется (см. рис. 22).

Рис. 22. Теплообмен только внутри системы
Рассмотрим первый случай, когда тепло передается системе тел извне.
В алюминиевой кастрюле массой 1,5 кг находится 5 кг воды при температуре 20 °С (см. рис. 23).

Рис. 23. Задача 1
Най
Количество теплоты. Удельная теплоемкость. Видеоурок. Физика 10 Класс
На этом уроке мы продолжим изучение внутренней энергии тела, а конкретнее – способов её изменения. И предметом нашего внимания на этот раз станет теплообмен. Мы вспомним, на какие виды он разделяется, в чём измеряется, и по каким соотношениям можно вычислить количество теплоты, переданное в результате теплообмена, также мы дадим определение удельной теплоёмкости тела.
Тема: Основы термодинамики
Урок: Количество теплоты. Удельная теплоемкость
Как мы уже знаем из младших классов, и как мы вспомнили на прошлом уроке, существует два способа изменить внутреннюю энергию тела: выполнить над ним работу или передать ему некое количество теплоты. О первом способе нам уже известно из, опять-таки, прошлого урока, но и о втором мы достаточно много говорили в курсе восьмого класса.
Процесс передачи теплоты (количества теплоты или энергии) без совершения работы называется теплообменом или теплопередачей. Разделяется он по механизмам передачи, как мы знаем, на три вида:
- Теплопроводность
- Конвекция
- Излучение
В результате одного из этих процессов телу передаётся некое количество теплоты, на значение которого, собственно, и меняется внутренняя энергия. Охарактеризуем эту величину.
Определение. Количество теплоты. Обозначение – Q. Единицы измерения – Дж. При изменении температуры тела (что эквивалентно изменению внутренней энергии) количество теплоты, затраченное на это изменение, можно вычислить по формуле:
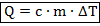
Здесь: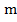 — масса тела;
— масса тела; 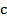 — удельная теплоёмкость тела;
— удельная теплоёмкость тела; 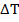 – изменение температуры тела.
– изменение температуры тела.
Причём, если 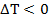 , то есть при охлаждении, говорят, что тело отдало некоторое количество теплоты, или же телу передали отрицательное количество теплоты. Если же
, то есть при охлаждении, говорят, что тело отдало некоторое количество теплоты, или же телу передали отрицательное количество теплоты. Если же  , то есть наблюдается нагрев тела, количество переданной теплоты, конечно же, будет положительным.
, то есть наблюдается нагрев тела, количество переданной теплоты, конечно же, будет положительным.
Особое внимание следует обратить на величину удельной теплоёмкости тела.
Определение. Удельная теплоёмкость – величина, численно равная количеству теплоты, которую необходимо передать, чтобы нагреть один килограмм вещества на один градус. Удельная теплоёмкость – индивидуальная величина для каждого отдельного вещества. Поэтому это табличная величина, заведомо известная при условии, что нам известно, порции какого вещества передаётся тепло.
Единицу измерения удельной теплоёмкости в системе СИ можно получить из вышеприведённого уравнения:
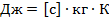
Таким образом:
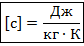
Рассмотрим теперь случаи, когда передача некого количества теплоты приводит к изменению агрегатного состояния вещества. Напомним, что такие переходы называются плавлением, кристаллизацией, испарением и конденсацией.
При переходе от жидкости к твёрдому телу и наоборот количество теплоты высчитывается по формуле:

Здесь:  — масса тела;
— масса тела; 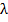 — удельная теплота плавления тела (количество теплоты, необходимое для полного плавления одного килограмма вещества).
— удельная теплота плавления тела (количество теплоты, необходимое для полного плавления одного килограмма вещества).
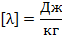
Для того чтобы расплавить тело, ему необходимо передать некое количество теплоты, а при конденсации тело само отдаёт в окружающую среду некое количество теплоты.
При переходе от жидкости к газообразному телу и наоборот количество теплоты высчитывается по формуле:
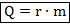
Здесь:  — масса тела;
— масса тела; 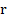 — удельная теплота парообразования тела (количество теплоты, необходимое для полного испарения одного килограмма вещества).
— удельная теплота парообразования тела (количество теплоты, необходимое для полного испарения одного килограмма вещества).
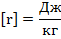
Для того чтобы испарить жидкость, ей необходимо передать некое количество теплоты, а при конденсации пар сам отдаёт в окружающую среду некое количество теплоты.
Следует подчеркнуть также, что и плавление с кристаллизацией, и испарение с конденсацией проходят при постоянной температуре (температура плавления и кипения соответственно) (рис. 1).
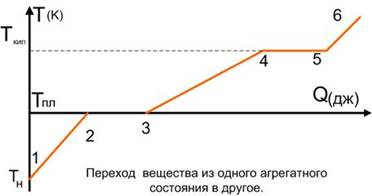
Рис. 1. График зависимости температуры (в градусах Цельсия) от полученного количества вещества (Источник)
Отдельно стоит отметить вычисление количества теплоты, выделяющееся при сгорании некоторой массы топлива:
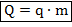
Здесь:  — масса топлива;
— масса топлива; 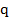 — удельная теплота сгорания топлива (количество теплоты, выделяющееся при сгорании одного килограмма топлива).
— удельная теплота сгорания топлива (количество теплоты, выделяющееся при сгорании одного килограмма топлива).
Особое внимание нужно обратить на тот факт, что помимо того, что для разных веществ удельные теплоёмкости принимают разные значения, этот параметр может быть различным и для одного и того же вещества при различных условиях. Например, выделяют разные значения удельных теплоёмкостей для процессов нагревания, протекающих при постоянном объёме ( ) и для процессов, протекающих при постоянном давлении (
) и для процессов, протекающих при постоянном давлении (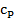 ).
).
Различают также молярную теплоёмкость и просто теплоёмкость.
Определение. Молярная теплоёмкость (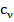 ) – количество теплоты, необходимое для того, чтобы нагреть один моль вещества на один градус.
) – количество теплоты, необходимое для того, чтобы нагреть один моль вещества на один градус.
Теплоёмкость (C) – количество теплоты, необходимое, чтобы нагреть на один градус порцию вещества определённой массы. Связь теплоёмкости с удельной теплоёмкостью:

На следующем уроке мы рассмотрим такой важный закон, как первый закон термодинамики, который связывает изменение внутренней энергии с работой газа и количеством переданной теплоты.
Список литературы
- Мякишев Г.Я., Синяков А.З. Молекулярная физика. Термодинамика. – М.: Дрофа, 2010.
- Генденштейн Л.Э., Дик Ю.И. Физика 10 класс. – М.: Илекса, 2005.
- Касьянов В.А. Физика 10 класс. – М.: Дрофа, 2010.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Словари и энциклопедии на Академике (Источник).
- Tt.pstu.ru (Источник).
- Elementy.ru (Источник).
Домашнее задание
- Стр. 83: № 643–646. Физика. Задачник. 10-11 классы. Рымкевич А.П. – М.: Дрофа, 2013. (Источник)
- Как связаны между собой молярная и удельная теплоёмкости?
- Почему иногда поверхности окон запотевают? С какой стороны окон это происходит?
- В какую погоду быстрее высыхают лужи: в спокойную или в ветреную?
- *На что затрачивается теплота, полученная телом при плавлении?
Удельная теплота парообразования и конденсации — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 19 декабря 2018; проверки требуют 6 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 19 декабря 2018; проверки требуют 6 правок.Уде́льная теплота́ парообразова́ния и конденса́ции — физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить количество жидкости с единичной массой в пар , при данной температуре жидкости и без её изменения (температуры) в процессе испарения. Равна удельной теплоте конденсации единичной массы пара в жидкость.
Удельная теплота парообразования и конденсации обозначается буквой L{\displaystyle L}. Рассчитывается по формуле:
- L=Qm,{\displaystyle L={\,Q \over m},}
где Q — теплота, истраченная на превращение жидкости в пар или пара в жидкость, m — масса.
Наименьшее значение удельной теплоты парообразования будет при температуре кипения жидкости.
Размерность удельной теплоты парообразования в СИ — Дж/кг. Устаревшие, но иногда применяемые единицы для теплоты парообразования — ккал/кг и кал/кг.
В химии теплота парообразования обычно приводится к молю вещества. Эта величина называется молярной теплотой испарения (конденсации); единица её измерения — Дж/моль. Также используются устаревшие единицы: ккал/моль, кал/моль.
Удельная теплота парообразования некоторых веществ при нормальном атмосферном давлении (760 мм. рт. ст. = 101,325 кПа) и температуре, равной температуре кипения вещества[1]:
Количество теплоты и тепловая мощность. Расчет в Excel.
Опубликовано 13 Окт 2013
Рубрика: Теплотехника | 82 комментария
Человечеству известно немного видов энергии – механическая энергия (кинетическая и потенциальная), внутренняя энергия (тепловая), энергия полей (гравитационная, электромагнитная и ядерная), химическая. Отдельно стоит выделить энергию взрыва,…
…энергию вакуума и еще существующую только в теории – темную энергию. В этой статье, первой в рубрике «Теплотехника», я попытаюсь на простом и доступном языке, используя практический пример, рассказать о важнейшем виде энергии в жизни людей — о тепловой энергии и о рождающей ее во времени тепловой мощности.
Несколько слов для понимания места теплотехники, как раздела науки о получении, передаче и применении тепловой энергии. Современная теплотехника выделилась из общей термодинамики, которая в свою очередь является одним из разделов физики. Термодинамика – это дословно «теплый» плюс «силовой». Таким образом, термодинамика – это наука об «изменении температуры» системы.
Воздействие на систему извне, при котором изменяется ее внутренняя энергия, может являться результатом теплообмена. Тепловая энергия, которая приобретается или теряется системой в результате такого взаимодействия с окружающей средой, называется количеством теплоты и измеряется в системе СИ в Джоулях.
Если вы не инженер-теплотехник, и ежедневно не занимаетесь теплотехническими вопросами, то вам, столкнувшись с ними, иногда без опыта бывает очень трудно быстро в них разобраться. Трудно без наличия опыта представить даже размерность искомых значений количества теплоты и тепловой мощности. Сколько Джоулей энергии необходимо чтобы нагреть 1000 метров кубических воздуха от температуры -37˚С до +18˚С?.. Какая нужна мощность источника тепла, чтобы сделать это за 1 час?.. На эти не самые сложные вопросы способны сегодня ответить «сходу» далеко не все инженеры. Иногда специалисты даже помнят формулы, но применить их на практике могут лишь единицы!
Прочитав до конца эту статью, вы сможете легко решать реальные производственные и бытовые задачи, связанные с нагревом и охлаждением различных материалов. Понимание физической сути процессов теплопередачи и знание простых основных формул – это главные блоки в фундаменте знаний по теплотехнике!
Количество теплоты при различных физических процессах.
Большинство известных веществ могут при разных температуре и давлении находиться в твердом, жидком, газообразном или плазменном состояниях. Переход из одного агрегатного состояния в другое происходит при постоянной температуре (при условии, что не меняются давление и другие параметры окружающей среды) и сопровождается поглощением или выделением тепловой энергии. Не смотря на то, что во Вселенной 99% вещества находится в состоянии плазмы, мы в этой статье не будем рассматривать это агрегатное состояние.
Рассмотрим график, представленный на рисунке. На нем изображена зависимость температуры вещества Т от количества теплоты Q, подведенного к некой закрытой системе, содержащей определенную массу какого-то конкретного вещества.
1. Твердое тело, имеющее температуру T1, нагреваем до температуры Tпл, затрачивая на этот процесс количество теплоты равное Q1.
2. Далее начинается процесс плавления, который происходит при постоянной температуре Тпл (температуре плавления). Для расплавления всей массы твердого тела необходимо затратить тепловой энергии в количестве Q2— Q1.
3. Далее жидкость, получившаяся в результате плавления твердого тела, нагреваем до температуры кипения (газообразования) Ткп, затрачивая на это количество теплоты равное Q3—Q2.
4. Теперь при неизменной температуре кипения Ткп жидкость кипит и испаряется, превращаясь в газ. Для перехода всей массы жидкости в газ необходимо затратить тепловую энергию в количестве Q4—Q3.
5. На последнем этапе происходит нагрев газа от температуры Ткп до некоторой температуры Т2. При этом затраты количества теплоты составят Q5—Q4. (Если нагреем газ до температуры ионизации, то газ превратится в плазму.)
Таким образом, нагревая исходное твердое тело от температуры Т1 до температуры Т2 мы затратили тепловую энергию в количестве Q5, переводя вещество через три агрегатных состояния.
Двигаясь в обратном направлении, мы отведем от вещества то же количество тепла Q5, пройдя этапы конденсации, кристаллизации и остывания от температуры Т2 до температуры Т1. Разумеется, мы рассматриваем замкнутую систему без потерь энергии во внешнюю среду.
Заметим, что возможен переход из твердого состояния в газообразное состояние, минуя жидкую фазу. Такой процесс именуется возгонкой, а обратный ему процесс – десублимацией.
Итак, уяснили, что процессы переходов между агрегатными состояниями вещества характеризуются потреблением энергии при неизменной температуре. При нагреве вещества, находящегося в одном неизменном агрегатном состоянии, повышается температура и также расходуется тепловая энергия.
Главные формулы теплопередачи.
Формулы очень просты.
Количество теплоты Q в Дж рассчитывается по формулам:
1. Со стороны потребления тепла, то есть со стороны нагрузки:
1.1. При нагревании (охлаждении):
Q=m*c*(Т2-Т1)
Здесь и далее:
m – масса вещества в кг
с – удельная теплоемкость вещества в Дж/(кг*К)
1.2. При плавлении (замерзании):
Q=m*λ
λ – удельная теплота плавления и кристаллизации вещества в Дж/кг
1.3. При кипении, испарении (конденсации):
Q=m*r
r – удельная теплота газообразования и конденсации вещества в Дж/кг
2. Со стороны производства тепла, то есть со стороны источника:
2.1. При сгорании топлива:
Q=m*q
q – удельная теплота сгорания топлива в Дж/кг
2.2. При превращении электроэнергии в тепловую энергию (закон Джоуля — Ленца):
Q=t*I*U=t*R*I^2=(t/R)*U^2
t – время в с
I – действующее значение тока в А
U – действующее значение напряжения в В
R – сопротивление нагрузки в Ом
Делаем вывод – количество теплоты прямо пропорционально массе вещества при всех фазовых превращениях и при нагреве дополнительно прямо пропорционально разности температур. Коэффициенты пропорциональности (c, λ, r, q) для каждого вещества имеют свои значения и определены опытным путем (берутся из справочников).
Тепловая мощность N в Вт – это количество теплоты переданное системе за определенное время:
N=Q/t
Чем быстрее мы хотим нагреть тело до определенной температуры, тем большей мощности должен быть источник тепловой энергии – все логично.
Расчет в Excel прикладной задачи.
В жизни бывает часто необходимо сделать быстрый оценочный расчет, чтобы понять – имеет ли смысл продолжать изучение темы, делая проект и развернутые точные трудоемкие расчеты. Сделав за несколько минут расчет даже с точностью ±30%, можно принять важное управленческое решение, которое будет в 100 раз более дешевым и в 1000 раз более оперативным и в итоге в 100000 раз более эффективным, чем выполнение точного расчета в течение недели, а то и месяца, группой дорогостоящих специалистов…
Условия задачи:
В помещение цеха подготовки металлопроката размерами 24м х 15м х 7м завозим со склада на улице металлопрокат в количестве 3т. На металлопрокате есть лед общей массой 20кг. На улице -37˚С. Какое количество теплоты необходимо, чтобы нагреть металл до +18˚С; нагреть лед, растопить его и нагреть воду до +18˚С; нагреть весь объем воздуха в помещении, если предположить, что до этого отопление было полностью отключено? Какую мощность должна иметь система отопления, если все вышесказанное необходимо выполнить за 1час? (Очень жесткие и почти не реальные условия – особенно касающиеся воздуха!)
Расчет выполним в программе MS Excel или в программе OOo Calc.
С цветовым форматированием ячеек и шрифтов ознакомьтесь на странице «О блоге».
Исходные данные:
1. Названия веществ пишем:
в ячейку D3: Сталь
в ячейку E3: Лед
в ячейку F3: Лед/вода
в ячейку G3: Вода
в ячейку G3: Воздух
2. Названия процессов заносим:
в ячейки D4, E4, G4, G4: нагрев
в ячейку F4: таяние
3. Удельную теплоемкость веществ c в Дж/(кг*К) пишем для стали, льда, воды и воздуха соответственно
в ячейку D5: 460
в ячейку E5: 2110
в ячейку G5: 4190
в ячейку H5: 1005
4. Удельную теплоту плавления льда λ в Дж/кг вписываем
в ячейку F6: 330000
5. Массу веществ m в кг вписываем соответственно для стали и льда
в ячейку D7: 3000
в ячейку E7: 20
Так как при превращении льда в воду масса не изменяется, то
в ячейках F7 и G7: =E7=20
Массу воздуха находим произведением объема помещения на удельный вес
в ячейке H7: =24*15*7*1,23=3100
6. Время процессов t в мин пишем только один раз для стали
в ячейку D8: 60
Значения времени для нагрева льда, его плавления и нагрева получившейся воды рассчитываются из условия, что все эти три процесса должны уложиться в сумме за такое же время, какое отведено на нагрев металла. Считываем соответственно
в ячейке E8: =E12/(($E$12+$F$12+$G$12)/D8)=9,7
в ячейке F8: =F12/(($E$12+$F$12+$G$12)/D8)=41,0
в ячейке G8: =G12/(($E$12+$F$12+$G$12)/D8)=9,4
Воздух также должен прогреться за это же самое отведенное время, читаем
в ячейке H8: =D8=60,0
7. Начальную температуру всех веществ T1 в ˚C заносим
в ячейку D9: -37
в ячейку E9: -37
в ячейку F9: 0
в ячейку G9: 0
в ячейку H9: -37
8. Конечную температуру всех веществ T2 в ˚C заносим
в ячейку D10: 18
в ячейку E10: 0
в ячейку F10: 0
в ячейку G10: 18
в ячейку h20: 18
Думаю, вопросов по п.7 и п.8 быть недолжно.
Результаты расчетов:
9. Количество теплоты Q в КДж, необходимое для каждого из процессов рассчитываем
для нагрева стали в ячейке D12: =D7*D5*(D10-D9)/1000=75900
для нагрева льда в ячейке E12: =E7*E5*(E10-E9)/1000= 1561
для плавления льда в ячейке F12: =F7*F6/1000= 6600
для нагрева воды в ячейке G12: =G7*G5*(G10-G9)/1000= 1508
для нагрева воздуха в ячейке h22: =H7*H5*(h20-H9)/1000= 171330
Общее количество необходимой для всех процессов тепловой энергии считываем
в объединенной ячейке D13E13F13G13h23: =СУММ(D12:h22) = 256900
В ячейках D14, E14, F14, G14, h24, и объединенной ячейке D15E15F15G15h25 количество теплоты приведено в дугой единице измерения – в ГКал (в гигакалориях).
10. Тепловая мощность N в КВт, необходимая для каждого из процессов рассчитывается
для нагрева стали в ячейке D16: =D12/(D8*60)=21,083
для нагрева льда в ячейке E16: =E12/(E8*60)= 2,686
для плавления льда в ячейке F16: =F12/(F8*60)= 2,686
для нагрева воды в ячейке G16: =G12/(G8*60)= 2,686
для нагрева воздуха в ячейке h26: =h22/(H8*60)= 47,592
Суммарная тепловая мощность необходимая для выполнения всех процессов за время t рассчитывается
в объединенной ячейке D17E17F17G17h27: =D13/(D8*60) = 71,361
В ячейках D18, E18, F18, G18, h28, и объединенной ячейке D19E19F19G19h29 тепловая мощность приведена в дугой единице измерения – в Гкал/час.
На этом расчет в Excel завершен.
Выводы:
Обратите внимание, что для нагрева воздуха необходимо более чем в два раза больше затратить энергии, чем для нагрева такой же массы стали.
При нагреве воды затраты энергии в два раза больше, чем при нагреве льда. Процесс плавления многократно больше потребляет энергии, чем процесс нагрева (при небольшой разности температур).
Нагрев воды в десять раз затрачивает больше тепловой энергии, чем нагрев стали и в четыре раза больше, чем нагрев воздуха.
Для получения информации о выходе новых статей и для скачивания рабочих файлов программ прошу вас подписаться на анонсы в окне, расположенном в конце статьи или в окне вверху страницы.
После ввода адреса своей электронной почты и нажатия на кнопку «Получать анонсы статей» НЕ ЗАБУДЬТЕ ПОДТВЕРДИТЬ ПОДПИСКУ кликом по ссылке в письме, которое тут же придет к вам на указанную почту (иногда — в папку «Спам»)!
Мы вспомнили понятия «количество теплоты» и «тепловая мощность», рассмотрели фундаментальные формулы теплопередачи, разобрали практический пример. Надеюсь, что мой язык был прост, понятен и интересен.
Жду вопросы и комментарии на статью!
Прошу УВАЖАЮЩИХ труд автора скачать файл ПОСЛЕ ПОДПИСКИ на анонсы статей.
Ссылка на скачивание файла: raschet-teplovoy-moshchnosti (xls 19,5KB).
Другие статьи автора блога
На главную



