Конденсация — Википедия
 Роса на паутине
Роса на паутине  Конденсация на бутылке холодной воды
Конденсация на бутылке холодной воды  Конденсация водяного пара в воздухе над чашкой горячей воды
Конденсация водяного пара в воздухе над чашкой горячей воды 
Конденса́ция паров (лат. condense «накопляю, уплотняю, сгущаю») — переход вещества в жидкое или твёрдое[1] состояние из газообразного (обратный последнему процессу называется сублимация). Максимальная температура, ниже которой происходит конденсация, называется критической. Пар, из которого может происходить конденсация, бывает насыщенным или ненасыщенным.
Конденсация имеет место во многих теплообменных аппаратах (например, в мазутоподогревателях на ТЭС), в опреснительных установках, технологических аппаратах (перегонные аппараты). Важнейшее применение на ТЭС — конденсаторы паровых турбин. В них конденсация происходит на охлаждаемых водой трубах. Для повышения КПД термодинамического цикла ТЭС важно снижать температуру конденсации (за счёт понижения давления), и обычно она близка к температуре охлаждающей воды (до 25÷30 °C).
Конденсация — процесс, в определённом смысле обратный к кипению. Но при конденсации важнее проблемы повышения теплоотдачи, чтобы при малых температурных напорах обеспечить быстрый отбор теплоты.
Виды конденсации[править | править код]
Конденсация может происходить в объёме (туман, дождь) и на охлаждаемой поверхности. В теплообменных аппаратах – конденсация на охлаждаемой поверхности. Её далее и будем рассматривать. Разумеется, при такой конденсации температура поверхности стенки Tw должна быть меньше температуры насыщения Ts, то есть Tw < Ts. В свою очередь, конденсация на охлаждаемой поверхности может быть двух видов:[2]
- Плёночная конденсация – имеет место, когда жидкость смачивает поверхность (жидкость – смачивающая, поверхность – смачиваемая, эти свойства изучаются в курсе Физики), тогда конденсат образует сплошную плёнку.
- Капельная конденсация
При плёночной конденсации теплоотдача намного меньше из-за термического сопротивления плёнки (плёнка мешает отводу тепла от пара к стенке). К сожалению, реализовать капельную конденсацию сложно – несмачиваемые материалы и покрытия (например, типа фторопласта) сами плохо проводят теплоту. А использование добавок – гидрофобизаторов (для воды типа масла, керосина) оказалось неэффективным. Поэтому обычно в теплообменных аппаратах имеет место пленочная конденсация. Гидрофобизатор, гидрофобность – от греческих “hydör” – “вода” и “phóbos” – страх. То есть гидрофобный – то же, что водоотталкивающий, несмачиваемый. Такие добавки для произвольных жидкостей называются лиофобизаторами.
Термин “неподвижный пар” в данном случае подразумевает отсутствие существенного вынужденного движения (разумеется, свободно-конвективное движение будет иметь место).
На поверхности стенки образуется плёнка конденсата. Она стекает вниз, при этом её толщина растёт благодаря продолжающейся конденсации (рис. …). Из-за термического сопротивления плёнки температура стенки заметно меньше температуры поверхности плёнки , причём на этой поверхности имеется небольшой скачок температур конденсата и пара (для воды скачок обычно порядка 0,02–0,04 К). Температура пара в объёме несколько выше температуры насыщения.
Сначала плёнка движется стабильно ламинарно – это ламинарный режим. Затем на ней появляются волны (со сравнительно большим шагом, пробегающие по плёнке и собирающие накапливающийся конденсат, так как в более толстом слое в волне скорость движения больше, и такой режим стекания энергетически выгоднее установившегося). Это ламинарно-волновой режим. Далее при большом количестве конденсата режим может стать турбулентным.
На вертикальных трубах картина аналогична случаю вертикальной стенки.
На горизонтальной трубе теплоотдача конденсации выше, чем на вертикальной (из-за меньшей в среднем толщины плёнки). При движущемся паре теплоотдача растёт, особенно при сдуве плёнки.
В случае пучков труб (в частности, в конденсаторах) имеют место особенности:
1) Скорости пара по мере прохождения по пучку уменьшаются вследствие его конденсации.
2) В горизонтальных пучках конденсат стекает с трубы на трубу, с одной стороны, увеличивая толщину плёнки на нижних трубах, что уменьшает теплоотдачу, с другой стороны, падение капель конденсата возмущает плёнку на нижних трубах, увеличивая теплоотдачу.
Интенсификация теплообмена в конденсаторах
Основной путь интенсификации – уменьшать толщину плёнки, удаляя её с поверхности теплообмена. С этой целью на вертикальных трубах устанавливают конденсатоотводные колпачки или закрученные рёбра. Например, колпачки, установленные с шагом 10 см, увеличивают теплообмен в 2÷3 раза. На горизонтальных трубах ставят невысокие рёбра, по которым конденсат быстро стекает. Эффективна подача пара тонкими струйками, разрушающими плёнку (теплообмен увеличивается в 3÷10 раз).
Влияние примеси газов на конденсацию
При содержании в паре даже небольшой примеси неконденсирующихся газов теплоотдача резко уменьшается, так как газ остаётся у стенки после конденсации пара и, накапливаясь, препятствует продвижению пара к стенке. Так, при содержании в паре 1% воздуха теплоотдача снижается в 2,5 раза, 2% – более чем в 3 раза.
При движении пара это влияние много меньше, но всё равно в промышленных установках воздух приходится откачивать из конденсаторов (иначе он занимает объём аппарата). И стараются вообще исключить его присутствие в паре.
Так как конденсация – процесс, обратный к кипению, то основная расчётная формула по существу та же, что при кипении:
G=Q/γ{\displaystyle G=Q/\gamma }
где G – количество образующегося конденсата (конденсирующегося пара), кг/с;
Q – отводимый от стенки тепловой поток, Вт;
γ – теплота фазового перехода, Дж/кг.
Эта формула не учитывает теплоту охлаждения пара до температуры насыщения ts и последующего охлаждения конденсата. Их нетрудно учесть при известных температурах пара на входе и конденсата на выходе. Но, в отличие от случая кипения, здесь сложно оценить даже приближенно величину Q из-за небольшого температурного напора теплопередачи (от пара к теплоносителю, охлаждающему стенку). Формулы для различных случаев конденсации имеются в учебниках и справочниках.
Конденсация насыщенных паров[править | править код]
При наличии жидкой фазы вещества конденсация происходит при сколь угодно малых пересыщениях и очень быстро. В этом случае возникает подвижное равновесие между испаряющейся жидкостью и конденсирующимися парами. Уравнение Клапейрона — Клаузиуса определяет параметры этого равновесия — в частности, выделение тепла при конденсации и охлаждение при испарении.
Конденсация перенасыщенного пара[править | править код]
- отсутствие жидкой или твёрдой фазы того же вещества.
- отсутствие ядер конденсации — взвешенных в атмосфере твёрдых частиц или капелек жидкости, а также ионов (наиболее активные ядра конденсации).
- конденсация в атмосфере другого газа — в этом случае скорость конденсации ограничена скоростью диффузии паров из газа к поверхности жидкости.
Прибор ядерной физики — камера Вильсона — основана на явлении конденсации на ионах.
При отсутствии ядер конденсации пересыщение может достигать 800—1000 и более процентов. В этом случае конденсация начинается во флуктуациях плотности пара (точках случайного уплотнения вещества).
Конденсация ненасыщенного пара[править | править код]
Конденсация ненасыщенного пара возможна в присутствии порошкообразных или твёрдых пористых тел. Кривая (в данном случае вогнутая) поверхность изменяет равновесное давление и инициирует капиллярную конденсацию.
Конденсация в твёрдую фазу[править | править код]
Конденсация, минуя жидкую фазу, происходит через образование мелких кристалликов (десублимация). Это возможно в случае давления паров ниже давления в тройной точке при пониженной температуре.
Конденсат на окнах[править | править код]
Образование конденсата на стёклах происходит в холодное время года. Образование конденсата на окнах происходит из-за понижения температуры поверхности ниже температуры точки росы. Температура точки росы зависит от температуры и влажности воздуха в помещении. Причина образования конденсата на окнах может состоять как в чрезмерном повышении влажности внутри помещения, вызванном нарушением вентиляции, так и в невысоких теплоизолирующих свойствах стеклопакета, металлопластиковой рамы, оконной коробки, в неправильной глубине монтажа окна в однородной стене, неправильной глубине монтажа относительно слоя стенового утеплителя, в полном отсутствии, либо в некачественном утеплении оконных откосов.
Конденсация пара в трубах[править | править код]
По мере прохождения по трубе пар постепенно конденсируется и на стенках образуется плёнка конденсата. При этом расход пара G» и его скорость в связи с уменьшением массы пара уменьшаются по длине трубы, а расход конденсата G увеличивается. Основной особенностью процесса конденсации в трубах является наличие динамического взаимодействия между паровым потоком и плёнкой. На плёнку конденсата действует также сила тяжести. В итоге в зависимости от ориентации трубы в пространстве и скорости пара характер движения конденсата может быть различным. В вертикальных трубах при движении пара сверху вниз силы тяжести и динамического воздействия парового потока совпадают по направлению и плёнка конденсата стекает вниз. В коротких трубах при небольшой скорости парового потока течение плёнки в основном определяется силой тяжести аналогично случаю конденсации неподвижного пара на вертикальной стенке. Такой же оказывается и интенсивность теплоотдачи. При увеличении скорости пара интенсивность теплоотдачи растет. Это объясняется уменьшением толщины конденсатной плёнки, которая под воздействием парового потока течёт быстрее. В длинных трубах при больших скоростях движения пара картина процесса усложняется. В этих условиях наблюдаются частичный срыв жидкости с поверхности плёнки и образование парожидкостной смеси в ядре потока. При этом влияние силы тяжести постепенно утрачивается, и закономерности процесса перестают зависеть от ориентации трубы в пространстве. В горизонтальных трубах при не очень больших скоростях парового потока взаимодействие сил тяжести и трения пара о плёнку приводит к иной картине течения. Под влиянием силы тяжести плёнка конденсата стекает по внутренней поверхности трубы вниз. Здесь конденсат накапливается и образует ручей. На это движение накладывается движение конденсата в продольном направлении под воздействием парового потока. В итоге интенсивность теплоотдачи оказывается переменной по окружности трубы: в верхней части более высокая, чем в нижней. Из-за затопления нижней части сечения горизонтальной трубы конденсатом средняя интенсивность теплоотдачи при небольших скоростях пара может оказываться даже более низкой, чем при конденсации неподвижного пара снаружи горизонтальной трубы того же диаметра.
Испарение и конденсация – кратко, все самое важное
Каждое вещество может находиться в одном из трёх основных состояний — твёрдом, жидком или газообразном. При этом для каждого из этих них характерен определённый диапазон температур.
С изменением температуры выше порогового значения, начинается постепенный переход из жидкости в пар — закипание, а при понижении температурного показателя начинается противоположный процесс превращения пара в жидкость — конденсация.
Содержание статьи:
Испарение – что это такое?
Наиболее наглядно описанные выше процессы можно проследить на примере воды. Чистая вода является жидкостью при t = 0…99°С. При понижении температуры ниже нуля происходит процесс затвердевания — превращения жидкости в лёд.
При увеличении t свыше ста градусов вода закипает и испаряется. Однако парообразование может осуществляться и при гораздо меньших показателях температур. Этот процесс именуется испарением, и осуществляется он не по всему объёму жидкости, а только на её поверхности.
Данный процесс сопровождается поглощением тепла. Связано это с затратой испаряющимися частицами энергии на преодоление силы поверхностного натяжения молекул вещества. Кинетическая энергия молекулярных частиц, имеющих наибольшую скорость, становится выше потенциальной энергии сцепления с прочими соседними молекулами.
В итоге им хватает энергии на то, чтобы оторваться от поверхности и перейти в парообразное состояние. При этом внутренняя энергия оставшихся молекул становится ниже среднего значения, и температура жидкости уменьшается.
Поскольку молекулы находятся в постоянном хаотичном броуновском движении, то и испарение идёт при t, даже близкой к 0°С. Единственное различие — при возрастании температуры, процесс испарения активируется в связи с получением частицами дополнительной энергии извне. Эта внутренняя энергия трансформируется в кинетическую, и в итоге происходит отрыв молекулы от поверхности.
Как влияет движение воздуха на испарение
Помимо температуры, на скорость испарения оказывает влияние и такой фактор, как движение воздуха. Легко заметить, что на ветру лужи или выстиранное бельё сохнут намного быстрее. Дело в том, что значительная часть молекул, истратив энергию на преодоление силы поверхностного натяжения и оторвавшись от поверхности воды, более не могут находиться в парообразном состоянии.
Их кинетическая энергия, и соответственно, скорость, резко падает, и они опускаются вновь в жидкость. Дующий ветер подхватывает их и уносит в сторону. В результате жидкость лишается источника пополнения, и со временем высыхает.
Скорость испарения напрямую зависит и от площади водной поверхности. Чем более она, тем больше молекул за определённую единицу времени могут оторваться от неё и превратиться в пар. Чтобы установить это, достаточно провести небольшой опыт: взять плоское блюдце и узкую пробирку.
В оба сосуда следует налить одинаковый объём воды и оставить на определённое время. Спустя день-два можно заметить, что блюдце совершенно сухое, в то же время в пробирке ещё достаточно воды.
Конденсация
Процесс обратного агрегатного перехода называется конденсация, от латинского слова «конденсио» — «сгущение». Данный процесс начинается при определённом значении температуры или давления, а также при сочетании этих обоих показателей.
Подобное сочетание в физике именуется «критическая точка». Так, для процесса конденсации необходима определённая температура, выше которой конденсация становится невозможной. Это значение получило название «критическая температура».
В «критической точке» происходит смешение состояний пара и жидкости, границы между ними размываются и количество молекул, отрывающихся от жидкости, становится равным количеству молекул, в неё возвращающихся.
То есть, оба процесса приходят в равновесие. При понижении температуры пара ниже критической отметки, его частички начинают массово оседать на холодных поверхностях, образуя капельки жидкости. Это и является процессом конденсации, а температура, при которой он начинается, именуется «точка росы».
Конденсация в природе
Понаблюдать процесс конденсации можно наблюдать, приблизив охлаждённую стеклянную или металлическую пластинку к носику кипящего чайника.
Выходящие из чайника в виде пара молекулы воды, при встрече с холодной поверхностью пластинки остужаются, теряют свою кинетическую энергию и оседают на её поверхности в виде маленьких капелек жидкости.
Оба этих явления достаточно часто можно видеть и в природе. Утренний туман является типичным примером испарения влаги, а образование росы на траве, или инея в прохладное время — конденсация парообразных частиц.
Благодаря конденсации и испарению происходит круговорот воды в природе, когда испарившаяся вода конденсируется в виде облаков, и проливается обратно на землю в виде дождя.
Конденсация — Класс!ная физика
Конденсация
Конденсация– это переход вещества из газообразного в жидкое состояние.
Молекулы жидкости, покинувшие ее в процессе испарения, находятся в воздухе в состоянии непрерывного теплового движения. Так как движение молекул хаотичное, то какая-то часть молекул вновь попадает в жидкость.Число таких молекул тем больше, чем больше давление пара над жидкостью. Пар конденсируется.
Процесс превращения пара в жидкость идет с выделением некоторого количества тепла.
Количество теплоты, выделяющееся при конденсации определяется по формуле:
где L — удельная теплота парообразования.
Приведенная выше формула годится одновременнодля расчета количества теплоты необходимого для превращения жидкости в пар ( при кипении) и для количества теплоты, выделяющейсяпри конденсации.
Скорость конденсации зависитот: рода жидкости, наличия центров конденсации и от температуры.
Температура вещества в процессе конденсации не изменяется.
Температура конденсации паров вещества равна температуре кипения этого вещества.
ИНТЕРЕСНЫЕ ЯВЛЕНИЯ
Конденсация в банке.
Какого цвета туман?
Капиллярная конденсация.
КАК ПОЯВЛЯЮТСЯ ТУМАН И РОСА
В воздухе всегдаесть водяные пары, хотя их плотность в сотни раз меньше плотности воздуха. Количество водяных паров в воздухе не может быть бесконечно большим. Существует предельная масса воды, которая при данной температуре может содержаться в 1 куб.м воздуха. Чем выше температура воздуха, тем большее количество водяных паров может содержаться в воздухе.
При понижениитемпературы воздуха водяные пары в какой-то момент становятся насыщенными.
При дальнейшем охлаждении начинают конденсироватьсяи проявляются в виде мельчайших капель на центрахконденсации – пылинках, частицах дыма, ионах газа.
Появившиеся капли в воздухе называются туманом.
А капли на поверхности земли, на листьях и траве называют росой.
Туманы не долговечны. Капли в воздухе могут сливаться, тогда выпадает дождь, или испаряться, тогда туман рассеивается.
ЗНАЕШЬ ЛИ ТЫ
… что, белый след на небе от летящего самолета – туман, образующийся из паров воды, поставщиком которых служит сгорающее топливо. Горячий выхлопной газ, насыщенный водяными парами, попадает в холодную атмосферу и образует туман.
ИНТЕРЕСНО
Если на газовой плите с предельно большим пламенем горелки стоит открытая кастрюля с водой, близкой к кипению, то как только выключить газ, над кастрюлей появляетсяобильный пар. Оказывается, что при работе горелки конденсация пара происходила на большом расстоянии от кастрюли, конденсат уносился конвекционными потоками воздуха, поэтому сконденсированные частицы пара не были видны. Когда горелку выключили, пар стал конденсироваться над кастрюлей и поэтому стал видимым.
Почему холодильник время от времени приходится выключать и размораживать. Большинство продуктов содержит воду. Испаряясь, она затем замерзает на самой холодной части холодильника — испарителе, и он покрывается толстой снеговой шубой, обладающей низкой теплопроводностью. Это приводит к уменьшению теплоотвода из камеры, и температура в холодильнике понижается недостаточно.
А НУ-КА
Почему стакан с холодной водой покрывается снаружи каплями воды, когда его приносим в теплую комнату?
Почему эти капли через некоторое время исчезают?
Испарение, конденсация, кипение. Насыщенные и ненасыщенные пары
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. Переход из одного состояния в другое называется фазовым переходом. Испарение и конденсация являются примерами фазовых переходов.
Все реальные газы (кислород, азот, водород и т. д.) при определенных условиях способны превращаться в жидкость. Однако такое превращение может происходить только при температурах ниже определенной, так называемой критической температуры Tкр. Например, для воды критическая температура равна 647,3 К, для азота 126 К, для кислорода 154,3 К. При комнатной температуре (≈ 300 К) вода может находиться и в жидком, и в газообразном состояниях, а азот и кислород существуют только в виде газов.
Испарением называется фазовый переход из жидкого состояния в газообразное. С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости (если нет подвода энергии от окружающих тел).
Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
 |
Модель. Испарение и конденсация. |
В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т. е. когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным.
Число молекул, вылетающих с единицы площади поверхности жидкости за одну секунду, зависит от температуры жидкости. Число молекул, возвращающихся из пара в жидкость, зависит от концентрации молекул пара и от средней скорости их теплового движения, которая определяется температурой пара. Отсюда следует, что для данного вещества концентрация молекул пара при равновесии жидкости и ее пара определяется их равновесной температурой. Установление динамического равновесия между процессами испарения и конденсации при повышении температуры происходит при более высоких концентрациях молекул пара. Так как давление газа (пара) определяется его концентрацией и температурой, то можно сделать вывод: давление насыщенного пара p0 данного вещества зависит только от его температуры и не зависит от объема. Поэтому изотермы реальных газов на плоскости (p, V) содержат горизонтальные участки, соответствующие двухфазной системе (рис. 3.4.1).
|
Рисунок 3.4.1. Изотермы реального газа. Область I – жидкость, область II – двухфазная система «жидкость + насыщенный пар», область III – газообразное вещество. K – критическая точка |
При повышении температуры давление насыщенного пара и его плотность возрастают, а плотность жидкости уменьшается из-за теплового расширения. При температуре, равной критической температуре Tкр для данного вещества, плотности пара и жидкости становятся одинаковыми. При T > Tкр исчезают физические различия между жидкостью и ее насыщенным паром.
Если изотермически сжимать ненасыщенный пар при T < Tкр, то его давление будет возрастать, пока не станет равным давлению насыщенного пара. При дальнейшем уменьшении объема на дне сосуда образуется жидкость и устанавливается динамическое равновесие между жидкостью и ее насыщенным паром. С уменьшением объема все большая часть пара конденсируется, а его давление остается неизменным (горизонтальный участок на изотерме). Когда весь пар превращается в жидкость, давление резко возрастает при дальнейшем уменьшении объема вследствие малой сжимаемости жидкости.
Из газообразного состояния в жидкое можно перейти, минуя двухфазную область. Для этого нужно совершить процесс в обход критической точки K. Один из возможных процессов такого рода показан на рис. 3.4.1 ломаной линией ABC.
 |
Модель. Изотермы реального газа. |
В атмосферном воздухе всегда присутствуют пары воды при некотором парциальном давлении p, которое, как правило, меньше давления насыщенного пара p0. Отношение p / p0, выраженное в процентах, называется относительной влажностью воздуха.
|
Ненасыщенный пар можно теоретически описывать с помощью уравнения состояния идеального газа при обычных для реальных газов ограничениях: давление пара должно быть не слишком велико (практически p ≤ (106–107) Па), а его температура выше некоторого определенного для каждого вещества значения. К насыщенному пару также можно приближенно применять законы идеального газа при условии, что для каждой температуры T давление p0 насыщенного пара определяется по кривой равновесия p0(T) для данного вещества.
Давление p0 насыщенного пара очень быстро возрастает с ростом температуры T. Зависимость p0 (T) нельзя получить из законов идеального газа. Давление газа при постоянной концентрации молекул растет прямо пропорционально температуре. В насыщенном паре при повышении температуры возрастает не только средняя кинетическая энергия движения молекул, но и их концентрация. Поэтому давление насыщенного пара при повышении температуры возрастает быстрее, чем давление идеального газа при постоянной концентрации молекул.
Испарение может происходить не только с поверхности, но и в объеме жидкости. В жидкости всегда имеются мельчайшие пузырьки газа. Если давление насыщенного пара жидкости равно внешнему давлению (т. е. давлению газа в пузырьках) или превышает его, жидкость будет испаряться внутрь пузырьков. Пузырьки, наполненные паром, расширяются и всплывают на поверхность. Этот процесс называется кипением. Таким образом, кипение жидкости начинается при такой температуре, при которой давление ее насыщенных паров становится равным внешнему давлению.
В частности, при нормальном атмосферном давлении вода кипит при температуре 100 °С. Это значит, что при такой температуре давление насыщенных паров воды равно 1 атм. При подъеме в горы атмосферное давление уменьшается, и поэтому температура кипения воды понижается (приблизительно на 1 °С на каждые 300 метров высоты). На высоте 7 км давление составляет примерно 0,4 атм, и температура кипения понижается до 70 °С.
В герметически закрытом сосуде жидкость кипеть не может, т. к. при каждом значении температуры устанавливается равновесие между жидкостью и ее насыщенным паром. По кривой равновесия p0 (T) можно определять температуру кипения жидкости при различных давлениях.
Изображенная на рис. 3.4.1 картина изотерм реального газа описывает процессы испарения и конденсации, т. е. фазовый переход между газообразной и жидкой фазами вещества. На самом деле эта картина является неполной, т. к. из газообразного и жидкого любое вещество может перейти в твердое состояние. При заданной температуре T термодинамическое равновесие между двумя фазами одного и того же вещества возможно лишь при определенном значении давления в системе. Зависимость равновесного давления от температуры называется кривой фазового равновесия. Примером может служить кривая равновесия p0 (T) насыщенного пара и жидкости. Если кривые равновесия между различными фазами данного вещества построить на плоскости (p, T), то они разбивают эту плоскость на отдельные области, в которых вещество существует в однородном агрегатном состоянии – твердом, жидком или газообразном (рис. 3.4.2). Изображенные в координатной системе (p, T) кривые равновесия называются фазовой диаграммой.
|
Рисунок 3.4.2. Типичная фазовая диаграмма вещества. K – критическая точка, T – тройная точка. Область I – твердое тело, область II – жидкость, область III – газообразное вещество |
Кривая 0T, соответствующая равновесию между твердой и газообразной фазами, называется кривой сублимации. Кривая TK равновесия между жидкостью и паром называется кривой испарения, она обрывается в критической точке K. Кривая TM равновесия между твердым телом и жидкостью называется кривой плавления.
Кривые равновесия сходятся в точке T, в которой могут сосуществовать в равновесии все три фазы. Эта точка называется тройной точкой.
Для многих веществ давление pтр в тройной точке меньше 1 атм ≈ 105 Па. Такие вещества при нагревании при атмосферном давлении плавятся. Например, тройная точка воды имеет координаты Tтр = 273,16 К, pтр = 6,02·102 Па и используется в качестве опорной для калибровки абсолютной температурной шкалы Кельвина. Существуют, однако, и такие вещества, у которых pтр превышает 1 атм. Так для углекислоты (CO2) давление pтр = 5,11 атм и температура Tтр = 216,5 К. Поэтому при атмосферном давлении твердая углекислота может существовать только при низкой температуре, а в жидком состоянии при p = 1 атм она вообще не существует. В твердом состоянии в равновесии со своим паром при атмосферном давлении углекислота находится при температуре 173 К или –80 °С. Это широко применяемый «сухой лед», который никогда не плавится, а только испаряется (сублимирует).
Конспект «Испарение. Конденсация» — УчительPRO
«Испарение. Конденсация»
Явление превращения вещества из жидкого состояния в газообразное называется парообразованием. Парообразование может осуществляться в виде двух процессов: испарение и кипение.
Испарение
Испарение происходит с поверхности жидкости при любой температуре. Так, лужи высыхают и при 10 °С, и при 20 °С, и при 30 °С. Таким образом, испарением называется процесс превращения вещества из жидкого состояния в газообразное, происходящий с поверхности жидкости при любой температуре.
С точки зрения молекулярно-кинетической теории строения вещества испарение жидкости объясняется следующим образом. Молекулы жидкости, участвуя в непрерывном движении, имеют разные скорости. Наиболее быстрые молекулы, находящиеся на границе поверхности воды и воздуха и имеющие сравнительно большую энергию, преодолевают притяжение соседних молекул и покидают жидкость. Таким образом, над жидкостью образуется пар.
Поскольку из жидкости при испарении вылетают молекулы, обладающие большей внутренней энергией по сравнению с энергией молекул, остающихся в жидкости, то средняя скорость и средняя кинетическая энергия молекул жидкости уменьшаются и, следовательно, температура жидкости уменьшается.
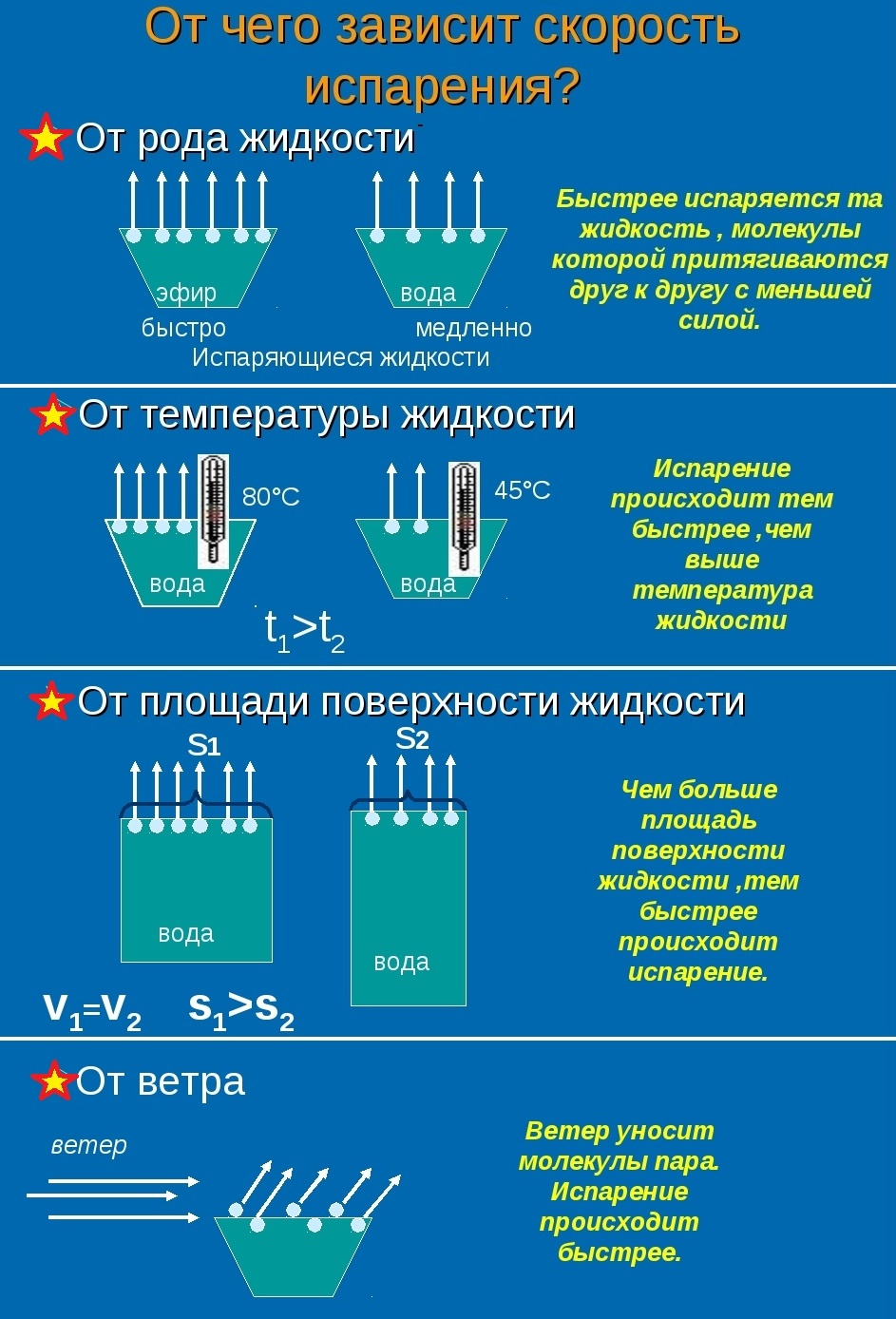
Скорость испарения жидкости зависит от рода жидкости. Так, скорость испарения эфира больше, чем скорость испарения воды и растительного масла. Кроме того, скорость испарения зависит от движения воздуха над поверхностью жидкости. Доказательством может служить то, что бельё сохнет быстрее на ветру, чем в безветренном месте при тех же внешних условиях.
Скорость испарения зависит от температуры жидкости. Например, вода при температуре 30 °С испаряется быстрее, чем вода при 10 °С.
Хорошо известно, что вода, налитая в блюдце, испариться быстрее, чем вода такой же массы, налитая в стакан. Следовательно, скорость испарения зависит от площади поверхности жидкости.
Конденсация
Процесс превращения вещества из газообразного состояния в жидкое называется конденсацией.
Процесс конденсации происходит одновременно с процессом испарения. Молекулы, вылетевшие из жидкости и находящиеся над её поверхностью, участвуют в хаотическом движении. Они сталкиваются с другими молекулами, и в какой-то момент времени их скорости могут быть направлены к поверхности жидкости, и молекулы вернутся в неё.
Если сосуд открыт, то процесс испарения происходит быстрее, чем конденсация, и масса жидкости в сосуде уменьшается. Пар, образующийся над жидкостью, называется ненасыщенным.
Если жидкость находится в закрытом сосуде, то вначале число молекул, вылетающих из жидкости, будет больше, чем число молекул, возвращающихся в неё, но с течением времени плотность пара над жидкостью возрастет настолько, что число молекул, покидающих жидкость, станет равным числу молекул, возвращающихся в неё. В этом случае наступает динамическое равновесие жидкости с её паром.
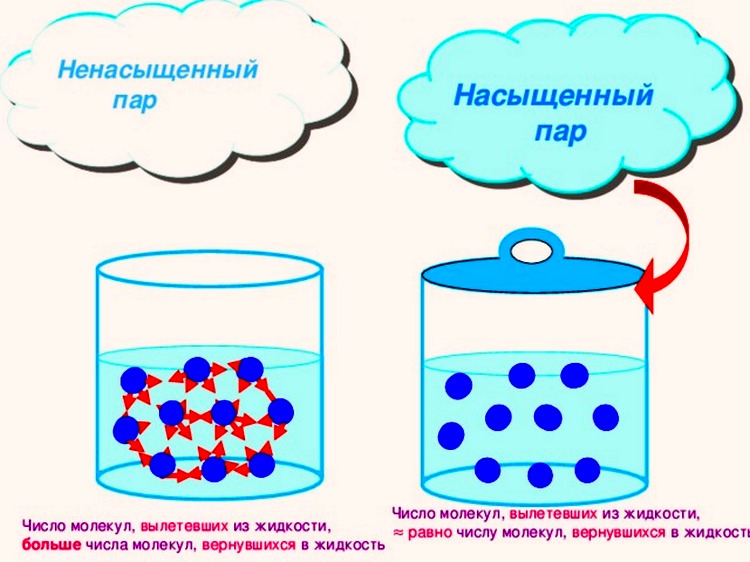
Пар, находящийся в состоянии динамического равновесия со своей жидкостью, называется насыщенным паром.
Если сосуд с жидкостью, в котором находится насыщенный пар, нагреть, то вначале число молекул, вылетающих из жидкости, увеличится и будет больше, чем число молекул, возвращающихся в неё. С течением времени равновесие восстановится, но плотность пара над жидкостью и соответственно его давление увеличатся.
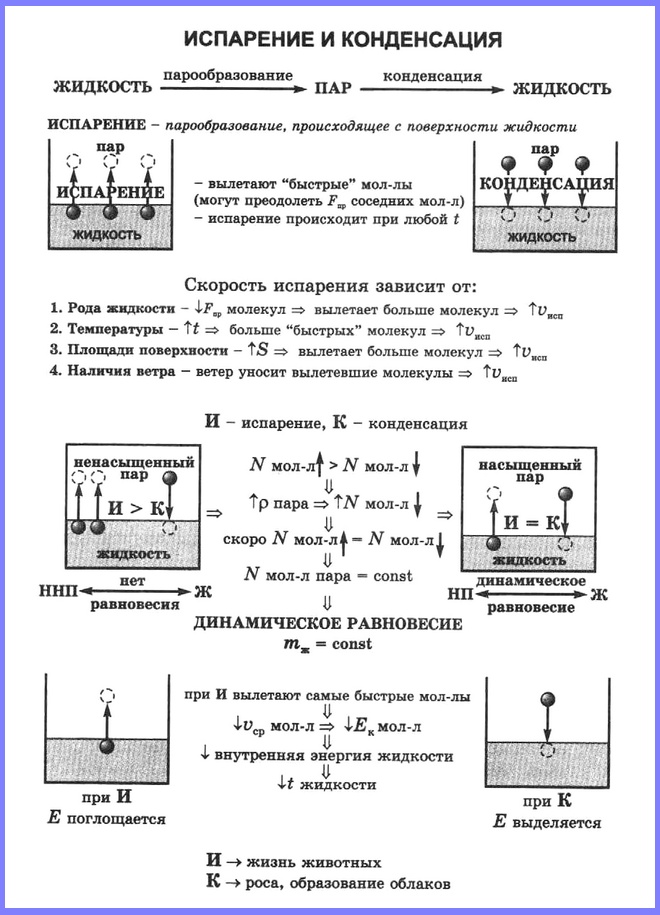
Конспект урока по физике в 8 классе «Испарение. Конденсация».
Следующая тема: «Кипение. Удельная теплота парообразования».
Испарение. Поглощение энергии при испарении жидкости и выделение ее при конденсации пара
Тема: Агрегатные состояния вещества
Урок: Испарение. Поглощение энергии при испарении жидкости и выделение её при конденсации пара
На этом уроке мы рассмотрим вопрос, связанный с испарением, а также с поглощением энергии при испарении жидкости и с выделением энергии при конденсации пара.
На предыдущих уроках мы рассматривали различные процессы и, в частности, говорили о плавлении, о нагревании тел, об отвердевании или кристаллизации тел.
Сегодня мы рассмотрим процессы, при которых образуется пар (разновидность газа) или газ.
Давайте вспомним схему, по которой происходят различные процессы превращения агрегатных состояний (Рис. 1).

Рис. 1.
Парообразование может происходить двумя способами: кипение и испарение. Как правило, указывают первый способ – кипение.
На сегодняшнем уроке мы подробно рассмотрим второй способ парообразования: испарение.
Определение
Испарение – это превращение или переход жидкости в газ (пар) со свободной поверхности жидкости. То есть тогда, когда поверхность жидкости открыта и с поверхности начинается переход вещества из жидкого состояния в газообразное.
Вспомним, для начала, схему, на которой представлена картина превращений одного состояния вещества в другое состояние.
| Конденсация | 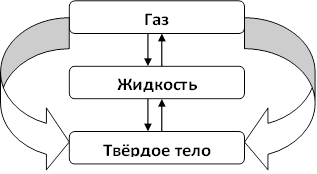 |
Парообразование |
| Десублимация | Сублимация | |
| Отвердевание | Плавление |
Таблица, в которой описаны названия процессов переходов между агрегатными состояниями вещества, выглядит следующим образом:
|
Переход |
Название |
|
Твёрдое |
Плавление |
|
Жидкое |
Отвердевание (кристаллизация) |
|
Жидкое |
Парообразование |
|
Газообразное |
Конденсация |
|
Твёрдое |
Сублимация |
|
Газообразное |
Десублимация |
Процесс испарения происходит не мгновенно, поэтому мы говорим, что испарение – процесс непрерывный и, соответственно, испарение жидкости происходит в течение некоторого времени.
Как происходит испарение?
Рассмотрим поверхность жидкости. Мы знаем, что жидкость состоит из атомов и молекул, которые находятся в непрерывном движении. Соответственно, может найтись такая частица данного вещества, у которой скорость (а, соответственно, и энергия) будет достаточно велика для того, чтобы преодолеть притяжение своих соседей и покинуть жидкость, то есть перейти в газообразное состояние. Поэтому говорят, что испарение происходит со свободной поверхности.
Рассмотрим факторы, которые влияют на испарение (в частности, его скорость).
1. Строение вещества
В первую очередь испарение связано со строением самого вещества. Можно привести следующий пример: возьмём две бумажные салфетки, смочим одну салфетку водой, а другую – эфиром. Можно заметить, что та салфетка, которая смочена эфиром, высохнет гораздо быстрее. Это объясняется тем, что сила взаимодействия между молекулами эфира гораздо меньше, чем сила взаимодействия между молекулами воды. И поэтому испарение происходит у эфира быстрее.
2. Площадь поверхности
Площадь свободной поверхности жидкости играет очень важную роль: если площадь поверхности достаточно большая, то количество частиц, покидающих жидкость, будет, конечно же, больше, и в этом случае испарение будет происходить быстрее. Можно привести такой пример: если в блюдце налить воду и такое же количество воды налить в стакан, то из блюдца испарение будет происходить гораздо быстрее (Рис. 2). Другой пример: все знают, что бельё, перед тем как его повесить сушиться, встряхивают и расправляют. В этом случае площадь белья увеличивается, соответственно, площадь испарения также увеличивается, и сам процесс испарения происходит быстрее.


Рис. 2. Блюдце и стакан с водой (Источник) (Источник)
3. Температура
Ещё одно явление, которое влияет на испарение, – это изменение температуры. Чем температура выше, тем быстрее происходит испарение. То есть, нагревая тело, мы можем увеличивать скорость процесса испарения, ускорять его, или, наоборот, если мы будем понижать температуру, то процесс испарения будет замедляться. Объясняется это тем, что с увеличением температуры возрастает скорость движения частиц. А раз скорость движения возрастает, то большее количество частиц может покинуть жидкость и перейти в газообразное состояние.
Поскольку движение частиц происходит непрерывно, то процесс испарения также непрерывен. Поскольку при любой температуре движение частиц не прекращается, то и испарение может происходить практически при любой температуре. Поэтому испарение происходит даже при низкой температуре. Например, лужи на улице высыхают не только летом, когда жарко, но и осенью, когда холодно (Рис. 3). Отличается лишь скорость высыхания луж.

Рис. 3. (Источник)
Возникает вопрос: что можно сказать об энергии жидкости при испарении? Так как жидкость покидают наиболее быстрые частицы, то они обладают большей кинетической энергией. Следовательно, в целом энергия испаряющейся жидкости уменьшается. Пояснить это можно на следующем примере: возьмём несколько человек, построим их в ряд и измерим их средний рост. Затем из этого строя уберём самых высоких и снова измерим средний рост. В результате, вполне логично, получится меньшее значение. То же самое происходит и с энергией. Каждый раз частицы с наибольшей энергией уходят из жидкости, и внутренняя энергия жидкости уменьшается.
Однако в жизни это охлаждение мы замечаем крайне редко. С чем же это связано? Это происходит из-за того, что жидкость сообщается с окружающими телами, в первую очередь, конечно, с воздухом, и поэтому, охлаждаясь, одновременно получает энергию из окружающих тел, то есть из воздуха. В результате этого «теплообмена» температура поддерживается на одном уровне. А испарение происходит с приблизительно одинаковой интенсивностью.
4. Ветер
Следующий фактор, который влияет на испарение, – это наличие ветра. Представьте себе, что над поверхностью жидкости образуется газ. Процесс испарения, как мы выяснили, продолжается непрерывно. Но точно так же будет происходить процесс возвращения молекул обратно в жидкость. Если же дует ветер, то он уносит молекулы, которые перешли из жидкости в газ, и не даёт им вернуться обратно в жидкость. В этом случае процесс испарения ускоряется, то есть скорость испарения возрастает.
Очень важно заметить и то, что в быту часто встречается так называемое испарение в закрытых сосудах. К примеру, если взять кастрюлю, в которой находится вода, то на поверхности крышки с внутренней стороны образуются капельки воды. То есть, поскольку внутри кастрюли ветра нет, то процесс испарения и возвращения молекул обратно в жидкость в данном случае выравнивается. Вот такое состояние называют динамическим равновесием.
Определение
Динамическое равновесие – это состояние системы «пар – жидкость», при которой количество молекул, вышедших из жидкости (перешедших в пар), равно количеству молекул, которое вернулось из пара обратно в жидкость.
Если же преобладает испарение над возвращением частиц обратно в жидкость, то такой пар, который находится над жидкостью, называется ненасыщенным.
Пар, находящийся в динамическом равновесии со своей жидкостью, называют насыщенным.
При динамическом равновесии общая масса системы «пар – жидкость» не меняется: количество молекул, которые «вылетели» с поверхности жидкости, равно количеству молекул, которые «вернулись». Поэтому в целом масса всей системы «пар – жидкость» не изменяется.
Кроме испарения существует и обратный ему процесс, который называется конденсацией (от латинского – «сгущаю»).
То есть, конденсация – это процесс перехода пара (газа) в жидкость. Этот процесс происходит всегда с выделением количества теплоты (так как внутренняя энергия вещества уменьшается). То есть температура окружающих тел будет повышаться (жидкость передаёт избыточную энергию окружающим телам).
Конденсация происходит так же непрерывно, как и испарение. Точнее, можно сказать, что эти два процесса происходят одновременно, непрерывно.
Подтверждением этого, например, является образование облаков, ведь облака – это сконденсированная жидкость. Выпадение росы или, например, дождь, который идёт, – это всё процессы, которые связаны с конденсацией.
Отметим, что существует испарение не только с поверхности жидкостей, но и твёрдых тел. Для этого существует наглядный пример: если зимой мокрое бельё повесить на улице, то оно замёрзнет, то есть покроется коркой льда. Но, через некоторое время выяснится, что бельё сухое, то есть вода, даже в твёрдом состоянии, куда-то исчезла. Это и есть процесс испарения твёрдого тела, в данном случае льда. Встречаются испарения и других веществ, например, нафталина. Запах нафталина, который мы чувствуем, говорит о том, что нафталин также способен к испарению.
На следующем уроке мы рассмотрим вопросы, связанные с другим процессом перехода из жидкого состояния в газообразное – парообразованием.
Список литературы
- Генденштейн Л. Э, Кайдалов А. Б., Кожевников В. Б. Физика 8 / Под ред. Орлова В. А., Ройзена И. И. – М.: Мнемозина.
- Перышкин А. В. Физика 8. – М.: Дрофа, 2010.
- Фадеева А. А., Засов А. В., Киселев Д. Ф. Физика 8. – М.: Просвещение.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Фестиваль педагогических идей «Открытый урок» (Источник).
- Сайт учителя информатики (Источник).
- Продленка (Источник).
Домашнее задание
- П. 16, вопросы 1–8, упр. 9 (1–7). Перышкин А. В. Физика 8. – М.: Дрофа, 2010.
- При какой температуре происходит испарение воды?
- Почему мокрое бельё на ветру сохнет быстрее?
- Почему жидкость при испарении охлаждается?
Конденсация — это… Что такое Конденсация?
 Роса на паутине
Роса на паутине  Конденсация на бутылке холодной воды
Конденсация на бутылке холодной воды  Конденсация водяного пара в воздухе над чашкой горячей воды
Конденсация водяного пара в воздухе над чашкой горячей водыКонденса́ция паров (лат. condense — уплотняю, сгущаю) — переход вещества в жидкое или твёрдое состояние из газообразного. Максимальная температура, ниже которой происходит конденсация, называется критической. Пар, из которого может происходить конденсация, бывает насыщенным или ненасыщенным.
Виды конденсации
Соотношения для разных видов конденсации выведены на основе опытных данных, а также статистической физики и термодинамики.
Конденсация насыщенных паров
При наличии жидкой фазы вещества конденсация происходит при сколь угодно малых пересыщениях и очень быстро. В этом случае возникает подвижное равновесие между испаряющейся жидкостью и конденсирующимися парами. Уравнение Клапейрона — Клаузиуса определяет параметры этого равновесия — в частности, выделение тепла при конденсации и охлаждение при испарении.
Конденсация перенасыщенного пара
Наличие перенасыщенного пара возможно в следующих случаях:
- отсутствие жидкой или твёрдой фазы того же вещества.
- отсутствие ядер конденсации — взвешенных в атмосфере твёрдых частиц или капелек жидкости, а также ионов (наиболее активные ядра конденсации).
- конденсация в атмосфере другого газа — в этом случае скорость конденсации ограничена скоростью диффузии паров из газа к поверхности жидкости.
Прибор ядерной физики — камера Вильсона — основана на явлении конденсации на ионах.
При отсутствии ядер конденсации пересыщение может достигать 800—1000 и более процентов. В этом случае конденсация начинается во флуктуациях плотности пара (точках случайного уплотнения вещества).
Конденсация ненасыщенного пара
Конденсация ненасыщенного пара возможна в присухность изменяет равновесное давление и инициирует капиллярную конденсацию.
Конденсация в твёрдую фазу
Конденсация, минуя жидкую фазу, происходит через образование мелких кристалликов (десублимация). Это возможно в случае давления паров ниже давления в тройной точке при пониженной температуре.
Конденсат на окнах
Образование конденсата на стеклах, происходит в холодное время года — либо зимой, либо поздней осенью. С точки зрения физики, образование конденсата на окнах происходит из-за разницы температур соприкасающихся поверхностей, особенно в местах стыка рамы и самого стекла. Чем больше эта разница, тем большее количество влаги оседает на единице поверхности за единицу времени. Если разница температур превышает 55-60°, то осевший конденсат может превратиться в тонкую корочку льда или инея. Причина образования конденсата на стекле состоит в замедленном циркулировании воздуха в помещении, а также в чрезмерной влажности.







 жидкое
жидкое