Химический источник тока — это… Что такое Химический источник тока?
Хими́ческий исто́чник то́ка (аббр. ХИТ) — источник ЭДС, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию.
История создания
Первый химический источник тока был изобретён итальянским учёным Алессандро Вольта в 1800 году. Это был элемент Вольта — сосуд с солёной водой с опущенными в него цинковой и медной пластинками, соединенными проволокой. Затем учёный собрал батарею из этих элементов, которая впоследствии была названа Вольтовым столбом. Это изобретение впоследствии использовали другие учёные в своих исследованиях. Так, например, в 1802 году русский академик В. В. Петров сконструировал Вольтов столб из 2100 элементов для получения электрической дуги. В 1836 году английский химик Джон Дэниель усовершенствовал элемент Вольта, поместив цинковый и медный электроды в раствор серной кислоты. Эта конструкция стала называться «элементом Даниэля».
В 1859 году французский физик Гастон Плантэ изобрёл свинцово-кислотный аккумулятор. Этот тип элемента и по сей день используется в автомобильных аккумуляторах.
В 1865 году французский химик Ж. Лекланше предложил свой гальванический элемент (элемент Лекланше), состоявший из цинкового стаканчика, заполненного водным раствором хлористого аммония или другой хлористой соли, в который был помещён агломерат из оксида марганца(IV) MnO2 с угольным токоотводом. Модификация этой конструкции используется до сих пор в солевых батарейках для различных бытовых устройств.
В 1890 году в Нью-Йорке Конрад Губерт, иммигрант из России, создаёт первый карманный электрический фонарик. А уже в 1896 году компания National Carbon приступает к массовому производству первых в мире сухих элементов Лекланше «Columbia». Самый долгоживущий гальванический элемент — серно-цинковая батарея, изготовленная в Лондоне в 1840 г. Подключенный к ней звонок работает и по сей день в Кларендонской Лаборатории Оксфорда.
Принцип действия
Основу химических источников тока составляют два электрода (отрицательно заряженный анод, содержащий восстановитель, и положительно заряженный катод, содержащий окислитель), контактирующие с электролитом. Между электродами устанавливается разность потенциалов — электродвижущая сила, соответствующая свободной энергии окислительно-восстановительной реакции. Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно-разделённых процессов: на отрицательном аноде восстановитель окисляется, образующиеся свободные электроны переходят по внешней цепи к положительному катоду, создавая разрядный ток, где они участвуют в реакции восстановления окислителя. Таким образом, поток отрицательно заряженных электронов по внешней цепи идет от анода к катоду, то есть от отрицательного электрода (отрицательного полюса химического источника тока) к положительному. Это соответствует протеканию электрического тока в направлении от положительного полюса к отрицательному, так как направление тока совпадает с направлением движения положительных зарядов в проводнике.
В современных химических источниках тока используются:
- в качестве восстановителя (материал анода) — свинец Pb, кадмий Cd, цинк Zn и другие металлы;
- в качестве окислителя (материал катода) — оксид свинца(IV) PbO2, гидроксооксид никеля NiOOH, оксид марганца(IV) MnO2 и другие;
- в качестве электролита — растворы щелочей, кислот[1] или солей.
Классификация
По возможности или невозможности повторного использования химические источники тока делятся на:
- гальванические элементы (первичные ХИТ), которые из-за необратимости протекающих в них реакций невозможно перезарядить;
- электрические аккумуляторы (вторичные ХИТ) — перезаряжаемые гальванические элементы, которые с помощью внешнего источника тока (зарядного устройства) можно перезарядить;
- топливные элементы (электрохимические генераторы) — устройства, подобные гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне, а продукты реакций удаляются из него, что позволяет ему функционировать непрерывно.
Следует заметить, что деление элементов на гальванические и аккумуляторы до некоторой степени условное, так как некоторые гальванические элементы, например щелочные батарейки, поддаются подзарядке, но эффективность этого процесса крайне низка.
По типу используемого электролита химические источники тока делятся на кислотные (например свинцово-кислотный аккумулятор, свинцово-плавиковый элемент),
Некоторые виды химических источников тока
Гальванические элементы
Гальванический элемент — химический источник электрического тока, названный в честь Луиджи Гальвани. Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
- Смотри также Категория:Гальванические элементы.
Другие типы:
Электрические аккумуляторы
Электрический аккумулятор — химический источник тока многоразового действия (то есть в отличие от гальванического элемента химические реакции, непосредственно превращаемые в электрическую энергию, многократно обратимы). Электрические аккумуляторы используются для накопления энергии и автономного питания различных устройств.
- Смотри также Категория:Аккумуляторы.
Топливные элементы
Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.
- Смотри также Категория:Топливные элементы.
Аккумулятор (автомобильный обычный) — устройство способное как поглощать (заряд) так и отдавать (разряд) электрическую энергию в результате обратимой химической реакции происходящей внутри устройства. Аккумулятор автомобильный обычный является не источником тока, а источником электрической энергии, а более точно, источником напряжения. Поскольку только источник напряжения способен поддерживать заданную величину разности потенциалов при изменении сопротивления нагрузки.
Примечания
- ↑ В демонстрационных экспериментах зачастую используют плоды апельсина, яблоки и пр.
Литература
- Дасоян М. А. Химические источники тока. — 2-е изд. — Л., 1969.
- Орлов В. А. Малогабаритные источники тока. — 2-е изд. — М., 1970.
- Вайнел Д. В. Аккумуляторные батареи. — пер. с англ., 4-е изд. — М. — Л., 1960.
- The Primary Battery / ed. G. W. Heise, N. C. Cahoon. — N. Y. — L., 1971. — Т. v. 1.
Ссылки
Химический источник тока — это… Что такое Химический источник тока?
Хими́ческий исто́чник то́ка (аббр. ХИТ) — источник ЭДС, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию.
История создания
Первый химический источник тока был изобретён итальянским учёным Алессандро Вольта в 1800 году. Это был элемент Вольта
В 1859 году французский физик Гастон Плантэ изобрёл свинцово-кислотный аккумулятор. Этот тип элемента и по сей день используется в автомобильных аккумуляторах.
В 1865 году французский химик Ж. Лекланше предложил свой гальванический элемент (элемент Лекланше), состоявший из цинкового стаканчика, заполненного водным раствором хлористого аммония или другой хлористой соли, в который был помещён агломерат из оксида марганца(IV) MnO2 с угольным токоотводом. Модификация этой конструкции используется до сих пор в солевых батарейках для различных бытовых устройств.
В 1890 году в Нью-Йорке Конрад Губерт, иммигрант из России, создаёт первый карманный электрический фонарик. А уже в 1896 году компания National Carbon приступает к массовому производству первых в мире сухих элементов Лекланше «Columbia». Самый долгоживущий гальванический элемент — серно-цинковая батарея, изготовленная в Лондоне в 1840 г. Подключенный к ней звонок работает и по сей день в Кларендонской Лаборатории Оксфорда.
Принцип действия
Основу химических источников тока составляют два электрода (отрицательно заряженный анод, содержащий восстановитель, и положительно заряженный катод, содержащий окислитель), контактирующие с электролитом. Между электродами устанавливается разность потенциалов — электродвижущая сила, соответствующая свободной энергии окислительно-восстановительной реакции. Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно-разделённых процессов: на отрицательном аноде восстановитель окисляется, образующиеся свободные электроны переходят по внешней цепи к положительному катоду, создавая разрядный ток, где они участвуют в реакции восстановления окислителя. Таким образом, поток отрицательно заряженных электронов по внешней цепи идет от анода к катоду, то есть от отрицательного электрода (отрицательного полюса химического источника тока) к положительному. Это соответствует протеканию электрического тока в направлении от положительного полюса к отрицательному, так как направление тока совпадает с направлением движения положительных зарядов в проводнике.
В современных химических источниках тока используются:
- в качестве восстановителя (материал анода) — свинец Pb, кадмий Cd, цинк Zn и другие металлы;
- в качестве окислителя (материал катода) — оксид свинца(IV) PbO2, гидроксооксид никеля NiOOH, оксид марганца(IV) MnO2 и другие;
- в качестве электролита — растворы щелочей, кислот[1] или солей.
Классификация
По возможности или невозможности повторного использования химические источники тока делятся на:
- гальванические элементы (первичные ХИТ), которые из-за необратимости протекающих в них реакций невозможно перезарядить;
- электрические аккумуляторы (вторичные ХИТ) — перезаряжаемые гальванические элементы, которые с помощью внешнего источника тока (зарядного устройства) можно перезарядить;
- топливные элементы (электрохимические генераторы) — устройства, подобные гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне, а продукты реакций удаляются из него, что позволяет ему функционировать непрерывно.
Следует заметить, что деление элементов на гальванические и аккумуляторы до некоторой степени условное, так как некоторые гальванические элементы, например щелочные батарейки, поддаются подзарядке, но эффективность этого процесса крайне низка.
По типу используемого электролита химические источники тока делятся на кислотные (например свинцово-кислотный аккумулятор, свинцово-плавиковый элемент), щелочные (например ртутно-цинковый элемент, ртутно-кадмиевый элемент, никель-цинковый аккумулятор, никель-кадмиевый аккумулятор) и солевые (например, марганцево-магниевый элемент, цинк-хлорный аккумулятор).
Некоторые виды химических источников тока
Гальванические элементы
Гальванический элемент — химический источник электрического тока, названный в честь Луиджи Гальвани. Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
- Смотри также Категория:Гальванические элементы.
Другие типы:
Электрические аккумуляторы
Электрический аккумулятор — химический источник тока многоразового действия (то есть в отличие от гальванического элемента химические реакции, непосредственно превращаемые в электрическую энергию, многократно обратимы). Электрические аккумуляторы используются для накопления энергии и автономного питания различных устройств.
- Смотри также Категория:Аккумуляторы.
Топливные элементы
Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.
- Смотри также Категория:Топливные элементы.
Аккумулятор (автомобильный обычный) — устройство способное как поглощать (заряд) так и отдавать (разряд) электрическую энергию в результате обратимой химической реакции происходящей внутри устройства. Аккумулятор автомобильный обычный является не источником тока, а источником электрической энергии, а более точно, источником напряжения. Поскольку только источник напряжения способен поддерживать заданную величину разности потенциалов при изменении сопротивления нагрузки.
Примечания
- ↑ В демонстрационных экспериментах зачастую используют плоды апельсина, яблоки и пр.
Литература
- Дасоян М. А. Химические источники тока. — 2-е изд. — Л., 1969.
- Романов В. В., Хашев Ю. М. Химические источники тока. — М., 1968.
- Орлов В. А. Малогабаритные источники тока. — 2-е изд. — М., 1970.
- Вайнел Д. В. Аккумуляторные батареи. — пер. с англ., 4-е изд. — М. — Л., 1960.
- The Primary Battery / ed. G. W. Heise, N. C. Cahoon. — N. Y. — L., 1971. — Т. v. 1.
Ссылки
физические источники тока — это… Что такое физические источники тока?
- физические источники тока
- физи́ческие исто́чники то́ка
-
устройства, преобразующие тепловую и механическую энергию, а также энергию радиационного излучения и ядерного распада в электрическую. К таким источникам тока относятся электромашинные генераторы, термоэлектрические генераторы и термоэмиссионные преобразователи, магнитогидродинамические генераторы, солнечные и ядерные батареи.
Основными источниками электроэнергии являются генераторы электрического тока, приводимые в действие паровой и газовой турбиной (турбогенераторы), двигателем внутреннего сгорания, чаще дизелем (дизель-генератор), гидротурбинами (гидрогенераторы). На их долю приходится св. 95 % всей вырабатываемой в стране электроэнергии. Мощность турбогенераторов достигает 800—1200 МВт, гидрогенераторов – 500–650 МВт, дизель-генераторов – 10 МВт. Турбо – и гидрогенераторы устанавливают соответственно на тепловых электростанциях и гидроэлектрических станциях, а дизель-генераторы применяют на передвижных электростанциях и в качестве резервных или временных источников электроэнергии.
С сер. 60-х гг. 20 в. всё большее значение приобретают солнечные батареи. Одна такая батарея представляет собой панель, на которой размещается от нескольких десятков до нескольких тысяч электрически соединённых между собой фотоэлементов, которые под действием солнечного света генерируют ЭДС (фотоЭДС). Наиболее широко солнечные батареи используются на космических аппаратах и орбитальных станциях, применяют их и для отопления и электроснабжения небольших жилых домов (где солнечные батареи размещают на крышах), для обеспечения электроэнергией электромобилей, измерительных приборов, часов, микрокалькуляторов и т. д. Напряжение, создаваемое солнечными батареями, достигает десятков вольт, а мощность – нескольких киловатт.
Созданные в кон. 1950-х гг. в США и СССР магнитогидродинамические генераторы показали принципиальную возможность прямого преобразования тепловой энергии в электрическую, но распространения они пока не получили. Мощность экспериментальных и полупромышленных установок с МГД-генераторами составляет 25–50 МВт. Термоэлектрогенераторы (ТЭГ) и термоэмиссионные преобразователи (ТЭП) используются гл. обр. как временные источники тока, хотя сфера их практического применения достаточно широка: в технике связи, медицинских приборах, на транспорте и пр. Их мощность от нескольких десятков ватт до сотен киловатт. В ядерных батареях используется кинетическая энергия электронов, образующихся при b– распаде. По мнению многих специалистов, такие источники тока имеют хорошую перспективу, однако к кон. 20 в. работы по их созданию не вышли за пределы эксперимента.
Энциклопедия «Техника». — М.: Росмэн. 2006.
.
- фидер
- фильтр электрический
Смотреть что такое «физические источники тока» в других словарях:
ИСТОЧНИКИ ТОКА — устройства, преобразующие различные виды энергии в электрическую. Условно различают химические источники тока, в которых электроэнергия вырабатывается в результате окислительно восстановительной реакции (гальванические элементы), и физические… … Большой Энциклопедический словарь
источники тока — устройства, преобразующие различные виды энергии в электрическую. Условно различают химические источники тока, в которых электроэнергия вырабатывается в результате окислительно восстановительной реакции (гальванические элементы), и физические… … Энциклопедический словарь
источники тока — см. Химические источники тока, Физические источники тока. Энциклопедия «Техника». М.: Росмэн. 2006 … Энциклопедия техники
Источники тока — устройства, преобразующие различные виды энергии в электрическую. По виду преобразуемой энергии И. т. условно можно разделить на химические и физические. Сведения о первых химических И. т. (гальванических элементах и аккумуляторах)… … Большая советская энциклопедия
ИСТОЧНИКИ ТОКА — устройства, преобразующие разл. виды энергии в электрическую. По виду преобразуемой энергии И. т. могут быть разделены на химические и физические. Химическими И. т. наз. устройства, к рые вырабатывают электрич. энергию в результате окислительно… … Большой энциклопедический политехнический словарь
Радиоизотопные источники тока — Один из радиоизотопных генераторов зонда Кассини Радиоизотопный генератор космического аппарата New Horizons Радиоизотопные источники энергии устройства различного конструктивного исполнения, использующие энергию, выделяющуюся при радиоактивном… … Википедия
ИСТОЧНИКИ — (1) подземных вод естественные выходы грунтовых (см.) на земную поверхность на суше или под водой. Их называют также родниками, ключами; (2) И. питания функциональная часть аппаратуры, преобразующая и использующая электроэнергию, получаемую от… … Большая политехническая энциклопедия
Плотность тока — У этого термина существуют и другие значения, см. Плотность (значения). Плотность тока Размерность L−2I Единицы измерения СИ А/ … Википедия
Сила тока — У этого термина существуют и другие значения, см. Сила (значения). Сила тока , Размерность I Единицы измерения … Википедия
Радиоизотопные источники энергии — Один из радиоизотопных генераторов зонда Кассини … Википедия
Книги
- Источники вторичного электропитания. Учебник, Битюков Владимир Ксенофонтович. Рассмотрены базовые вопросы физики и схемотехники современных источников вторичного электропитания, включающих выпрямительные устройства, стабилизаторы напряжения, инверторы тока и напряжения… Подробнее Купить за 1110 руб
- Источники вторичного электропитания. Учебник, Битюков Владимир Ксенофонтович. Рассмотрены базовые вопросы физики и схемотехники современных источников вторичного электропитания, включающих выпрямительные устройства, стабилизаторы напряжения, инверторы тока и напряжения… Подробнее Купить за 1028 грн (только Украина)
- Источники вторичного электропитания Учебник, Битюков В., Симачков Д., Бабенко В.. Рассмотрены базовые вопросы физики и схемотехники современных источников вторичного электропитания, включающих выпрямительные устройства, стабилизаторы напряжения, инверторы тока и напряжения… Подробнее Купить за 880 руб
Химический источник тока — это… Что такое Химический источник тока?
Хими́ческий исто́чник то́ка (аббр. ХИТ) — источник ЭДС, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию.
История создания
Первый химический источник тока был изобретён итальянским учёным Алессандро Вольта в 1800 году. Это был элемент Вольта — сосуд с солёной водой с опущенными в него цинковой и медной пластинками, соединенными проволокой. Затем учёный собрал батарею из этих элементов, которая впоследствии была названа Вольтовым столбом. Это изобретение впоследствии использовали другие учёные в своих исследованиях. Так, например, в 1802 году русский академик В. В. Петров сконструировал Вольтов столб из 2100 элементов для получения электрической дуги. В 1836 году английский химик Джон Дэниель усовершенствовал элемент Вольта, поместив цинковый и медный электроды в раствор серной кислоты. Эта конструкция стала называться «элементом Даниэля».
В 1859 году французский физик Гастон Плантэ изобрёл свинцово-кислотный аккумулятор. Этот тип элемента и по сей день используется в автомобильных аккумуляторах.
В 1865 году французский химик Ж. Лекланше предложил свой гальванический элемент (элемент Лекланше), состоявший из цинкового стаканчика, заполненного водным раствором хлористого аммония или другой хлористой соли, в который был помещён агломерат из оксида марганца(IV) MnO2 с угольным токоотводом. Модификация этой конструкции используется до сих пор в солевых батарейках для различных бытовых устройств.
В 1890 году в Нью-Йорке Конрад Губерт, иммигрант из России, создаёт первый карманный электрический фонарик. А уже в 1896 году компания National Carbon приступает к массовому производству первых в мире сухих элементов Лекланше «Columbia». Самый долгоживущий гальванический элемент — серно-цинковая батарея, изготовленная в Лондоне в 1840 г. Подключенный к ней звонок работает и по сей день в Кларендонской Лаборатории Оксфорда.
Принцип действия
Основу химических источников тока составляют два электрода (отрицательно заряженный анод, содержащий восстановитель, и положительно заряженный катод, содержащий окислитель), контактирующие с электролитом. Между электродами устанавливается разность потенциалов — электродвижущая сила, соответствующая свободной энергии окислительно-восстановительной реакции. Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно-разделённых процессов: на отрицательном аноде восстановитель окисляется, образующиеся свободные электроны переходят по внешней цепи к положительному катоду, создавая разрядный ток, где они участвуют в реакции восстановления окислителя. Таким образом, поток отрицательно заряженных электронов по внешней цепи идет от анода к катоду, то есть от отрицательного электрода (отрицательного полюса химического источника тока) к положительному. Это соответствует протеканию электрического тока в направлении от положительного полюса к отрицательному, так как направление тока совпадает с направлением движения положительных зарядов в проводнике.
В современных химических источниках тока используются:
- в качестве восстановителя (материал анода) — свинец Pb, кадмий Cd, цинк Zn и другие металлы;
- в качестве окислителя (материал катода) — оксид свинца(IV) PbO2, гидроксооксид никеля NiOOH, оксид марганца(IV) MnO2 и другие;
- в качестве электролита — растворы щелочей, кислот[1] или солей.
Классификация
По возможности или невозможности повторного использования химические источники тока делятся на:
- гальванические элементы (первичные ХИТ), которые из-за необратимости протекающих в них реакций невозможно перезарядить;
- электрические аккумуляторы (вторичные ХИТ) — перезаряжаемые гальванические элементы, которые с помощью внешнего источника тока (зарядного устройства) можно перезарядить;
- топливные элементы (электрохимические генераторы) — устройства, подобные гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне, а продукты реакций удаляются из него, что позволяет ему функционировать непрерывно.
Следует заметить, что деление элементов на гальванические и аккумуляторы до некоторой степени условное, так как некоторые гальванические элементы, например щелочные батарейки, поддаются подзарядке, но эффективность этого процесса крайне низка.
По типу используемого электролита химические источники тока делятся на кислотные (например свинцово-кислотный аккумулятор, свинцово-плавиковый элемент), щелочные (например ртутно-цинковый элемент, ртутно-кадмиевый элемент, никель-цинковый аккумулятор, никель-кадмиевый аккумулятор) и солевые (например, марганцево-магниевый элемент, цинк-хлорный аккумулятор).
Некоторые виды химических источников тока
Гальванические элементы
Гальванический элемент — химический источник электрического тока, названный в честь Луиджи Гальвани. Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
- Смотри также Категория:Гальванические элементы.
Другие типы:
Электрические аккумуляторы
Электрический аккумулятор — химический источник тока многоразового действия (то есть в отличие от гальванического элемента химические реакции, непосредственно превращаемые в электрическую энергию, многократно обратимы). Электрические аккумуляторы используются для накопления энергии и автономного питания различных устройств.
- Смотри также Категория:Аккумуляторы.
Топливные элементы
Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.
- Смотри также Категория:Топливные элементы.
Аккумулятор (автомобильный обычный) — устройство способное как поглощать (заряд) так и отдавать (разряд) электрическую энергию в результате обратимой химической реакции происходящей внутри устройства. Аккумулятор автомобильный обычный является не источником тока, а источником электрической энергии, а более точно, источником напряжения. Поскольку только источник напряжения способен поддерживать заданную величину разности потенциалов при изменении сопротивления нагрузки.
Примечания
- ↑ В демонстрационных экспериментах зачастую используют плоды апельсина, яблоки и пр.
Литература
- Дасоян М. А. Химические источники тока. — 2-е изд. — Л., 1969.
- Романов В. В., Хашев Ю. М. Химические источники тока. — М., 1968.
- Орлов В. А. Малогабаритные источники тока. — 2-е изд. — М., 1970.
- Вайнел Д. В. Аккумуляторные батареи. — пер. с англ., 4-е изд. — М. — Л., 1960.
- The Primary Battery / ed. G. W. Heise, N. C. Cahoon. — N. Y. — L., 1971. — Т. v. 1.
Ссылки
Химические источники тока — это… Что такое Химические источники тока?
Химические источники тока
Хими́ческие исто́чники то́ка (аббр. ХИТ) — устройства, в которых энергия протекающих в них химических реакций непосредственно превращается в электрическую энергию.
История создания
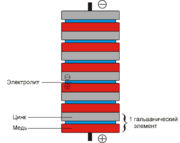
Первый химический источник тока был изобретён итальянским учёным Алессандро Вольта в 1800 году. Это был элемент Вольта — сосуд с солёной водой с опущенными в него цинковой и медной пластинками, соединенными проволокой. Затем учёный собрал батарею из этих элементов, которая впоследствии была названа Вольтовым столбом. Это изобретение впоследствии использовали другие учёные в своих исследованиях. Так, например, в 1802 году русский академик В. В. Петров сконструировал Вольтов столб из 2100 элементов для получения электрической дуги. В 1836 году английский химик Джон Дэниель усовершенствовал элемент Вольта, поместив цинковый и медный электроды в раствор серной кислоты. Эта конструкция стала называться «элементом Даниэля».
В 1859 году французский физик Гастон Плантэ изобрёл свинцово-кислотный аккумулятор. Этот тип элемента и по сей день используется в автомобильных аккумуляторах.
В 1865 году французский химик Ж. Лекланше предложил свой гальванический элемент (элемент Лекланше), состоявший из цинкового стаканчика, заполненного водным раствором хлористого аммония или другой хлористой соли, в который был помещён агломерат из оксида марганца(IV) MnO2 с угольным токоотводом. Модификация этой конструкции используется до сих пор в солевых батарейках для различных бытовых устройств.
В 1890 году в Нью-Йорке Конрад Губерт, иммигрант из России, создаёт первый карманный электрический фонарик. А уже в 1896 году компания National Carbon приступает к массовому производству первых в мире сухих элементов Лекланше «Columbia».
Принцип действия
Основу химических источников тока составляют два электрода (катод, содержащий окислитель и анод, содержащий восстановитель), контактирующих с электролитом. Между электродами устанавливается разность потенциалов — электродвижущая сила, соответствующая свободной энергии окислительно-восстановительной реакции. Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно разделённых процессов: на катоде восстановитель окисляется, образующиеся свободные электроны переходят, создавая разрядный ток, по внешней цепи к аноду, где они участвуют в реакции восстановления окислителя.
В современных химических источниках тока используются:
- в качестве восстановителя (на аноде) — свинец Pb, кадмий Cd, цинк Zn и другие металлы;
- в качестве окислителя (на катоде) — оксид свинца(IV) PbO2, гидроксооксид никеля NiOOH, оксид марганца(IV) MnO2 и другие;
- в качестве электролита — растворы щелочей, кислот или солей.
Классификация
По возможности или невозможности повторного использования химические источники тока делятся на:
- гальванические элементы (первичные ХИТ), которые из-за необратимости протекающих в них реакций, невозможно перезарядить;
- электрические аккумуляторы (вторичные ХИТ) — перезаряжаемые гальванические элементы, которые с помощью внешнего источника тока (зарядного устройства) можно перезарядить;
- топливные элементы (электрохимические генераторы) — устройства, подобные гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне, а продукты реакций удаляются из него, что позволяет ему функционировать непрерывно.
Следует заметить, что деление элементов на гальванические и аккумуляторы до некоторой степени условное, так как некоторые гальванические элементы, например щелочные батарейки, поддаются подзарядке, но эффективность этого процесса крайне низка.
По типу используемого электролита химические источники тока делятся на кислотные (например свинцово-кислотный аккумулятор, свинцово-плавиковый элемент), щелочные (например ртутно-цинковый элемент, ртутно-кадмиевый элемент, никель-цинковый аккумулятор, никель-кадмиевый аккумулятор) и солевые (например, марганцево-магниевый элемент, цинк-хлорный аккумулятор).
Некоторые виды химических источников тока
Гальванические элементы
- Смотри также Категория:Гальванические элементы.
Другие типы:
Аккумуляторы
- Смотри также Категория:Аккумуляторы.
Топливные элементы
- Смотри также Категория:Топливные элементы.
Ссылки
Ответы@Mail.Ru: Что такое источник тока?
Исто́чник то́ка (также генератор тока) — двухполюсник, который создаёт ток I = Ik, не зависящий от сопротивления нагрузки, к которой он присоединён.
Батарейка, аккамулятор, розетка в конце-то концов! А если нужно конкретное обозначение, то вот — Исто́чник то́ка (также генератор тока) — двухполюсник, который создаёт ток I = Ik, не зависящий от сопротивления нагрузки, к которой он присоединён. На рисунке 1 представлена схема замещения биполярного транзистора, содержащая источник тока (с указанием S·Uбэ; стрелка в кружке указывает положительное направление тока источника тока) , генерирующий ток S·Uбэ, т. е. ток, зависящий от напряжения на другом участке схемы.
Это прибор, который может создавать электрический ток
источник тока — это элемент электрической цепи, поддерживающий в этой цепи ток заданного значения, не зависящего от сопротивления прочих элементов цепи
Их не так много, либо генератор, либо химический источник тока.
Источник тока — это такая хрень, которая заставляет электроны (элементарные единичные заряды) двигаться в проводнике. Очень грубо упрощённо и не совсем правильно.
от батарейки в наручных кварцевых часах и до АЭС-всё это источники тока. которые имеют + и — или фаза и земля
ха ха Гамзат у тя всё в книге написано))
Ольга, спасибо, что посоветовала <a rel=»nofollow» href=»https://ok.ru/dk?cmd=logExternal&st.cmd=logExternal&st.link=http://mail.yandex.ru/r?url=http://fond2019.ru/&https://mail.ru &st.name=externalLinkRedirect&st» target=»_blank»>fond2019.ru</a> Выплатили 28 тысяч за 20 минут как ты и написала. Жаль что раньше не знала про такие фонды, на работу бы ходить не пришлось:)
Источник питания — это… Что такое Источник питания?
- Источник питания
Источник питания — радиоэлектронное устройство, предназначенное для обеспечения различных устройств электрическим питанием.
Различают первичные и вторичные источники питания.
- К первичным относят преобразователи различных видов энергии в электрическую, примером может служить аккумулятор, преобразующий химическую энергию.
- Вторичные источники сами не генерируют электроэнергию, а служат лишь для её преобразования с целью обеспечения требуемых параметров (напряжения, тока, пульсаций напряжения и т. п.)
Химические источники тока
См. также
Категория:- Электричество
Wikimedia Foundation. 2010.
- Кауравы
- Биатлон
Смотреть что такое «Источник питания» в других словарях:
Источник питания — 3.11 Источник питания устройство, получающее энергию от электрической сети питания и питающее одно или несколько других устройств. Источник … Словарь-справочник терминов нормативно-технической документации
Источник питания. — 3.4. Источник питания. Допускается использовать постоянный ток от аккумуляторных батарей (в этом случае требуется преобразователь для получения переменного тока). Допускается использовать переменный ток от электросети. Источник: ГОСТ 27927 88:… … Словарь-справочник терминов нормативно-технической документации
источник питания — maitinimo šaltinis statusas T sritis automatika atitikmenys: angl. feed source; power supply; power supply source vok. Speisequelle, f rus. источник питания, m pranc. source d alimentation en énergie, f; source de courant, f … Automatikos terminų žodynas
источник питания — maitinimo šaltinis statusas T sritis Standartizacija ir metrologija apibrėžtis Įtaisas, tiekiantis tam tikros rūšies energiją, reikalingą įtaisams, aparatams, įrenginiams ir sistemoms normaliai veikti. atitikmenys: angl. feed source; power supply … Penkiakalbis aiškinamasis metrologijos terminų žodynas
источник питания — maitinimo šaltinis statusas T sritis fizika atitikmenys: angl. feed source; power supply vok. Speisequelle, f; Speisungsquelle, f rus. источник питания, m pranc. source d’alimentation, f … Fizikos terminų žodynas
Источник питания — устройство генерации стабилизированного напряжения для питания ЭВМ … Краткий толковый словарь по полиграфии
источник питания (в электроснабжении) — источник питания источник питания электроэнергией [Интент] источник электропитания — [Я.Н.Лугинский, М.С.Фези Жилинская, Ю.С.Кабиров. Англо русский словарь по электротехнике и электроэнергетике, Москва, 1999 г.] Характеристики внешних… … Справочник технического переводчика
источник питания лазера — источник питания Ндп. источник накачки Часть лазера, предназначенная для преобразования подводимой к нему электрической энергии к виду, необходимому для функционирования излучателя лазера. [ГОСТ 15093 90] Недопустимые, нерекомендуемые источник… … Справочник технического переводчика
Источник питания электроэнергией — электроустановка, от которой осуществляется питание потребителя или группы потребителей электроэнергии … Российская энциклопедия по охране труда
источник (питания) переменного тока — — [Я.Н.Лугинский, М.С.Фези Жилинская, Ю.С.Кабиров. Англо русский словарь по электротехнике и электроэнергетике, Москва, 1999 г.] Тематики электротехника, основные понятия EN ac supplyac power supply … Справочник технического переводчика



