Графен, его производство, свойства и применение в электронике и др.
Графен, его производство, свойства и применение в электронике и др.
Графен является самым прочным материалом на Земле. В 300 раз прочнее стали. Лист графена площадью в один квадратный метр и толщиной, всего лишь в один атом, способен удерживать предмет массой 4 килограмма. Графен, как салфетку, можно сгибать, сворачивать, растягивать. Бумажная салфетка рвется в руках. С графеном такого не случится.
Описание графена
Свойства и преимущества графена
Физические свойства графена
Получение графена
Получение графена в домашних условиях
Применение графена
Другие формы углерода: графен, усиленный – арматурный графен, карбин, алмаз, фуллерен, углеродные нанотрубки, “вискерсы”.
Описание графена:
Графен – это двумерная аллотропная форма углерода, в которой объединённые в гексагональную кристаллическую решётку атомы образуют слой толщиной в один атом. Атомы углерода в графене соединяются между собой sp
Углерод имеет множество аллотропов. Некоторые из них, например, алмаз и графит, известны давно, в то время как другие открыты относительно недавно (10-15 лет назад) – фуллерены и углеродные нанотрубки. Следует отметить, что известный многие десятилетия графит представляет собой стопку листов графена, т.е. содержит несколько графеновых плоскостей.
На основе графена получены новые вещества: оксид графена, гидрид графена (называемый графан) и флюорографен (продукт реакции графена со фтором).
Графен обладает уникальными свойствами, что позволяет его использовать в различных сферах.
Свойства и преимущества графена:
– благодаря двумерной структуре графена, он является очень гибким материалом, что позволит использовать его, например, для плетения нитей и других верёвочных структур. При этом тоненькая графеновая «верёвка» по прочности будет аналогична толстому и тяжёлому стальному канату,
– в определённых условиях у графена активируется ещё одна способность, которая позволяет ему «залечивать» «дырки» в своей кристаллической структуре в случае её повреждений,
– графен обладает более высокой электропроводностью. Графен практически не имеет сопротивления. У графена в 70 раз мобильность электронов выше, чем у кремния. Скорость электронов в графене составляет 10 000 км/с, хотя в обычном проводнике скорость электронов порядка 100 м/с.
– обладает высокой электроемкостью. Удельная энергоемкость графена приближается к 65 кВт*ч/кг. Данный показатель в 47 раз превышает тот, который имеют столь распространенные ныне литий-ионные аккумуляторы,
– характерна полная оптическая прозрачность. Он поглощает всего 2,3% света,
– графеновая плёнка пропускает молекулы воды и при этом задерживает все остальные, что позволяет использовать ее как фильтр для воды,
– самый легкий материал. В 6 раз легче пера,
– инертность к окружающей среде,
– впитывает радиоактивные отходы,
– благодаря Броуновскому движению (тепловым колебаниям) атомов углерода в листе графена последний способен «производить» электрическую энергию,
– при протекании соленой воды по листу графена последний способен генерировать электрическую энергию за счет преобразования кинетической энергии движения потока соленой воды в электрическую (т.н. электрокинетический эффект).
Физические свойства графена*:
| Наименование показателя: | Значение: |
| Длина связи С–С, нм | 0,142 |
| Плотность, мг/м2 | 0,77 |
| Удельная площадь поверхности, м2 /г | 2630 |
| Подвижность электронов, см | 1,5 × 104 |
| Модуль Юнга, ТПа | 1 |
| Теплопроводность, Вт/(м К) | 5,1 × 103 |
| Оптическая проницаемость | 0,977 |
* при комнатной температуре.
Получение графена:
Основными способами получения графена считаются:
– микромеханическое отшелушивание слоев графита (метод Новоселова – метод скотча). Образец графита помещали между лентами скотча и последовательно отшелушивали слои, пока не остался последний тонкий слой, состоящий из графена,
– диспергирование графита в водных средах,
– механическая эксфолиация;
– химическое парофазное охлаждение (CVD-процесс),
– метод “выпотевания” углерода из растворов в металлах или при разложении карбидов.
Получение графена в домашних условиях:
Необходимо взять кухонный блендер мощностью не менее 400 Вт. В чашу блендера выливают 500 мл воды, добавляя в жидкость 10-25 миллилитров любого моющего вещества и 20-50 грамм толченого грифеля от карандаша. Далее блендер должен поработать от 10 минут до получаса вплоть до появления взвеси из чешуек графена. Полученный материал будет обладать высокой проводимостью, что позволит использовать его в электродах фотоэлементов. Также произведенный в бытовых условиях графен способен улучшить свойства пластика.
Применение графена:
– солнечная энергетика,
– водоочистка, фильтрация воды, опреснение морской воды,
– электроника (ЖК-мониторы, транзисторы, микросхемы и пр.),
– в аккумуляторах и источниках энергии. Графеновый аккумулятор позволяет автомобилю без подзарядки преодолевать 1000 км, время зарядки которого не более 16 секунд,
– медицина. Ученые обнаружили, что графеновые чешуйки оксида графена ускоряют размножение стволовых клеток и регенерацию клеток костной ткани,
– создание суперкомпозитов,
– очистка воды от радиоактивных загрязнений. Оксид графена быстро удаляет радиоактивные вещества из загрязненной воды. Хлопья оксида графена быстро связываются с естественными и искусственными радиоизотопами и конденсируют их, превращая в твердые вещества. Сами хлопья растворимы в жидкости, и их легко производить в промышленных масштабах.




карта сайта
как сделать графен википедия материал аккумулятор свойства аэрогель углерод графит купить цена видео россия презентация плотность
техническое применение открытие получение технология производство структура изобретение графена в светодиодных устройствах мастер нож
Коэффициент востребованности 5 149
Получение графена — Википедия
- композитные материалы, проводящие чернила и т. п.;
- графен низкого качества для электронных приложений;
- графен высокого качества для электронных приложений.
Для первого класса, обычно получаемого химическим расщеплением, характерны размеры графена в сотни нанометров, а восстановленные химическими методами из оксидов графена и графита плёнки имеют размер порядка 100 микрон. Такие кристаллы не подходят для транспортных измерений, так как их подвижность низка, но их можно производить в больших количествах. Для третьего класса методов, в которые включается и механическое расщепление размеры монокристаллов составляют около миллиметра и образцы применяются в исследовательских лабораториях благодаря высокой подвижности носителей тока. Для этого класса методов не существует массового производства. Второй класс методов получение графена занимает промежуточное положение как по размерам монокристаллов, так и по подвижности, благодаря чему часто используется в лабораториях и обладает потенциалом для применения в промышленности
 Рис. 1. Кусочки тонких слоёв графита, полученные в процессе отшелушивания, на поверхности липкой ленты.
Рис. 1. Кусочки тонких слоёв графита, полученные в процессе отшелушивания, на поверхности липкой ленты.Альтернативный метод предложен в работе[7]. Метод заключается в том, что окисленную подложку кремния покрывают эпоксидным клеем (в работе использовался слой толщиной ~10 мкм) и тонкую пластинку графита прижимают к клею при помощи пресса. После удаления графитовой пластинки с помощью липкой ленты на поверхности клея остаются области с графеном и графитом. Толщину графита определяли с помощью комбинационного рассеяния света и атомно-силовым микроскопом измеряли шероховатость графена, которая оказалась равной всего 0.16 нм (в два раза меньше шероховатости графена на подложке кремния[8]).
В статье[9] предложен метод печати графеновых электрических схем (ранее этот метод использовался для печати тонкоплёночных транзисторов на основе нанотрубок и для органической электроники.[10][11]). Сам процесс печати состоит из последовательного переноса с подложки Si/SiO2 золотых контактов, графена и наконец диэлектрика (PMMA) с металлическим затвором на прозрачную подложку из полиэтилентерефталата (ПЭТФ) предварительно нагретую выше температуры размягчения до 170 °C, благодаря чему контакты вдавливаются в ПЭТФ, а графен приобретает хороший контакт с материалом подложки. При таком методе нанесения графена подвижность не становится меньше, хотя и появляется заметная асимметрия между электронной (μe=10000 см2В−1с−1) и дырочной (μh=4000 см2В−1с−1) областями проводимости. Этот метод пригоден для нанесения графена на любую подложку, пригодную, в частности, для оптических измерений.
Кусочки графена также можно приготовить из графита, используя химические методы[13]. Для начала микрокристаллы графита подвергаются действию смеси серной и азотной кислот. Графит окисляется, и на краях образца появляются карбоксильные группы графена. Их превращают в хлориды при помощи тионилхлорида. Затем под действием октадециламина в растворах тетрагидрофурана, тетрахлорметана и дихлорэтана они переходят в графеновые слои толщиной 0,54 нм. Этот химический метод не единственный, и, меняя органические растворители и химикаты, можно получить нанометровые слои графита[14][15][16].
В статьях[17][18] описан ещё один химический метод получения графена, встроенного в полимерную матрицу.
Восстановлением монослойной плёнки оксида графита, например, в атмосфере гидразина с последующим отжигом в смеси аргон/водород, могут быть получены графеновые плёнки. Однако качество графена, полученного восстановлением оксида графита, ниже по сравнению с графеном, полученным скотч-методом вследствие неполного удаления различных функциональных групп. Нанесение плёнки оксида графита на DVD-диск и обработка лазером в DVD-дисководе привели к получению на диске плёнки графена с высокой электропроводностью (1738 См/м) и удельной поверхностью 1520 м2/г[19][20].
Следует упомянуть ещё два метода: радиочастотное плазмохимическое осаждение из газовой фазы (англ. PECVD)[21] и рост при высоком давлении и температуре (англ. HPHT)[22]. Из этих методов только последний можно использовать для получения плёнок большой площади.
Работы[23][24] посвящены получению графена, выращенного на подложках карбида кремния SiC(0001). Графитовая плёнка формируется при термическом разложении поверхности подложки SiC (этот метод получения графена гораздо ближе к промышленному производству), причём качество выращенной плёнки зависит от того, какая стабилизация у кристалла: C-стабилизированная или Si-стабилизированная поверхность — в первом случае качество плёнок выше. В работах[25][26] та же группа исследователей показала, что, несмотря на то, что толщина слоя графита составляет больше одного монослоя, в проводимости участвует только один слой в непосредственной близости от подложки, поскольку на границе SiC-C из-за разности работ выхода двух материалов образуется нескомпенсированный заряд. Свойства такой плёнки оказались эквивалентны свойствам графена.
Графен можно вырастить на металлических подложках рутения[27] и иридия[28].
Если кристалл пиролитического графита и подложку поместить между электродами, то, как показано в работе[29], можно добиться того, что кусочки графита с поверхности, среди которых могут оказаться плёнки атомарной толщины, под действием электрического поля могут перемещаться на подложку окисленного кремния. Для предотвращения пробоя (между электродами прикладывали напряжение от 1 до 13 кВ) между электродами также помещали тонкую пластину слюды.
Некоторая комбинация механического метода (графитовым стержнем пишут по поверхности подложки кремния, оставляя плёнки при разрушении) и последующего высокотемпературного отжига (~1100 K) использована для получения тонких слоёв графита вплоть до однослойных плёнок[30].
- ↑ 1 2 Novoselov K. S., Fal’ko V. I., Colombo L., Gellert P. R., Schwab M. G., Kim K. Дорожная карта для графена (англ.) = A roadmap for graphene // Nature. — 2012. — Vol. 490. — P. 192—200. — DOI:10.1038/nature11458.
- ↑ 1 2 Zhang Y.et. al. «Experimental observation of the quantum Hall effect and Berry’s phase in graphene» Nature 438, 201 (2005) DOI:10.1038/nature04235
- ↑ Kuzmenko A. B. cond-mat/0810.2400
- ↑ Novoselov, K. S. et al. «Two-dimensional atomic crystals», PNAS 102, 10451 (2005) DOI:10.1073/pnas.0502848102
- ↑ Ferrari A. C. et. al. Raman Spectrum of Graphene and Graphene Layers Phys. Rev. Lett. 97, 187401 (2006) DOI:10.1103/PhysRevLett.97.187401
- ↑ Novoselov K. S. et al. «Two-dimensional gas of massless Dirac fermions in graphene», Nature 438, 197 (2005) DOI:10.1038/nature04233
- ↑ Huc V., et. al. Large and flat graphene flakes produced by epoxy bonding and reverse exfoliation of highly oriented pyrolytic graphite Nanotechnology 19, 455601 (2008) DOI:10.1088/0957-4484/19/45/455601 Препринт
- ↑ Ishigami M. et. al. Atomic Structure of Graphene on SiO2 Nano Lett., 7, 1643, (2007) DOI:10.1021/nl070613a
- ↑ Chen J.-H. et. al. Printed Graphene Circuits Adv. Mater. 19, 3623 (2007) DOI:10.1002/adma.200701059 Препринт
- ↑ Hines D. R. et. al. Nanotransfer printing of organic and carbon nanotube thin-film transistors on plastic substrates Appl. Phys. Lett. 86, 163101 (2005) DOI:10.1063/1.1901809
- ↑ Hines D. R. et. al. Transfer printing methods for the fabrication of flexible organic electronics Appl. Phys. 101, 024503 (2007) DOI:10.1063/1.2403836
- ↑ Shioyama H. Cleavage of graphite to graphene J. Mat. Sci. Lett. 20, 499—500 (2001)
- ↑ Solution Properties of Graphite and Graphene Sandip Niyogi, Elena Bekyarova, Mikhail E. Itkis, Jared L. McWilliams, Mark A. Hamon, and Robert C. Haddon J. Am. Chem. Soc.; 2006; 128(24) pp 7720 — 7721; (Communication) DOI:10.1021/ja060680r
- ↑ Bunch J. S. et al. Coulomb Oscillations and Hall Effect in Quasi-2D Graphite Quantum Dots Nano Lett. 5, 287 (2005) DOI:10.1021/nl048111+
- ↑ Li X. et. al. Highly conducting graphene sheets and Langmuir-Blodgett films Nature Nanotechnology 3, 538 (2008) DOI:10.1038/nnano.2008.210
- ↑ Hernandez Y. et. al. High-yield production of graphene by liquid-phase exfoliation of graphite Nature Nanotech. 3, 563 (2008) DOI:10.1038/nnano.2008.215
- ↑ Stankovich S. et al. «Stable aqueous dispersions of graphitic nanoplatelets via the reduction of exfoliated graphite oxide in the presence of poly(sodium 4-styrenesulfonate)», J. Mater. Chem. 16, 155 (2006) DOI:10.1039/b512799h
- ↑ Stankovich S. et al. «Graphene-based composite materials», Nature 442, 282 (2006) DOI:10.1038/nature04969
- ↑ Laser Scribing of High-Performance and Flexible Graphene-Based Electrochemical Capacitors (неопр.). Sciencemag.org (16 марта 2012). Дата обращения 2 мая 2013. Архивировано 16 июня 2013 года.
- ↑ Marcus, Jennifer Researchers develop graphene supercapacitor holding promise for portable electronics / UCLA Newsroom (неопр.). Newsroom.ucla.edu (15 марта 2012). Дата обращения 2 мая 2013. Архивировано 16 июня 2013 года.
- ↑ Wang J. J. et. al. Free-standing subnanometer graphite sheets Appl. Phys. Lett. 85, 1265 (2004) DOI:10.1063/1.1782253
- ↑ Parvizi F., et. al. Graphene Synthesis via the High Pressure — High Temperature Growth Process Micro Nano Lett., 3, 29 (2008) DOI:10.1049/mnl:20070074 Препринт
- ↑ Rollings E. et. al. Synthesis and characterization of atomically thin graphite films on a silicon carbide substrate J. Phys. Chem. Solids 67, 2172 (2006) DOI:10.1016/j.jpcs.2006.05.010
- ↑ Hass J. et. al. Highly ordered graphene for two dimensional electronics Appl. Phys. Lett. 89, 143106 (2006) DOI:10.1063/1.2358299
- ↑ Berger, C. et al. «Electronic Confinement and Coherence in Patterned Epitaxial Graphene», Science 312, 1191 (2006) DOI:10.1126/science.1125925
- ↑ J. Hass et. al. Why Multilayer Graphene on 4H-SiC(000-1) Behaves Like a Single Sheet of Graphene Phys. Rev. Lett. 100, 125504 (2008).
- ↑ Sutter P. W. et. al. Epitaxial graphene on ruthenium Nature Mat. 7, 406 (2008) DOI:10.1038/nmat2166
- ↑ N’Diaye A. T. et. al. Structure of epitaxial graphene on Ir(111) New J. Phys. 10, 043033 (2008) DOI:10.1088/1367-2630/10/4/043033
- ↑ Sidorov A. N. et al., Electrostatic deposition of graphene, Nanotechnology 18, 135301 (2007) DOI:10.1088/0957-4484/18/13/135301
- ↑ Banerjee A. and Grebel H. Depositing graphene films on solid and perforated substrates, Nanotechnology 19, 365303 (2008) DOI:10.1088/0957-4484/19/36/365303
Свойства графена и его получение
Графит используется в карандашах с 1564 г. Как минерал его описал Геснер в 1565 г., название дал Вернер Шееле в 1779 г. от греч. γράφω – рисовать, писать.
Графит состоит из атомов углерода, является полуметаллом, поскольку с ростом температуры сопротивление уменьшается.
Кристалл
графита представляет собой стопку
плоских шестиугольных кристаллических
решеток. Соседние слои расположены на
расстоянии 3,37 Å друг от друга и повернуты
на 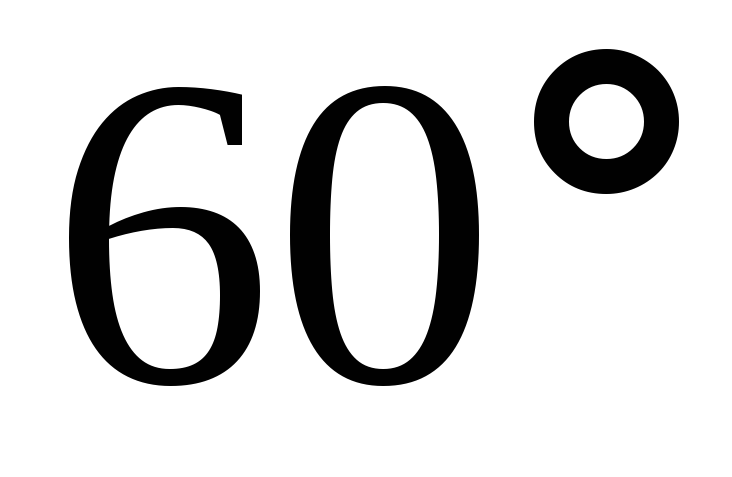 ,
их положения повторяются через одну
решетку для α-гафита, и через две – для
метастабильного β-графита. Между
решетками связи ван-дер-ваальсовы –
сила притяжения вызвана диполь-дипольным
взаимодействием. Сила слабая, решетки
отделяются друг от друга, оставляя след
карандаша на бумаге. Отделенная от
графита плоская гексагональная решетка
называетсяграфеном.
,
их положения повторяются через одну
решетку для α-гафита, и через две – для
метастабильного β-графита. Между
решетками связи ван-дер-ваальсовы –
сила притяжения вызвана диполь-дипольным
взаимодействием. Сила слабая, решетки
отделяются друг от друга, оставляя след
карандаша на бумаге. Отделенная от
графита плоская гексагональная решетка
называетсяграфеном.

Толщина графена ~(0,6–0,8) Å, расстояние между соседними атомами 1,42 Å. Связи ковалентные – валентные электроны соседних атомов являются общими для двух атомов – в своем движении охватывают оба атома. Связи сильные, поэтому решетка практически не имеет дефектов.
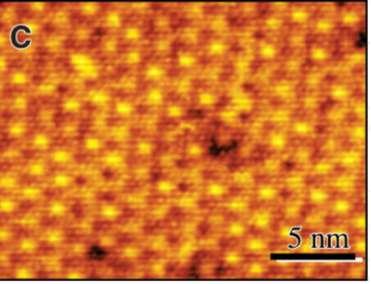
Графен в туннельном микроскопе
Свойства графена
1. Химически стабилен, оптически прозрачен. Графен на Si, покрытом слоем SiO2 толщиной d ~ 300 нм, наблюдается оптически в виде темного пятна. Модуль Юнга превышает сталь в ~20 раз.
2. Атом углерода имеет четыре валентных электрона, три обеспечивают ковалентные связи с соседними атомами гексагональной решетки. Четвертый не образует ковалентной связи, его орбиталь сосредоточена вблизи перпендикуляра к кристаллической плоскости. Орбитали соседних атомов направлены в противоположные стороны от плоскости. Поэтому гексагональная решетка состоит из двух треугольных подрешеток. Проводимость без свободных носителей обеспечивается перескакиванием четвертого электрона с одного атома на другой в обеих подрешетках. Отсутствие этого электрона является дыркой.
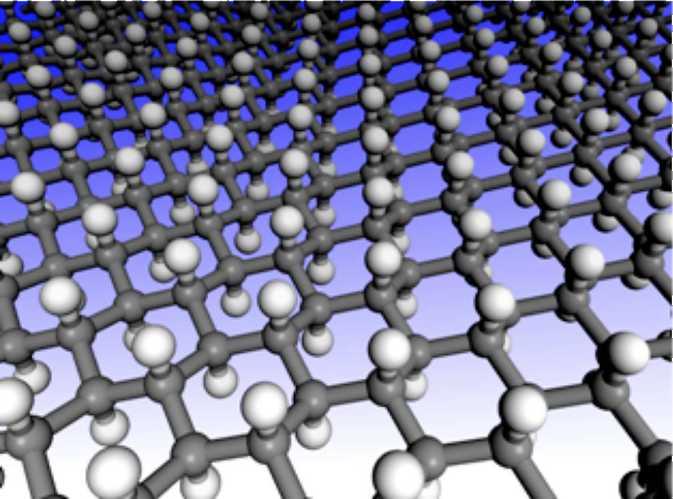
3.
В пространстве векторов обратной решетки
первая зона Бриллюэна имеет форму
шестиугольника с двумя неэквивалентными
вершинами  и
и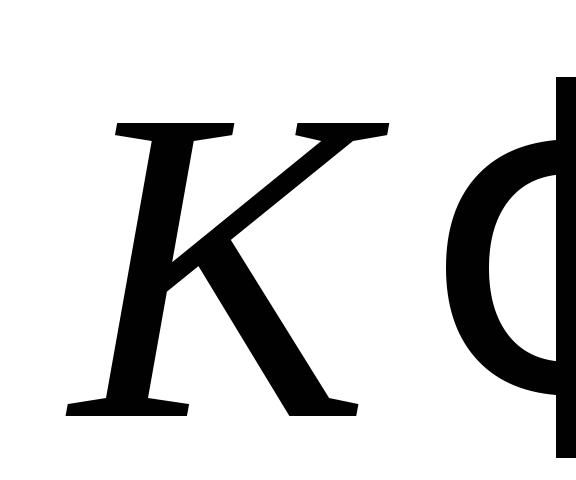 ,
называемымиточками
Дирака.
От этих точек отсчитывается энергия.
Области около точек Дирака называются долинами.
В долинах при
,
называемымиточками
Дирака.
От этих точек отсчитывается энергия.
Области около точек Дирака называются долинами.
В долинах при 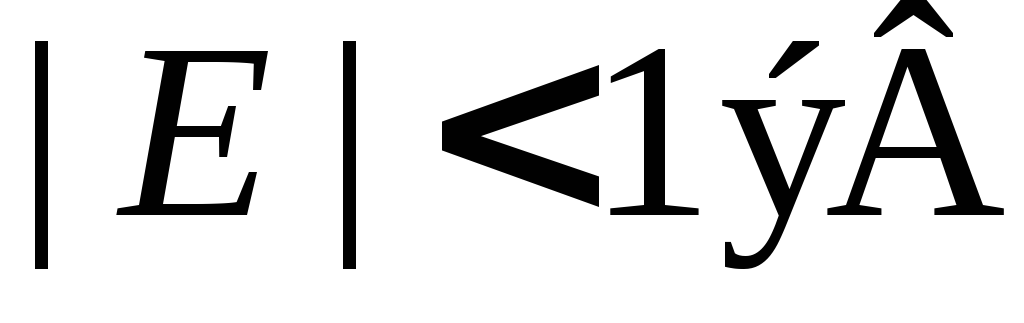 зонная структура
имеет коническую
форму. На рис. a0
2,46 Å.
зонная структура
имеет коническую
форму. На рис. a0
2,46 Å.
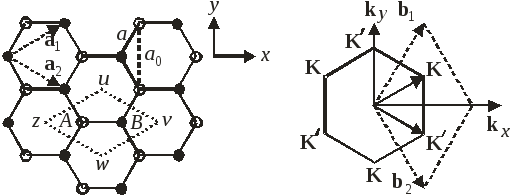
Решетка графена Зона Бриллюэна
и элементарная ячейка (u,v,w,z) обратной решетки
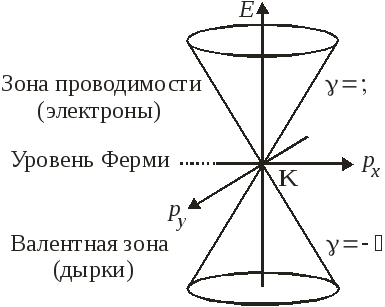
Зоны графена
Точка Дирака K совпадает с уровнем Ферми, в ней соприкасаются зона проводимости с валентной зоной, запрещенная зона отсутствует. В зоне проводимости носителем тока является электрон, в валентной зоне – дырка. При комнатной и более низкой температуре носители тока находятся вблизи уровня Ферми.
4.
Электроны и дырки имеют нулевую
эффективную массу,
высокую подвижность и при комнатной
температуре проходят без рассеяния
более 1 мкм – тысячи межатомных расстояний.
Проводимость конечная даже при нулевой
концентрации свободных носителей тока
и равна кванту проводимости 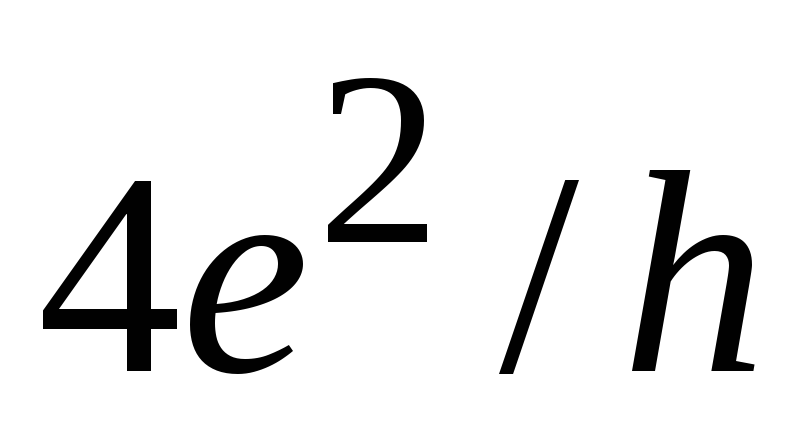 ,
где множитель 4 учитывает электрон и
дырку в двух долинах.
,
где множитель 4 учитывает электрон и
дырку в двух долинах.
5. В графене наблюдается релятивистский эффект Клейна – при нормальном падении на потенциальный барьер любой высоты электрон проходит его без отражения.
6.
В магнитном поле спектр не эквидистантный,
как для уровней Ландау, имеется уровень
с нулевой энергией. Магнитные состояния
термостабильны – разность энергий
уровней превышает тепловую энергию при
комнатной температуре 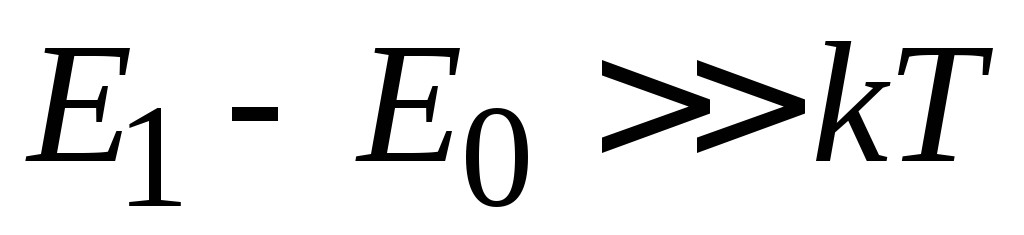 .
.
7. Нанолента графена может быть полуметаллом с нулевой шириной запрещенной зоны, или полупроводником с запрещенной зоной, ширина которой зависит от поперечного размера наноленты, от кристаллической формы края, от посторонних атомов, присоединенных к краю, от внешних электрического и магнитного полей.
8. В графене наблюдается целочисленный квантовый эффект Холла при нормальной температуре в сильном магнитном поле ~30 Тл.
9. Упругое напряжение сдвига вдоль главных кристаллографических направлений раздвигает конусы энергетических зон в точках Дирака в противоположные стороны и создает поля, подобные электромагнитному полю.
10.
Молекулы, адсорбированные на поверхность
графена, выступают как доноры (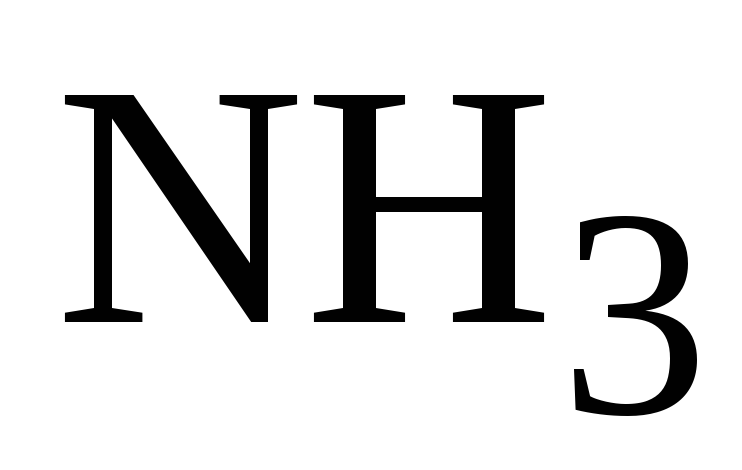 ,
,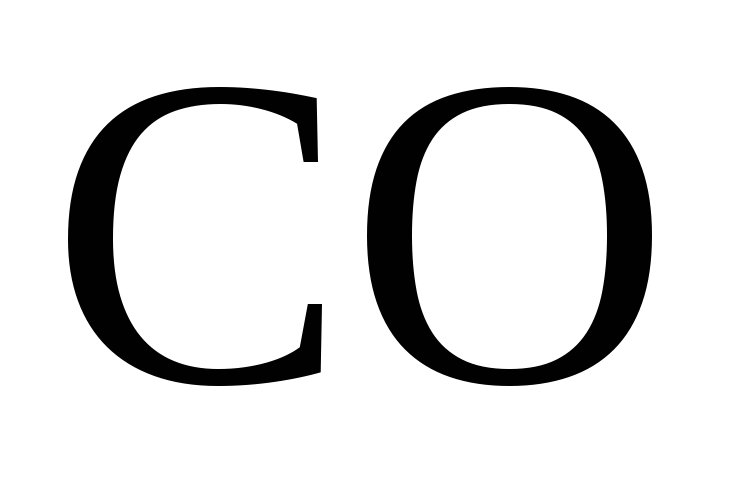 ,
, ),
как или акцепторы (
),
как или акцепторы (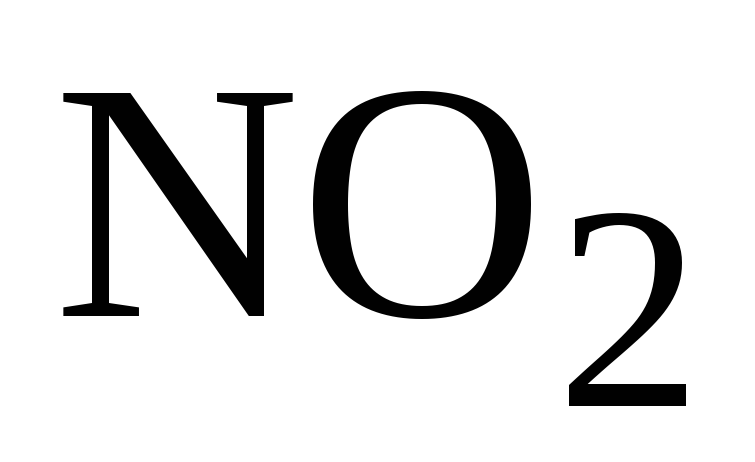 ,
,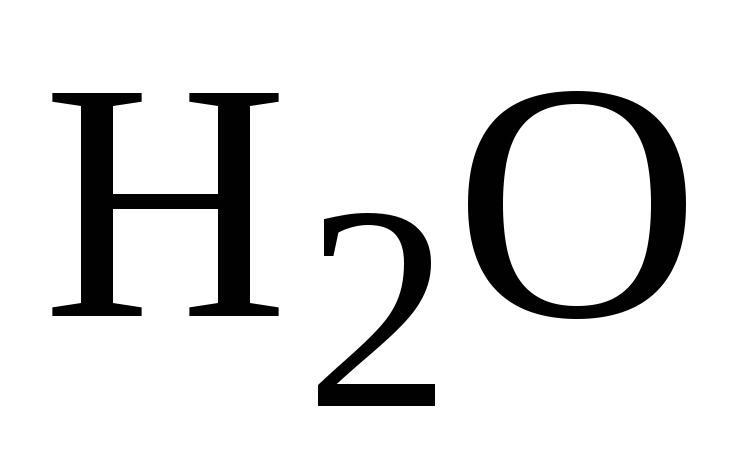 ).
В результате изменяется концентрация
носителей тока и сопротивление графена.
Поэтому графен являетсясенсором отдельных молекул.
).
В результате изменяется концентрация
носителей тока и сопротивление графена.
Поэтому графен являетсясенсором отдельных молекул.
11. Для движущихся носителей заряда n–p-переход в графене создает отрицательный показатель преломления. Плоский n–p—переход преобразует расходящийся электронный пучок в сходящийся.
12. Присоединение атомов водорода к атомам графена посредством химической реакции дает графан, являющийся диэлектриком с энергетической щелью ~5,4 эВ. Комбинирование на одной пленке графена и графана (проводника и изолятора) создает устройства с разнообразными физическими свойствами.
13. На основе графена получен полевой транзистор p-типа в 2006 г., из графеновой наноленты создан полевой транзистор n-типа в 2009 г. Размеры затворов ~10 нм.
14.
Графен является перспективным материалом
в наноэлектронике – в элементах памяти,
в солнечных элементах, как накопитель
электроэнергии, как оптически прозрачный
электрод с высокой электро- и
теплопроводностью, как стандарт
электрического сопротивления, как
транзистор терагерцевого диапазона
частот (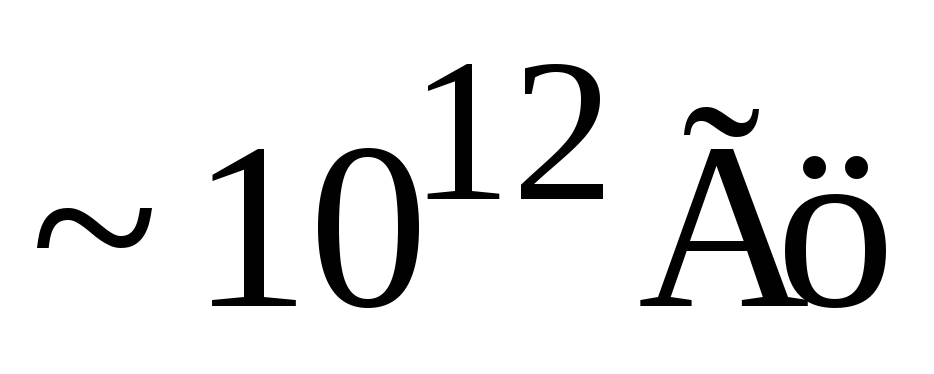 ).
Главным препятствием для широкого
использования графена является трудность
получения при массовом производстве
качественной однослойной решетки
площадью 100х100 мкм и выше.
).
Главным препятствием для широкого
использования графена является трудность
получения при массовом производстве
качественной однослойной решетки
площадью 100х100 мкм и выше.
Получение графена. В 1935–37 г.г. Р. Пайерлс и Л.Д. Ландау доказали, что в двумерной системе отсутствует дальний кристаллический порядок. Тепловые флуктуации смещений атомов вызывают искривление плоскости и ее самопроизвольное сворачивание. В 1973–77 г.г. показано, что при низких температурах может быть квазидальний порядок. Критические температуры и расстояния были неизвестны. В 2004 г. К.С. Новоселов, А.К. Гейм и С.В. Морозов получили графен площадью до 1000 мкм2 методом микромеханического расслоения графита при трении о поверхность окисленного кремния. Графен в виде мембраны в пространстве, или на подложке, оказался механически стабильным при комнатной температуре. Тепловые колебания вызывают лишь локальные искривления нанометрового размера – рипплы.
Методы получения:
Термодеструкция. При нагревании кристалла карбида кремния SiC в вакууме происходит переход в газовую фазу кремния, на поверхности кристалла остается углерод, образуются ковалентные связи, возникает графен. Существует проблема отделения графена от подложки. Если его оставить на подожке, то графен имеет энергетическую щель ~0,26 эВ;
Расслаивание графита при помощи липкой пленки с последующим переносом на поверхность окисленного кремния. Механические напряжения при расслаивании превышают предел прочности пленки и не позволяют получить ее размер, больший нескольких микрометров. Присутствуют многослойные участки;
Осаждение из газовой фазы. Переходной металл Ni, Cu, Pt, Co выдерживается в парах углеводорода, например метана, или бензола
 при
при ,
, Углеводород диссоциирует на поверхности
металла благодаря катализационному
процессу, водород десорбируется. При
медленном охлаждении углерод образует
графеновый слой в пределах кристаллического
зерна металла размером в несколько
микрометров. На краю кристаллита число
слоев возрастает из-за поступления
углерода, растворенного в металле.
Сложно отделить графен от подложки.
Углеводород диссоциирует на поверхности
металла благодаря катализационному
процессу, водород десорбируется. При
медленном охлаждении углерод образует
графеновый слой в пределах кристаллического
зерна металла размером в несколько
микрометров. На краю кристаллита число
слоев возрастает из-за поступления
углерода, растворенного в металле.
Сложно отделить графен от подложки.Интеркаляция. Используется пиролитический графит в виде мягкой, эластичной, неприлипающей пленки с рекордно высокой теплопроводностью. Молекулы
 при 110°C внедряются между слоями пиролитического
графита. Последующее резкие повышение
температуры в СВЧ-печи до значений,
превышающих температуру кипения серной
кислоты, вызывают отделение слоев
графита.
при 110°C внедряются между слоями пиролитического
графита. Последующее резкие повышение
температуры в СВЧ-печи до значений,
превышающих температуру кипения серной
кислоты, вызывают отделение слоев
графита.
Мембрана графена получается отделением графенового слоя от подложки путем ее травления. Далее графен переносится на устройство. На рис. (а) показан электромеханический резонатор на основе графена. Графен и подложка из Si образуют конденсатор. Переменное электрическое поле вызывает колебания графена. На рис. (б) дано изображение реального устройства в сканирующем электронном микроскопе с масштабом 1 мкм.
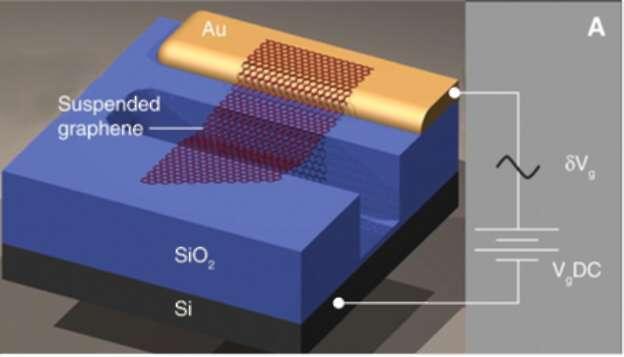

а б
Концентрация свободных носителей тока, степень заполнения зон и положение уровня Ферми регулируется затвором. Электрическое напряжение V прикладывается между подложкой из кремния и графеном. В зависимости от полярности напряжения графен обогащается электронами или дырками, возникает p—n переход.
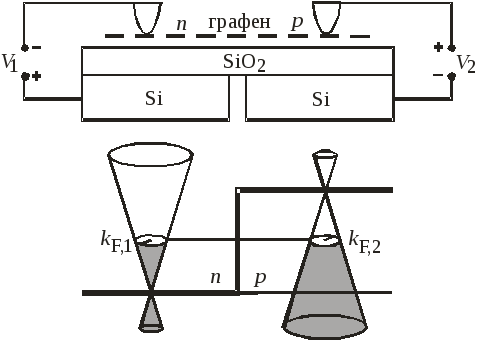
Величина
напряжения ограничена пробоем диэлектрика
SiO2 толщиной  нм
с
нм
с .
Возникающий конденсатор имеет
электроемкость
.
Возникающий конденсатор имеет
электроемкость
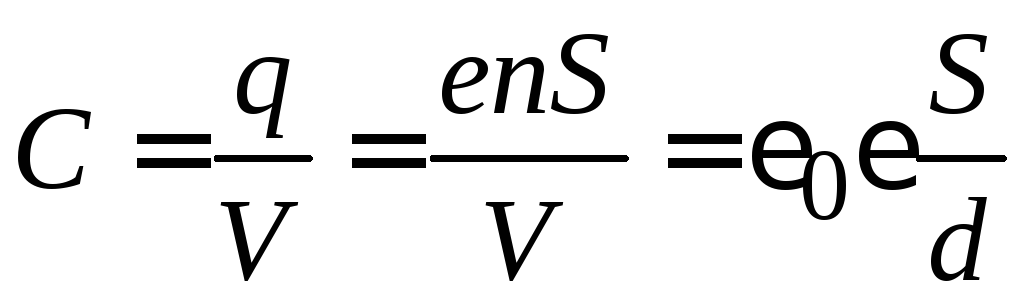 ,
,
n – поверхностная концентрация зарядов;
S – площадь графена.
Поверхностная концентрация свободных носителей тока пропорциональна напряжению
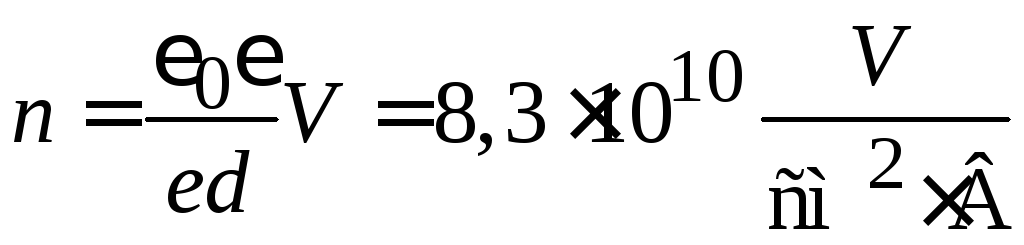 .
.
Достигнуто значение
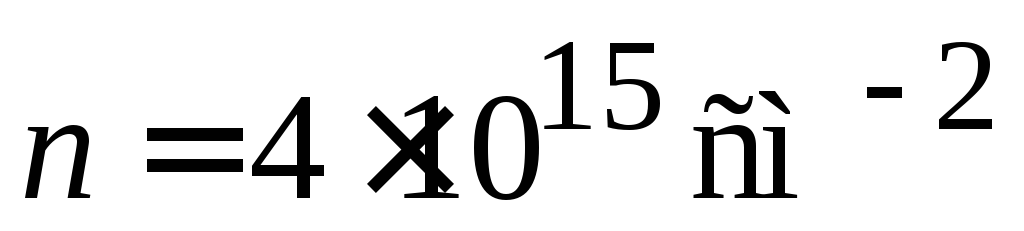 .
.
В случае дырок это означает удаление практически всех электронов, которые не задействованы в ковалентных связях. Минимальное значение
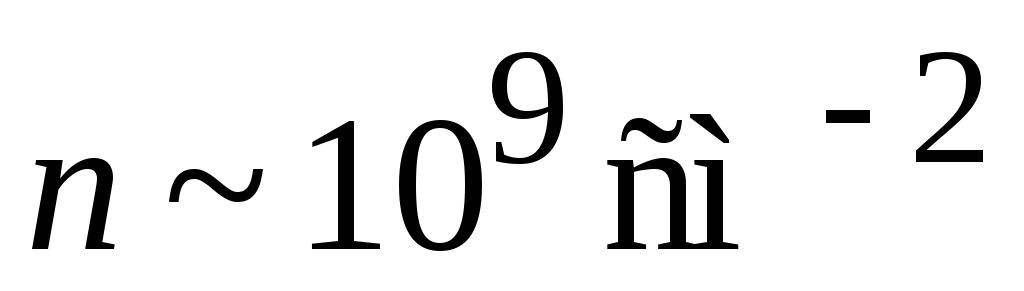 .
.
При нормальной температуре носители тока имеют высокую и слабо зависящую от температуры подвижность
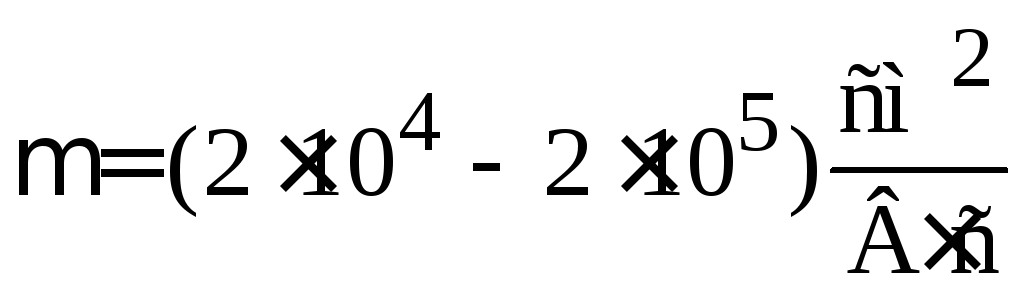 .
.
Она
существенно снижается при помещении
графена на SiO2.
Отсутствие дефектов решетки не дает
рассеяния. В результате велики время
рассеяния
и длина свободного пробега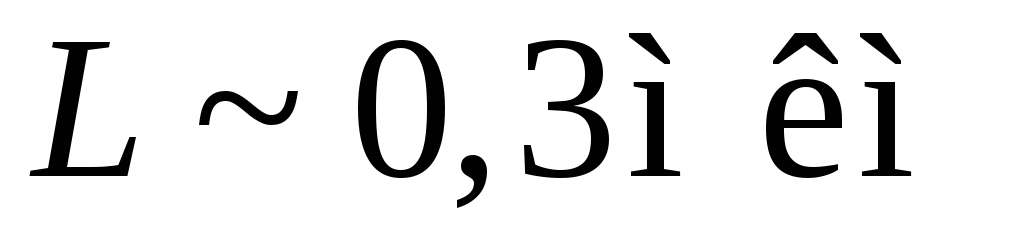 даже при комнатной температуре, что
соответствуетбаллистическому
движению зарядов.
Эти данные сопоставимы с показателями
для гетероструктуры GaAs-AlGaAs
при низкой температуре
даже при комнатной температуре, что
соответствуетбаллистическому
движению зарядов.
Эти данные сопоставимы с показателями
для гетероструктуры GaAs-AlGaAs
при низкой температуре 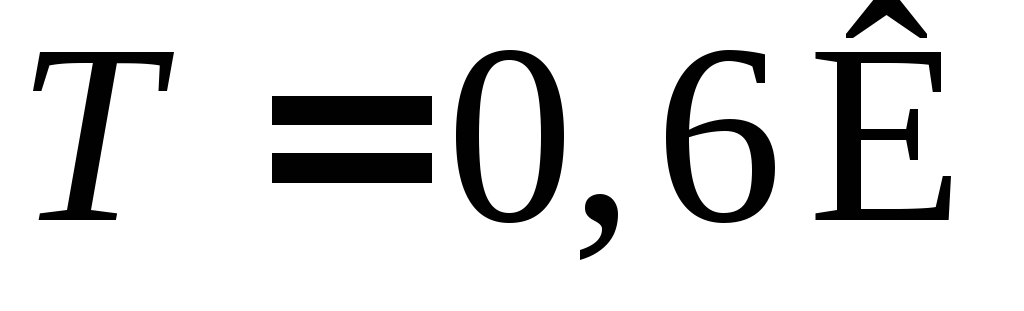
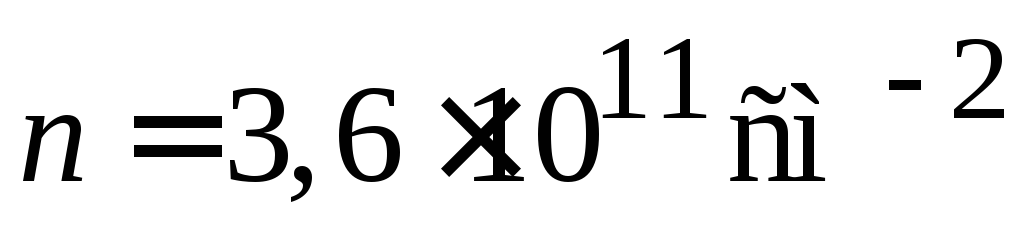 ,
, 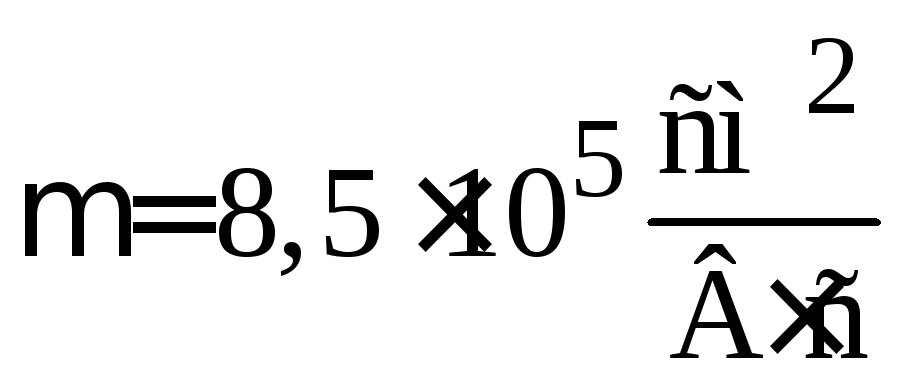 ,
,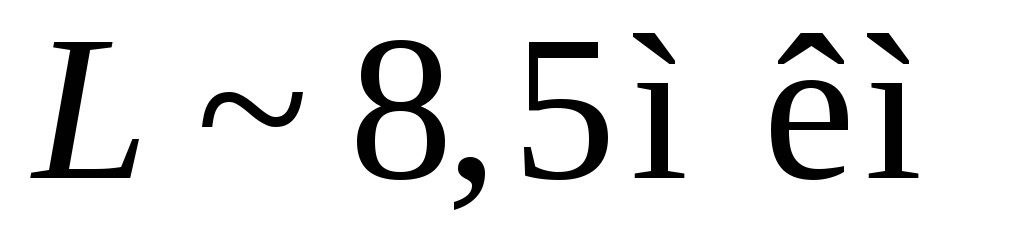 .
.
191
Двухслойный графен — Википедия
Материал из Википедии — свободной энциклопедии
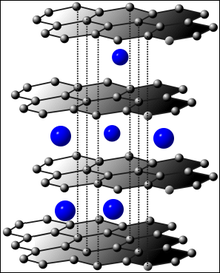
Двухслойный графен — двумерная аллотропная модификация углерода, образованная двумя близко расположенными слоями графена. Так как они расположены на расстоянии меньше 1 нм друг от друга, электроны из одного слоя графена могут туннелировать в другой, что приводит к появлению нового закона дисперсии для носителей тока. Обычно рассматривают двуслойный графен, в котором второй слой повёрнут на 60 градусов относительно первого. Это приводит к тому, что подрешётки A в нижнем графене и подрешётка B в верхнем графене выровнены в вертикальном направлении. Эта конфигурация называется AB stacking и встречается в графите.
Транспортные свойства двухслойного графена были впервые исследованы в Манчестерском университете в лаборатории А. Гейма.[1]
Гамильтониан двухслойного графена при приложенном электрическом поле между слоями записывается в виде[2][3]
- H=(−V/2cπ†00cπ−V/2t⊥00t⊥V/2cπ†00cπV/2),{\displaystyle H=\left({\begin{array}{cccc}-V/2&c\pi ^{\dagger }0&0\\c\pi &-V/2&t_{\bot }&0\\0&t_{\bot }&V/2&c\pi ^{\dagger }\\0&0&c\pi &V/2\\\end{array}}\right),}
где V — потенциал слоёв, c — фермиевская скорость, π=px+ipy{\displaystyle \pi =p_{x}+ip_{y}}, π†=px−ipy{\displaystyle \pi ^{\dagger }=p_{x}-ip_{y}}, px и py — импульсы по x и по y, t⊥{\displaystyle t_{\bot }} — туннелирование между слоями. Этот гамильтониан действует на вектор Ψ=(ψ1A,ψ1B,ψ2A,ψ2B)T{\displaystyle \Psi =(\psi _{1A},\psi _{1B},\psi _{2A},\psi _{2B})^{T}}, где индексы обозначают слой, а буквы подрешётку. Спин и долина здесь не учитывается.
Оксид графена — первый двумерный материал, достигший стадии коммерческого применения – Наука – Коммерсантъ
текст Владимир Тесленко, кандидат химических наук
В последние два десятилетия обнаружены или синтезированы многочисленные новые формы углеродных наноматериалов, в том числе фуллерены, углеродные нанотрубки и графеновые слои. Они являются перспективными материалами для многих отраслей наноиндустрии, так как обладают уникальными электронными, электромагнитными, термическими, оптическими и сорбционными свойствами.
Графен — это атомы углерода, собранные в плоскую сетку из сочлененных шестиугольников [02]. Принципиально, что графен имеет именно одноатомную толщину.
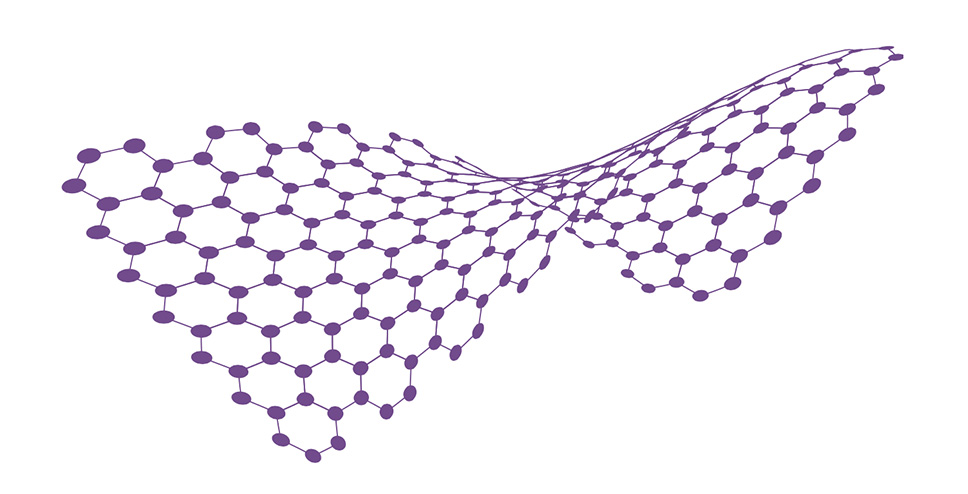
Рис. 2 Схематичное изображение графена
Крупнейший производитель графена расположен в Китае. Это компания Ningbo Morsh Technology, основанная в 2012 году. В прошлом году она запустила крупнейшую в мире линию на 300?т/г. графена. Главным потребителем выступила родственная компания Chongqing Morsh Technology, которая использует графен для производства 2 млн шт/г. прозрачных проводящих пленок для мобильных телефонов.
Особенности оксидов графена
Термин «оксиды графена» еще не получил международной дефиниции. Под оксидами графена понимают частицы графена с присоединенными по краям или внутри углеродной сетки кислородсодержащими функциональными группами и/или молекулами. Номенклатура этих групп обширна: гидроксильные, фенольные, карбонильные, карбоксильные, арильные, эфирные, фосфорсодержащие и т.?п. Разновидностью являются оксиды графена, модифицированные полимерами, такими как полиэтиленгликоль, полиэфиры, поливинилы, полиакрилы и т.д. Еще одну группу оксидов графена составляют допированные соединения. В частности, известны оксиды графена, содержащие в своей структуре один или несколько атомов бора, азота, алюминия, фосфора, кремния, серы или же группы на их основе, например меламин, фосфин, силан, полисилоксан, сульфиды и т.д.
Самые красивые оксиды графена получаются при инкорпорации молекулами краун-эфиров [03]. Их в конце 2014 года получили в знаменитом ядерными
Оксид графита — Википедия
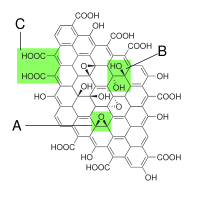
 Формула Декани
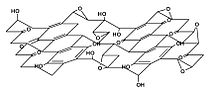
Формула Декани 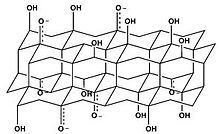 Формула Накадзима-Мацуо
Формула Накадзима-Мацуо 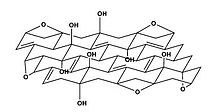 Формула Ресса
Формула Ресса 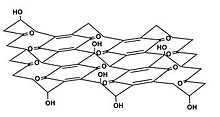 Формула Шольца-Боема
Один лист кристаллической решетки оксида графита. Показаны несколько кислородсодержащих функциональных групп. Абсолютные и относительные количества функциональных групп зависит от конкретного метода синтеза (структура Лерфа — Клиновского)
Формула Шольца-Боема
Один лист кристаллической решетки оксида графита. Показаны несколько кислородсодержащих функциональных групп. Абсолютные и относительные количества функциональных групп зависит от конкретного метода синтеза (структура Лерфа — Клиновского) 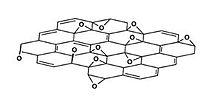 Структурная модель Гоффмана
Структурная модель ГоффманаОксид графита (оксид графена) — соединение углерода, водорода и кислорода в различных соотношениях, которое образуется при обработке графита сильными окислителями[1]. Наиболее окисленные формы являются твёрдыми жёлтыми веществами с соотношением C:O в пределах от 2,1 до 2,9.
Существует множество моделей структуры оксида графита. Это обусловлено тем что он является бертоллидом и имеет непростую аморфную структуру, а также отсутствием аналитических методов для характеристики таких материалов.
- Структура Хоффмана состоит из эпоксидных групп, распределённых по плоскости и приписывает оксиду формулу С2O.
- Ресс предложил другой вариант с использованием гидроксильных групп. Базальная плоскость превратилась из sp2— в sp3-гибридизованную систему. Эта формула была создана как аналог таковой в полимере карбон монофторида (англ.)русск..
- Модель Шольца-Боема не содержит эпоксидных групп.
- Структура Декани — модификация двух предыдущих.
- Структура Наккадзима-Мацуо является аналогом полимера дикарбон монофторида.
- Новейшая модель Лерфа — Клиновского более сосредоточена на нестехиометрической, аморфной альтернативе[1].
Основную часть оксида графита используют для приготовления дисперсной системы с щелочами для получения мономолекулярных листов, которые называют оксидом графена (по аналогии с графеном, который является однослойной формой графита)[2].
Листы из оксида графена были использованы для создания очень прочного материала, который напоминает бумагу, и как промежуточный продукт для получения графена (по состоянию на 2010 это невозможно, так как графен, полученный этими реакциями, до сих пор имеет многие химические и структурные дефекты)[2]
Оксид графита впервые был приготовлен оксфордским учёным Бенджамином Броди в 1859 году при обработке графита смесью хлората калия с азотной кислотой. В 1957 году учёными Вильямом Хаммерсом и Ричардом Офферманом был найден более надёжный, быстрый и эффективный процесс с использованием смеси серной кислоты H2SO4, нитрата натрия NaNO3 и перманганата калия KMnO4[3]. Этот метод всё еще широко распространён и до сих пор используется для синтеза оксида графита.
Недавно смесь H2SO4 и KMnO4 была использована для продольного «разрезания» углеродных нанотрубок[4], в результате чего образовались микроскопические плоские ленты из графена несколько атомов длиной, с «крышами» из атомов кислорода или гидроксильных групп[3].
Оксид графита также может быть приготовлен по методу Тан-Лау, в котором используется глюкоза. Этот метод является более безопасным, более лёгким и более экологически чистым по сравнению с традиционными реакциям с применением сильных окислителей. Другое важное преимущество метода Тан-Лау — это лёгкое управление толщиной[5].
Структура и свойства оксида графита зависят от конкретного метода синтеза и степени окисленности. Обычно сохраняются слои, как и у графита, но расстояние между ними увеличивается примерно в два раза (~0,7 нм) по сравнению с графитом. Строго говоря, «оксид» является неправильным, но исторически сложившимся названием. Кроме эпоксидных групп есть и другие экспериментально установленные функциональные группы, например, карбонильная, гидроксильная, фенольные. Существуют свидетельства «изгибов» и растрескивания графеновых листов оксида при осаждении слоев на субстрате. Детальная структура до сих пор не понятна из-за сильного расстройства и нерегулярной упаковки слоёв[3].
Толщина графеновых слоёв оксида составляет около 1,1 ± 0,2 нм. При помощи туннельной микроскопии были найдены местные регионы, где атомы кислорода расположены в постоянной решетке 0,27 нм × 0,41 нм, края каждого слоя обрываются карбоксильными и карбонильными группами. Рентгеновская фотоэлектронная спектроскопия показывает наличие атомов углерода в кольцах, не содержащих кислорода (284,8 эВ), C-O (286,2 эВ) в C=O (287,8 эВ) и в O-C=O (289,0 эВ)[6].
Оксид графита легко гидратируется, в результате чего увеличивается межплоскостное расстояние (до 1,2 нм в насыщенном состоянии). Дополнительное количество воды также включается в прослойку из-за высокого давления индуцированных эффектов[7]. Основной продукт поглощает влагу из окружающего воздуха пропорционально влажности. Полное удаление воды очень тяжело, так как нагревание при 60-80 °С приводит к частичному разложению и деградации материала. Подобно воде, оксид графита также легко включает другие полярные растворители, например, спирты (а также ДМФА и N-метилпирролидон). Разделение слоев оксида графита пропорционально размеру молекулы спирта, дополнительные монослои вставляются в структуру при высоком давлении[8].
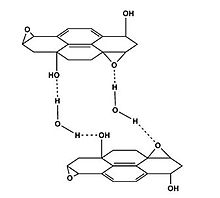 Предполагаемые водородные мостики между оксидом графита и водой
Предполагаемые водородные мостики между оксидом графита и водойОксид графита разлагается при быстром нагревании при умеренно высоких температурах (~280—300 °C) с образованием мелкодисперсного аморфного углерода, немного похожего на активированный уголь. Сажа состоит из тончайших графитовых чешуек толщиной 2—5 нм, диаметр которых может доходить до нескольких сотых долей миллиметра, что зависит от природы исходного графита. Поскольку при этом высвобождается кислород, связанный в виде СО и СO2 в оксиде графита, не исключено, что в решетке графита возникают пустоты атомарных размеров.
Благодаря специфической двумерной структуре и существованию разных кислородсодержащих функциональных групп оксид графита имеет множество применений в самых разнообразных областях[2].
Суперконденсаторы[править | править код]
Гидроксид калия реструктурирует оксид графита, создавая трёхмерную пористую конструкцию. Каждая её стенка имеет атомарную толщину, а площадь поверхности «активированного» оксида графита доходит до 3100 м²/г. Материал также отличается высокой удельной электропроводностью. Диаметр большей части пор в готовых образцах попадает в интервал 0,6—5 нм. В экспериментах суперконденсатор, построенный с использованием нового электродного материала, показал очень хорошие гравиметрические ёмкость и плотность энергии, причём последняя приближалась к показателям свинцово-кислотных аккумуляторов. После 10 000 циклов зарядки/разрядки «активированный» оксид графита продолжал работать на 97 % исходной ёмкости.
Сверхпрочная бумага[править | править код]
При растворении в воде оксид графита расслаивается на слои оксида графена. Полученный раствор фильтруют через специальную мембрану, на которой слои вновь связываются, но уже в гораздо более прочную, чем графит, структуру — графеновую бумагу. Слои обычного графита связаны между собой очень слабо и разрыв связей происходит легко. В графеновой бумаге, напротив, слои переплетаются между собой, поэтому нагрузка может распределяться равномерно по всей структуре, делая её весьма прочной. То, как слои переплетаются, позволяет им слегка смещаться друг относительно друга, делая всю структуру гибкой. Что еще важнее, можно химически управлять свойствами данного материала, изменяя количество кислорода в слоях. Например, уменьшив его, можно сделать бумагу из диэлектрика хорошим проводником. Также планируется внедрять в структуру графеновой бумаги различные полимеры и металлы, создавая композиты, превосходящие по своим свойствам как чистый графен, так и допант.
Исследования ДНК[править | править код]
Большая плоская поверхность оксида графена позволяет одновременно исследовать несколько ДНК-зондов, меченных различными красителями, обеспечивая обнаружение нескольких целевых ДНК в том же растворе. Дальнейший прогресс в поиске сенсоров из оксида графена и ДНК может привести к созданию недорогих систем экспресс-анализа ДНК[9]. В медицине для лечения рака мозга, щитовидной железы, и тд.
- ↑ 1 2 He H., Klinowski J., Forsterb M., Lerf A. A new structural model for graphite oxide (англ.) // Chemical Physics Letters. — 1988. — Vol. 287, no. 1—2. — P. 53—56. — DOI:10.1016/S0009-2614(98)00144-4.
- ↑ 1 2 3 Niyogi S., Bekyarova E., Itkis M. E., McWilliams J. L., Hamon M. A., Haddon R. C. Solution Properties of Graphite and Graphene (англ.) // J. Am. Chem. Soc. — 2006. — Vol. 128, no. 24. — P. 7720—7721. — DOI:10.1021/ja060680r.
- ↑ 1 2 3 Hummers Jr. W. S., Offeman R. E. Preparation of Graphitic Oxide (англ.) // J. Am. Chem. Soc. — 1958. — Vol. 80, no. 6. — P. 1339. — DOI:10.1021/ja01539a017.
- ↑ Kosynkin D. V., Higginbotham A. L., Sinitskii A., Lomeda J. R., Dimiev A., Price B. K., Tour J. M. Longitudinal unzipping of carbon nanotubes to form graphene nanoribbons (англ.) // Nature. — 2009. — Vol. 458, no. 7240. — P. 872—876. — DOI:10.1038/nature07872. — PMID 19370030.
- ↑ Tang L., Li X., Ji R., Teng K. S., Tai G., Ye J., Wei C., Lau S. P. Bottom-up synthesis of large-scale graphene oxide nanosheets (англ.) // J. Mater. Chem. — 2012. — Vol. 22. — P. 5676—5683. — DOI:10.1039/C2JM15944A.
- ↑ Stankovich S., Piner R. D., Chen X., Wu N., Nguyen S. T., Ruoff R. S. Stable aqueous dispersions of graphitic nanoplatelets via the reduction of exfoliated graphite oxide in the presence of poly(sodium 4-styrenesulfonate) (англ.) // J. Mater. Chem. — 2006. — Vol. 16. — P. 155—158. — DOI:10.1039/B512799H.
- ↑ Talyzin A. V., Solozhenko V. L., Kurakevych O. O., Szabó T., Dékány I., Kurnosov A., Dmitriev V. Colossal Pressure-Induced Lattice Expansion of Graphite Oxide in the Presence of Water (англ.) // Angew. Chem. Int. Ed. — 2008. — Vol. 47, no. 43. — P. 8268—8271. — DOI:10.1002/anie.200802860. — PMID 18814163.
- ↑ Talyzin A. V., Sundqvist B., Szabó T., Dékány I., Dmitriev V. Pressure-Induced Insertion of Liquid Alcohols into Graphite Oxide Structure (англ.) // J. Am. Chem. Soc. — 2009. — Vol. 131, no. 51. — P. 18445—18449. — DOI:10.1021/ja907492s. — PMID 19947629.
- ↑ He S., Song B., Li D., Zhu C., Qi W., Wen Y., Wang L., Song S., Fang H., Fan C. A Graphene Nanoprobe for Rapid, Sensitive, and Multicolor Fluorescent DNA Analysis (англ.) // Advanced Functional Materials. — 2010. — Vol. 20, no. 3. — P. 453—459. — DOI:10.1002/adfm.200901639.
Подвешенный графен — Википедия
Материал из Википедии — свободной энциклопедии
Подвешенный графен — графен, который не касается подложки, свободновисящая плёнка, которая удерживается только частично благодаря подложке или контактам.
Существует несколько способов сделать подвешенный графен.
Первый метод был предложен в работе[1], где в подложке кремния покрытой слоем диэлектрика SiO2 перед нанесением графена протравливались канавки шириной около 1 микрона. После осаждения графена с липкой ленты на эту подложку приходилось искать удачно осаждённый графен на область с канавкой. Графен держался благодаря хорошей адгезии в местах контакта с диэлектриком в по обе стороны от канавки[2]. В работе[1] изучались механические свойства графена. Позже этот метод использовался и для измерения распределения напряжений в подвешенной плёнке[3].
Для оптических измерений или для электронного просвечивающего микроскопа необходимо избавиться от подложки, что и было сделано в работах Мейера и других исследователей[4][5]. В этих работах было показано, что графен в свободном состоянии, не соединённый с подложкой, принимает волнистую форму с высотой неоднородностей около 1 нм. В работе[6] была измерена оптическая прозрачность подвешенного графена и показана её универсальность, определяемая только постоянной тонкой структуры.
Ещё один способ получить подвешенный графен — это вытравить диэлектрик под одноатомной плёнкой[7][8]. Из-за того, что основной вклад в рассеяние носителей в графене вносят заряженные примеси в диэлектрике[9], исследователи стали искать способ избавиться от этого механизма рассеяния или свести его к минимуму. Избавление от подложки и отжиг привел к существенному повышению подвижности носителей в графене (около 200000 см2В−1с−1)[7]. В таких плёнках доминирующий механизм меняется и основной вклад в рассеяние вносят фононы или границы образца[10]. В последнем случае можно говорить о баллистическом транспорте.




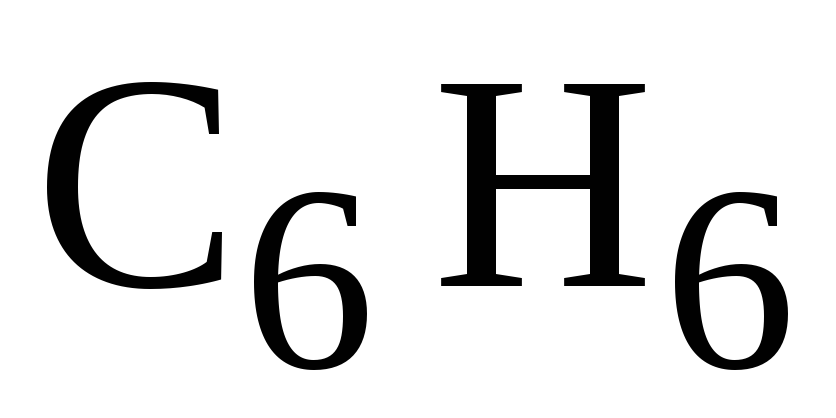 при
при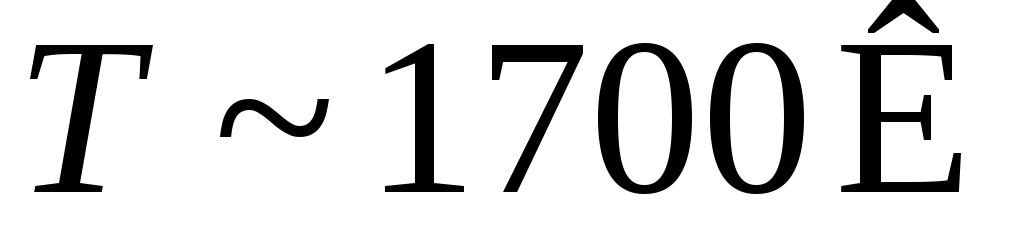 ,
,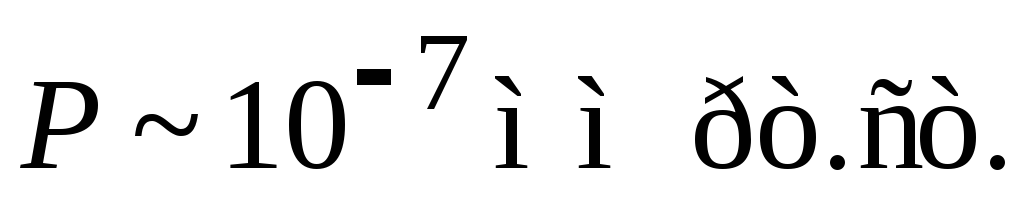 Углеводород диссоциирует на поверхности
металла благодаря катализационному
процессу, водород десорбируется. При
медленном охлаждении углерод образует
графеновый слой в пределах кристаллического
зерна металла размером в несколько
микрометров. На краю кристаллита число
слоев возрастает из-за поступления
углерода, растворенного в металле.
Сложно отделить графен от подложки.
Углеводород диссоциирует на поверхности
металла благодаря катализационному
процессу, водород десорбируется. При
медленном охлаждении углерод образует
графеновый слой в пределах кристаллического
зерна металла размером в несколько
микрометров. На краю кристаллита число
слоев возрастает из-за поступления
углерода, растворенного в металле.
Сложно отделить графен от подложки.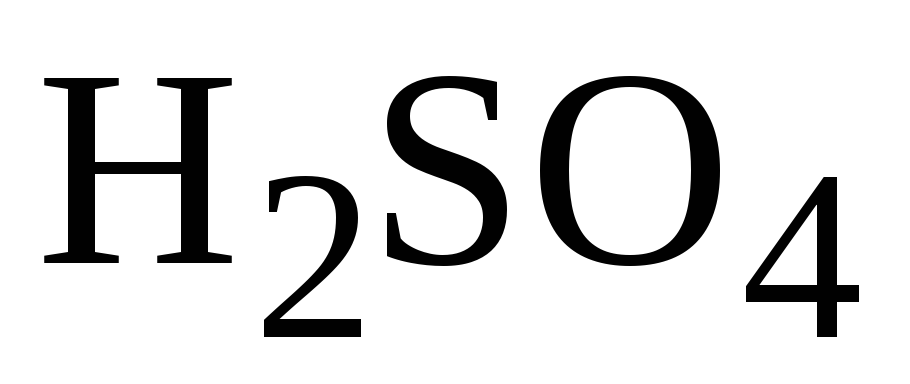 при 110°C внедряются между слоями пиролитического
графита. Последующее резкие повышение
температуры в СВЧ-печи до значений,
превышающих температуру кипения серной
кислоты, вызывают отделение слоев
графита.
при 110°C внедряются между слоями пиролитического
графита. Последующее резкие повышение
температуры в СВЧ-печи до значений,
превышающих температуру кипения серной
кислоты, вызывают отделение слоев
графита.