Замена электролита в аккумуляторе в домашних условиях
Автомобильные аккумуляторы сегодня представлены двумя наиболее распространенными типами: необслуживаемые и обслуживаемые АКБ. В первом случае штатно реализована только возможность дозаряжать батарею при помощи зарядного устройства.
Второй тип аккумуляторов позволяет не только заряжать батарею, но и производить проверку плотности электролита в «банках» (секциях), анализировать его состояние. При необходимости уровень электролита также можно повысить или полностью заменить жидкость.
Что касается необслуживаемых батарей, получение доступа к электролиту также возможно, однако предполагает самостоятельное внесение изменений в устройство корпуса аккумулятора. Если точнее, потребуется высверливать дополнительные отверстия и затем их герметизировать.
Далее мы поговорим о том, для чего нужен электролит в аккумуляторе, можно ли доливать электролит в аккумулятор и как это правильно сделать.
Содержание статьи
Когда нужно доливать электролит в аккумулятор и как это делается
Начнем с того, что общий принцип работы батареи заключается в возможности накопления электрического заряда благодаря протекающим химическим реакциям между электролитом и свинцовыми пластинами внутри аккумулятора. Указанные реакции протекают под воздействием электрического тока.
Ток подается на АКБ во время работы двигателя. Если точнее, подача электричества происходит от автомобильного генератора. Также отдельно заряжать аккумулятор можно при помощи внешнего зарядного устройства (ЗУ). В процессе эксплуатации наиболее частой неисправностью аккумулятора является потеря плотности электролита. К основным причинам можно отнести старение, сульфатацию пластин, перезаряд или недозаряд АКБ.
Сульфатация пластин, как правило, является результатом недостаточно заряда. Дело в том, что внутри батареи находятся специальные решетки, в которых находится диоксид свинца. При разряде батареи оксид свинца восстанавливается на катоде, при этом также активизируется окислительный процесс на аноде. Если просто, анод и катод можно условно считать более привычным «плюсом» и «минусом».
Указанные процессы приводят к тому, что происходит усиленное образование сульфата свинца. Результатом такого образования становится снижение плотности серной кислоты в составе электролита. В этом случае необходимо измерить плотность специальным прибором (ареометром), после чего необходимо поднять данный показатель до нужного значения.
При этом неправильным подходом является долив электролита сразу после замеров, то есть прямо на авто. Чтобы избежать ошибок, нужно знать, как добавлять электролит в аккумулятор. Дело в том, что плотность следует измерять на АКБ, которая была предварительно полностью заряжена.
Также в «банках» должен быть нормальный уровень электролита. Игнорирование данных правил приводит к тому, что процесс сульфатации не прекращается, батарея выходит из строя. Если же плотность на заряженной батарее находится в рекомендуемых пределах от 1.27 до 1.29, тогда электролит просто доливается по уровню и аккумулятор эксплуатируется далее.
Когда плотность оказывается меньше рекомендуемой, тогда для начала следует реализовать несколько циклов, предполагающих полный заряд-разряд АКБ. Только затем можно долить свежий электролит, добиваясь нужной плотности. В тех случаях, когда плотность электролита выше нормы, тогда в аккумулятор доливают дистиллированную воду. Использование обычной воды не рекомендуется, так как возможно выпадение осадка и другие нежелательные последствия.
Добавим, что еще важно учитывать, сколько нужно электролита в аккумулятор. Данная информация пригодится в ситуациях с доливом, так как в случае полной замены электролита желательно заранее уточнить необходимое количество у продавцов АКБ, на профильных авто форумах или из других источников.
Что касается обслуживаемого аккумулятора, ответом на вопрос, как проверить уровень электролита в аккумуляторе, является необходимость выкрутить пробки на «банках». После их откручивания можно увидеть метки, указывающие на уровень. Если таких меток нет, дистиллированную воду или электролит доливают так, чтобы перекрыть поверхность пластин на 5 или 7 мм.
Следует отдельно учитывать, что уровень не должен быть слишком высоким. Нужно добиться того, чтобы оставалось 2 см. до среза пробки. С необслуживаемым аккумулятором возникают дополнительные сложности как с получением доступа к «банкам», так и с определением уровня, количества электролита и т.п. По этой причине производить такие манипуляции без соответствующего опыта не рекомендуется.
Как поменять электролит в аккумуляторе автомобиля и когда это нужно
Итак, теперь давайте рассмотрим ситуацию, когда требуется полная замена электролита в АКБ. Чаще всего понять, нужно ли менять электролит в аккумуляторе, помогает его визуальная оценка и некоторые другие характерные признаки.
Как правило, на необходимость замены указывает:
- мутный электролит в аккумуляторе, изменение цвета;
- не удается добиться нужной плотности после зарядки АКБ;
Также специалисты рекомендуют в полном объеме поменять электролит в тех случаях, когда относительно новый аккумулятор стал быстро разряжаться после полной зарядки при помощи ЗУ, во время проверки было выявлено, что в аккумуляторе в одной банке нет электролита, ранее происходило замерзание электролита и т.д.
На практике помутнение указывает на то, что в АКБ изначально залит электролит низкого качества, также возможен вариант использования низкосортного продукта на долив. Также к помутнениям приводит заливание проточной, а не дистиллированной воды. Еще возможно, что доливаемая вода содержит посторонние примеси.
Следующей причиной того, что электролит мутный, становится повреждение, а также осыпание пластин. Параллельно не следует исключать вероятность короткого замыкания в одной секции или сразу в нескольких. Как правило, появление мутного осадка серого цвета указывает на осыпание пластин, черный или темный цвет электролита выступает признаком плохого качества основных компонентов электролита (воды и/или кислоты). Коричневый цвет свидетельствует о том, что в аккумуляторе короткое замыкание.
Как правило, появление мутного осадка серого цвета указывает на осыпание пластин, черный или темный цвет электролита выступает признаком плохого качества основных компонентов электролита (воды и/или кислоты). Коричневый цвет свидетельствует о том, что в аккумуляторе короткое замыкание.
Необходимо учитывать, что в случае осыпания или короткого замыкания решение поменять электролит в ряде случаев может не привести к положительному результату. Дело в том, что для восстановления работоспособности необходимо также отдельно ремонтировать секции АКБ, при этом такая операция требует спецоборудования.
В остальных случаях замена электролита в аккумуляторе в домашних условиях вполне возможна. Более того, правильно выполненная процедура может существенно продлить срок службы АКБ. Для реализации задачи понадобиться заранее подготовить:
- свежий электролит с нужной плотностью;
- дистиллированную воду;
- ареометр для замеров плотности;
- резиновую грушу или шприц для откачки старого электролита из банок;
- воронку для удобства залива чистой воды и электролита;
- емкость для слива старого электролита, выкачиваемых излишков и т.
 п.
п.
Обычные стеклянные банки или бутылки хорошо подойдут в качестве емкости, так как на них не воздействует серная кислота. Еще желательно иметь защитные очки и резиновые перчатки, так как работа с кислотными растворами предполагает соблюдение определенных правил техники безопасности.
Дело в том, что электролит после попадания на открытую кожу может причинить химические ожоги. Также значительную опасность такой раствор представляет для глаз. При попадании на кожу электролит нужно немедленно смыть при помощи содового раствора. В случае попадания в глаза нужно промыть их большим количеством воды, после чего немедленно обратиться за профессиональной медицинской помощью.
Итак, перейдем к замене. Сразу отметим, на начальном этапе нужно знать, как правильно слить электролит с аккумулятора. Вполне очевидно, что многие стремятся быстрее убрать жидкость из АКБ, при этом не задумываясь о том, можно ли переворачивать аккумулятор при замене электролита.
Казалось бы, достаточно открутить пробки на банках, перевернуть батарею и слить из корпуса старый электролит. Обратите внимание, в половине случаев такой подход приводит к окончательному выходу аккумулятора из строя. Дело в том, что частицы осадка, которые осели в нижней части, после переворачивания застревают между пластинами. В результате в АКБ далее возникнет короткое замыкание. Если вы ранее не обслуживали батарею, тогда рекомендуем ознакомиться с тем, как правильно заправить аккумулятор электролитом.
Обратите внимание, в половине случаев такой подход приводит к окончательному выходу аккумулятора из строя. Дело в том, что частицы осадка, которые осели в нижней части, после переворачивания застревают между пластинами. В результате в АКБ далее возникнет короткое замыкание. Если вы ранее не обслуживали батарею, тогда рекомендуем ознакомиться с тем, как правильно заправить аккумулятор электролитом.
- Первым делом нужно снять батарею и обтереть корпус, удаляя различные загрязнения. Для этих целей лучше всего подходить тряпка, которую предварительно смачивают в растворе воды и соды. Чтобы сделать сам раствор, следует пару столовых ложек соды развести в литре воды.
- Затем нужно окрутить заливные пробки на АКБ, после чего производится проверка уровня электролита, его состояние, цвета. Также нужно оценить степень заряда батареи при помощи мультиметра.
- Если жидкость явно нуждается в замене, тогда далее старый электролит откачивается из банок грушей, шприцем или при помощи любого другого подобного решения.

- Далее в опустевшие банки нужно залить дистиллированную воду, после чего аккумулятор слегка покачивают. Это нужно для промывки. Промывают АКБ несколько раз, на каждом этапе сливая воду из банок. Делать это необходимо до тех пор, пока вода не станет полностью прозрачной.
- Затем можно залить в банки свежий электролит, причем не нужно сразу стремиться довести его плотность до нормы.
- Теперь аккумулятор нужно поставить на зарядку от ЗУ. Только после полного окончания процесса зарядки производится проверка плотности ареометром.
- Дополнительно перед замерами рекомендуется выждать время, чтобы батарея успела остыть. Обычно требуется 1.5-2 часа. Затем (на основании полученных при замерах данных) осуществляется корректировка путем подбора нужного соотношения воды или электролита.
На практике процедура замены предполагает откачивание из каждой банки электролита, после чего производится его слив в заготовленную для этих целей емкость. При этом нужно учесть, что удалить жидкость полностью таким способом не выйдет.
- Для наиболее эффективного удаления нужно медленно наклонять корпус АКБ, выбирая жидкость. Однако нужно помнить, что переворачивать корпус категорически запрещено, как и было сказано выше. Чтобы не держать батарею, можно подкладывать под корпус бруски или другие предметы для упора.
- Также на носике груши можно дополнительно установить гибкую трубку (например, от капельницы). Главное, чтобы диаметр трубки, позволял плотно ее надеть и зафиксировать.
- После слива жидкости из банок наклоненный аккумулятор устанавливается в нормальное положение, затем в каждую банку заливается дистиллированная вода через воронку.
- Во время промывки не допускается трясти аккумулятор, резко наклонять корпус и т.д. Будет достаточно нескольких плавных наклонов в разные стороны. После этого вода сливается, процедура промывки повторяется.
- Теперь можно залить электролит, однако не следует сразу доводить его количество до нужного уровня. Дело в том, что электролиты в продаже имеют повышенную плотность.
 Это значит, что далее раствор нужно разбавлять дистиллированной водой. В самом начале будет достаточно придерживаться приблизительных показателей, так как до нормы плотность доводится уже после заряда АКБ.
Это значит, что далее раствор нужно разбавлять дистиллированной водой. В самом начале будет достаточно придерживаться приблизительных показателей, так как до нормы плотность доводится уже после заряда АКБ.
Также добавим, что после того, как электролит был залит, нужно плавно наклонить аккумулятор несколько раз (как и при промывке). Это позволит удалить воздух из банок аккумуляторной батареи. Теперь пробки можно прикрыть, но не закручивать полностью. Саму батарею необходимо оставить на пару часов. Это нужно для отстаивания жидкости в банках.
Затем потребуется снова проверить уровень электролита и его плотность, доливая кислоту или воду при такой необходимости. Также при необходимости можно добавить в электролит специальную присадку, которая помогает удалить сульфаты с электродов. Далее нужно выждать, пока под действием электролита из корпуса окончательно не выйдут все остатки воздуха, а также растворится присадка. Отметим, что добавка растворяется около 2 суток. После этого АКБ можно ставить на зарядку.
После замены электролита сколько нужно заряжать аккумулятор
В самом начале заряжать батарею после замены электролита рекомендуется малыми токами (0.1 А). Для зарядки нужно открутить пробки и подключить ЗУ. Главное, чтобы аккумулятор после замены электролита заряжался циклично, то есть предполагается схема «заряд-разряд».
Данный процесс нужно повторять до тех пор, пока плотность электролита не достигнет нужного показателя. Параллельно нужно следить за тем, чтобы электролит в АКБ не выкипал. На полную зарядку укажет напряжение 2.4 В применительно к отдельной секции или 14-15 В на клеммах батареи.
После того, как будет достигнуто номинальное напряжение, ток заряда следует уменьшить в два раза. Если в течение 2 часов плотность электролита не меняется, тогда можно прекратить процесс зарядки.
Что касается разряда-заряда и цикличности, разряжать батарею нужно, в среднем, до половины емкости, после чего снова производится полная зарядка. Для разряда АКБ к клеммам подключается потребитель (для этих целей можно использовать простые 12 В автолампочки). После подключения производится контроль напряжения батареи, чтобы не допустить глубокого разряда. Когда разрядка достигает отметки 10.5 В, аккумулятор снова ставится на зарядку.
После подключения производится контроль напряжения батареи, чтобы не допустить глубокого разряда. Когда разрядка достигает отметки 10.5 В, аккумулятор снова ставится на зарядку.
Что в итоге
Как видно, в ряде случаев удается эффективно восстановить работоспособность автомобильного аккумулятора путем промывки банок и заправки нового электролита. При этом все равно не стоит рассчитывать на то, что замена электролита позволит батарее отработать долгий срок. В одних случаях АКБ нормально работает 6-12 и более месяцев, тогда как в других проблемы могут начаться через несколько дней.
Напоследок добавим, что также не рекомендуется производить какие-либо манипуляции с необслуживаемыми АКБ. Такие батареи лучше сразу менять на новые в том случае, если элементу не удается вернуть работоспособность после одного или нескольких циклов «разряд-заряд».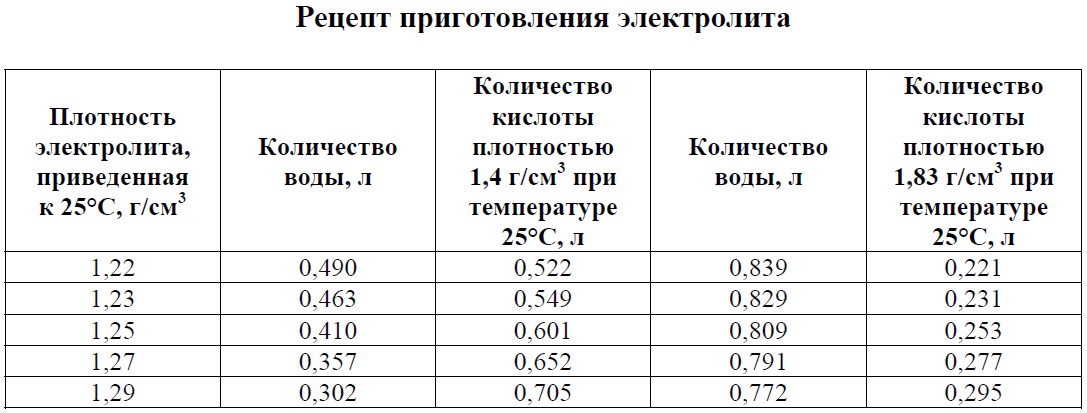
Что касается утилизации старого электролита, нельзя сливать раствор в водоемы, выливать на землю, в каналаизацию и т.п. Дело в том, что кислоту нужно сначала нейтрализовать. Для решения задачи рекомендуем отдельно изучить этот вопрос на профильных форумах или получить профессиональную консультацию специалистов. Это позволит точно определиться с наиболее подходящим вариантом, кторый будет оптимальным в каждом отдельном случае.
Читайте также
Делаем электролит для АКБ собственноручно | Описания, разъяснения | Статьи
Без электролита не возможен процесс накопления энергии. На данный момент технологии стремятся вверх и источники питания уже с завода заправляются электрохимической жидкостью и заряжаются, по сути вам нет нужды что-либо делать, данный аккумуляторные батареи именуют как необслуживаемыми, у них в пластинах имеются части «кальция» и «серебра».
Однако, так было не во а все времен, еще в Советском Союзе огромная популярность была у сурьмянистых аккумуляторных батареях, а вот они в свою очередь, как правило шли сухозаряженные («залить» и «зарядить» необходимо было вам самим). Всем владельцам АКБ необходимо знать, что такое этот электролит? Это токопроводящая жидкость, какая под влиянием своего состава на свинцовые пластины может помогать при накапливанию или отдаче электрического тока.
Как раз, почти все жидкости на Земле могут быть электролитом, в той или другой мерой. В частности, обыкновенная вода! К тому же, в человеческой крови, тоже иметься понятие электролита, наши с вами нервные клетки передают импульсы как раз через нее.
СОСТАВ ЭЛЕКТРОЛИТА
Именно, тут нет ничего трудного. Вам необходимо смешать серную кислоту и дистиллированную воду в необходимой пропорции. Стандартная «водопроводная» вода не подойдет, ибо в ней иметься огромное количество различных примесей солей, примесей хлора и другого, все это пагубно влияет на пластины источника питания! Электролит автомобиля имеет необходимую концентрацию, ее отзеркаливает плотность готового состава, как правило она колеблется от 1,23 до 1,29 г/см3. Различные значения контролирует температурные зоны Украины. Так плотность в 1,23 г/см3 применяется в теплых регионах, а 1,29 (и даже больше) в холодных. Не стоит забывать, что если значения плотность мало, то аккумулятор автомобиля элементарно может замерзнуть при кране сильном холоде.
Различные значения контролирует температурные зоны Украины. Так плотность в 1,23 г/см3 применяется в теплых регионах, а 1,29 (и даже больше) в холодных. Не стоит забывать, что если значения плотность мало, то аккумулятор автомобиля элементарно может замерзнуть при кране сильном холоде.
КАК ПРОИЗВЕСТИ СОБСТВЕННОРУЧНО РУКАМИ
Перед тем как начать это, вам необходимо знать, что всякие операции по изготовлению электролита своими руками очень опасны для вашего здоровья! Ибо нам необходимо будет трудиться с серной кислотой в огромных концентрациях. НА вас непременно должны быть одеты защитные средства, для рук, тела, дыхательных путей.
ЧТО БУДЕТ НЕОБХОДИМО:
- Серная кислота плотностью более чем 1,83 г/см3
- Дистиллированная вода
- Фарфоровая посудина
Процесс производства крайне легок, нам необходимо смешать наши ингредиенты в необходимой пропорции. В частности, в процессе изготовления выделяется обильное количество тепла, вследствие этого не стоит применять стеклянные емкости, они элементарно могут лопнуть. Безупречно для этого вам подойдет фарфор, далее, когда температура состава уменьшиться, можно перелить в стеклянную или пластиковую тару.
Безупречно для этого вам подойдет фарфор, далее, когда температура состава уменьшиться, можно перелить в стеклянную или пластиковую тару.
Далее, смешиваем ингредиенты и меряем плотность одержанного состава ареометром, после того как дошли до необходимого показателя — электролит готов.
Как бы там ни было, ареометр есть ни у каждого в гараже! Оттого, тут стоит немного помочь, какое количество и что добавлять. Для плотности электролита:
1,23г/см3 – необходимо в литр дистиллированной воды, долить 280грамм серной кислоты
1,25г/см3 – на 1л. воды 310грамм кислоты
1,27г/см3 – на 1л. – 345грамм
1,29г/см3 – на 1л. – 385гр.
Вот так вот, можно собственноручно приготовить электролит, больше ничего не требуется!
ЭЛЕКТРОЛИТ В ЗАРЯЖЕННЫЙ АВТОМОБИЛЬНЫЙ ИСТОЧНИК ПИТАНИЯ
При разрядах плотность электролита может уменьшаться. Это случается, ибо кислота, объединяясь со свинцом, обосновывается в виде сульфатов на пластинах. Необходимо совершить процесс подзарядки аккумуляторной батареи и сульфаты приниматься распадаться, концентрация возобновляется.
Как бы там ни было, при глубоких разрядах, сульфаты создадут крупные кристаллы, какие тривиально запаковывают пластины, да и плотность критически падает.
ЧИТАЙТЕ ТАКЖЕ
Как правильно добавить дистиллированную воду в аккумулятор
Как правильно добавить дистиллированную воду в аккумулятор При эксплуатации аккумуляторов уровень электролита в банках неизбежно снижается. С не обслуживаемыми АКБ проще уровень жидкости в отсеках практически не меняется на протяжении 5-6 лет. Что касается обслуживаемых аккумуляторов владельцам постоянно приходится контролировать уровень электролита и своевременно принимать меры. В статье расскажем, как долить дистиллированную воду в аккумулятор, сколько ее нужно и можно ли чем-то заменить.Где взять дистиллированную воду для аккумулятора Лет 20 назад у автомобилистов вопросов о приобретении дистиллированной воды не возникало она продавалась практически в каждой аптеке. Сейчас ситуация изменилась. Дело в том, что эта жидкость пригодна для использования в медицинских целях в течение трех суток, поэтому достать ее можно только в аптечном пункте, имеющем свой дистиллятор.
Сейчас ситуация изменилась. Дело в том, что эта жидкость пригодна для использования в медицинских целях в течение трех суток, поэтому достать ее можно только в аптечном пункте, имеющем свой дистиллятор.
Современные альтернативные варианты: магазины авто запчастей автозаправочные станции, имеющие торговую точку; хозяйственные магазины (дистиллированная вода используется в утюгах и отпаривателях). Еще один вариант поиск воды в интернет-магазинах. Подойдет он тем, кто хочет сделать запас впрок. Срок доставки в зависимости от региона может быть несколько недель, для экстренной доливки жидкости в АКБ такой способ не походит. Некоторые автомобилисты не хотят тратить время на посещение магазинов, и задаются вопросом, можно ли заливать в аккумулятор простую или кипяченую воду. Первый вариант не подходит категорически. В воде из-под крана присутствуют посторонние вещества хлор, магний, фосфор и т.д. При зарядке аккумулятора они осядут на свинцовых пластинах. В лучшем случае это приведет к снижению емкости АКБ, в худшем к замыканию и выходу батареи из строя. Что касается кипяченой воды полноценно заменить дистиллированную она не сможет, в ней имеются соли металлов, пусть и в небольшом количестве. Такой вариант подойдет, если нужно срочно привести аккумулятор в боевую готовность, но затем придется промывать каждую банку и заливать новый электролит.
Что касается кипяченой воды полноценно заменить дистиллированную она не сможет, в ней имеются соли металлов, пусть и в небольшом количестве. Такой вариант подойдет, если нужно срочно привести аккумулятор в боевую готовность, но затем придется промывать каждую банку и заливать новый электролит.
Попытка заменить дистиллированную воду кипяченой или какой-либо другой может привести к снижению емкости батареи, разрушению свинцовых пластин и другим неприятным последствиям. Как доливать дистиллированную воду в автомобильный аккумулятор правильно Если в вашем аккумуляторе увеличилась плотность электролита или вы заметили, что он не выдает нужного напряжения скорее всего причина в снижении количества дистиллированной воды. В норме ее должно быть 65 % на 35 % серной кислоты. Последовательность работ при доливке дистиллята в аккумулятор. Чтобы правильно долить жидкость в банки воспользуйтесь инструкцией. Уберите грязь и пыль с верхней части аккумулятора, особенно вокруг пробок. Протрите область вокруг горловин тряпкой, смоченной в содовом растворе, для нейтрализации серной кислоты, которая могла выплеснуться при зарядке. Осторожно открутите пробки берегите руки от воздействия электролита. Возьмите медицинскую спринцовку, шприц или ареометр, наберите дистиллированной воды. Залейте жидкость в банки с недостаточным уровнем электролита. Закрутите пробки. Через 2-3 часа проверьте плотность электролита ареометром (нормальное значение в таблице ниже). Если все сделано правильно поставьте АКБ на зарядку.
Протрите область вокруг горловин тряпкой, смоченной в содовом растворе, для нейтрализации серной кислоты, которая могла выплеснуться при зарядке. Осторожно открутите пробки берегите руки от воздействия электролита. Возьмите медицинскую спринцовку, шприц или ареометр, наберите дистиллированной воды. Залейте жидкость в банки с недостаточным уровнем электролита. Закрутите пробки. Через 2-3 часа проверьте плотность электролита ареометром (нормальное значение в таблице ниже). Если все сделано правильно поставьте АКБ на зарядку.
Доливка дистиллированной воды в аккумулятор должна проводиться на горизонтальной поверхности. В противном случае уровень жидкости в банках будет различный, поэтому вы или перельете воду, или не дольете. Рекомендуемая плотность электролита в аккумуляторе зависит от климатических условий вашего региона. Климатический пояс Плотность электролита (г/см3) 1,25 Средняя полоса 1,27 Север 1,29 Чтобы при измерении плотности электролита результат был точным держите ареометр вертикально, не допускайте касания поплавка его стенок. Набрав электролит в колбу, постепенно снижайте давление, чтобы поплавок свободно плавал. Если вы смогли этого достичь обратите внимание на место соприкосновения жидкости со шкалой. Это и будет плотность электролита в аккумуляторе. Проверьте плотность электролита после добавления дистиллированной воды в АКБ.
Набрав электролит в колбу, постепенно снижайте давление, чтобы поплавок свободно плавал. Если вы смогли этого достичь обратите внимание на место соприкосновения жидкости со шкалой. Это и будет плотность электролита в аккумуляторе. Проверьте плотность электролита после добавления дистиллированной воды в АКБ.
Сколько дистиллированной воды доливать в аккумуляторную батарею В современном аккумуляторе проще всего понять, сколько нужно заливать дистиллированной воды. Его корпус изготовлен из прозрачного пластика с нанесенной на нем шкалой. Достаточно следить, чтобы не был превышен рекомендуемый производителем уровень. В случае, если у вас аккумулятор другого типа, воспользуйтесь следующими советами. В некоторых АКБ чуть ниже горловины банки расположен металлический или пластмассовый язычок. Уровень электролита должен быть выше язычка на 5 мм. Если никаких отметок в банке нет доливайте дистиллированную воду так, чтобы уровень электролита был выше свинцовых пластин на 10-15 мм. Если вы не можете визуально определить, сколько электролита в банке возьмите стеклянную трубку, опустите ее в отсек, зажмите верхнюю часть пальцем и аккуратно извлеките. Количество жидкости в ней будет равным расстоянию от свинцовых пластин до поверхности электролита. Старайтесь соблюдать правила заливки, чтобы добиться верного соотношения соляной кислоты к дистиллированной воде. Если кислоты будет больше она разрушит свинцовые детали аккумулятора, если меньше аккумулятор разморозит при отрицательной температуре. Как получить дистиллированную воду в домашних условиях Некоторые автолюбители предпочитают не покупать дистиллированную воду, а делать ее самостоятельно. Обычно это люди старшего поколения, привыкшие к временам дефицита и не желающие перестраиваться. Но и жителям отдаленных поселков, в которых нет магазинов, приходится приспосабливаться подобным образом. Сразу заметим, что получить качественную дистиллированную воду в домашних условиях невозможно. Для этого нужен дистиллятор, стоимость которого не сопоставима с ценой за бутылку воды.
Если вы не можете визуально определить, сколько электролита в банке возьмите стеклянную трубку, опустите ее в отсек, зажмите верхнюю часть пальцем и аккуратно извлеките. Количество жидкости в ней будет равным расстоянию от свинцовых пластин до поверхности электролита. Старайтесь соблюдать правила заливки, чтобы добиться верного соотношения соляной кислоты к дистиллированной воде. Если кислоты будет больше она разрушит свинцовые детали аккумулятора, если меньше аккумулятор разморозит при отрицательной температуре. Как получить дистиллированную воду в домашних условиях Некоторые автолюбители предпочитают не покупать дистиллированную воду, а делать ее самостоятельно. Обычно это люди старшего поколения, привыкшие к временам дефицита и не желающие перестраиваться. Но и жителям отдаленных поселков, в которых нет магазинов, приходится приспосабливаться подобным образом. Сразу заметим, что получить качественную дистиллированную воду в домашних условиях невозможно. Для этого нужен дистиллятор, стоимость которого не сопоставима с ценой за бутылку воды. В качестве альтернативы можно использовать самогонный аппарат, если вынуть из него змеевик. Но выход дистиллированной воды при таком способе незначительный около стакана за 3-4 часа. Дистиллированная вода имеет формулу h3O, то есть не содержит посторонних примесей. Как бы вы не старались, получить подобный результат дома практически невозможно незначительная часть солей металлов в воде останется.
В качестве альтернативы можно использовать самогонный аппарат, если вынуть из него змеевик. Но выход дистиллированной воды при таком способе незначительный около стакана за 3-4 часа. Дистиллированная вода имеет формулу h3O, то есть не содержит посторонних примесей. Как бы вы не старались, получить подобный результат дома практически невозможно незначительная часть солей металлов в воде останется.
Если вам нужно срочно долить в аккумулятор воду наберите ее в пластмассовую бутылку и уберите в холодильник на 2-3 часа. Затем слейте не замерзшую воду в раковину, а лед растопите и пользуйтесь для заливки в банки. В этом случае ущерб для АКБ будет минимальным. Можно собирать в пластмассовую посуду дождевую воду, затем тщательно фильтровать и использовать по назначению. Важно, чтобы вода не соприкасалась с металлами. Например, та, что стекает с жестяных крыш, для заливки аккумулятора не подойдет. Подведем итоги Теперь вы знаете, как долить дистиллированную воду и при этом не испортить аккумулятор. Рекомендуем приобрести ареометр, чтобы контролировать плотность электролита в банках. Без этого прибора достичь нужной плотности невозможно, а ее изменение может вывести из строя вашу АКБ.
Рекомендуем приобрести ареометр, чтобы контролировать плотность электролита в банках. Без этого прибора достичь нужной плотности невозможно, а ее изменение может вывести из строя вашу АКБ.
Что нельзя делать с аккумулятором летом, чтобы он не «умер» зимой
Когда ваш автомобильный аккумулятор подводит и машина не заводится, это крайне неприятно. Между тем нередко виноват сам водитель, не выполнявший ряд простых правил. Разберемся, какие именно ошибки могут сократить жизнь АКБ даже летом.
Как можно убить аккумулятор быстрее всего
Самый простой путь вывести из строя аккумулятор — это долить в электролит обычную воду — электроды в таком случае выйдут из строя.
Жизнь АКБ может радикально сократить также заряд током чрезмерно большой силы, перегрев электролита и его повышенная плотность, повышенное и пониженное напряжение в бортовой сети автомобиля, загрязнение электролита и короткое замыкание (возможно при неосторожном обращении с инструментом вблизи контактов батареи, или при повреждения изоляции силового кабеля). Однако существуют и менее явные огрехи, которые также вредны для АКБ. Читайте о них ниже.
Однако существуют и менее явные огрехи, которые также вредны для АКБ. Читайте о них ниже.
Не поддерживать чистоту
При эксплуатации автомобиля в особенности в условиях повышенной загрязненности (пыль, песок, пыльца деревьев и т.п.) следует уделять особое внимание чистоте корпуса АКБ. Ведь если грязь просочится в электролит, печальная судьба батареи по сути предрешена.
Загрязнения на корпусе следует регулярно устранять мягкой тряпкой, смоченной в растворе нашатырного спирта или кальцинированной соды.
Используйте зубную щетку или мелкую шкурку, чтобы удалить любые следы коррозии, если вы обнаружите их на клеммах аккумулятора. Лишняя грязь и следы окисления на клеммах провоцируют замыкание и разрядку АКБ. Не забывайте также проверять надежность крепления как самого аккумулятора, так и его клемм.
Игнорировать температурный режим
Не секрет, что аккумуляторы постепенно подсаживаются от скачков температуры в межсезонье и долгого отсутствия нагрузки. При падении плотности электролит замерзает — это вызывая деформации и осыпание пластин, равно как прожоги от коротких замыканий. Поэтому не следует оставлять ваш автомобиль на недели и месяцы на улице в мороз.
Поэтому не следует оставлять ваш автомобиль на недели и месяцы на улице в мороз.
Регулярно заводите ваш автомобиль зимой, а еще лучше — совершайте хотя бы короткие поездки, чтобы батарея могла подзарядиться. Гаражное хранение — идеальный вариант, но даже в этом случае следует замерять тестером уровень заряда АКБ на заглушенном двигателе хотя бы раз в месяц. При полном заряде показания стремятся к значению 12.7 вольт. При почти полной разрядке будет примерно 12 вольт. При нормальной плотности электролита, которая должно составлять 1,27 г/см куб., образование льда начнется только при температуре ниже -65 град.
Перегружать батарею
Прежде всего, не перегружайте сеть. Различные усилители, доп.оборудование и девайсы типа видеорегистратора, радар-детектора и просто несколько подключенных к «мультимедийке» гаджетов — это, конечно, замечательно. Но такая прорва потребителей неизбежно повысит нагрузку на сеть.
Нередки также случаи запредельных разрядов, например, после пуска двигателя стартером. Или, скажем, если вы регулярно даете «прикурить» друзьям и соседям (особенно если потенциал их АКБ больше, чем у вашего), это также не идет на пользу батарее. Кроме того, помогая такому аккумулятору, который уже «дышит на ладан», донор может еще и спалить бортовую электронику.
Или, скажем, если вы регулярно даете «прикурить» друзьям и соседям (особенно если потенциал их АКБ больше, чем у вашего), это также не идет на пользу батарее. Кроме того, помогая такому аккумулятору, который уже «дышит на ладан», донор может еще и спалить бортовую электронику.
Неправильное обслуживание
Если ваш аккумулятор обслуживаемый, то в рамках самостоятельного «ТО» следует долить нужное количество смести дистиллированной воды и электролита (у автомобильных аккумуляторов принято считать нормальным уровень заливки на 10-15 мм выше верхней кромки пластин) и убедиться в том что раствор имеют оптимальную плотность (1.27 г/см3).
Если в АКБ пониженная плотность смеси, то это может привести к быстрому разряду и замерзанию раствора. Если плотность повышенная — тоже плохо: чревато «обезвоживанием», и, как следствие, разъеданием пластин. Плотность состава измеряется специальным прибором — ареометром (денсиметром).
Совет «подснежникам» — отнесите аккумулятор домой зимой
Есть категория водителей, которые по тем или иным причинам не ездят зимой. Для таких людей имеет прямой смысл позаботится об аккумуляторе. АКБ необходимо снять и отнести домой или в теплый гараж. Хранить батарею рекомендуется при комнатной температуре. При этом каждые два — три месяца аккумулятор рекомендуется подзаряжать, предварительно проверяя уровень зарядки с помощью вольтметра.
Для таких людей имеет прямой смысл позаботится об аккумуляторе. АКБ необходимо снять и отнести домой или в теплый гараж. Хранить батарею рекомендуется при комнатной температуре. При этом каждые два — три месяца аккумулятор рекомендуется подзаряжать, предварительно проверяя уровень зарядки с помощью вольтметра.
Как приготовить электролит для аккумулятора
Приготовление электролита для аккумуляторов своими руками
В настоящее время выбор аккумуляторных батарей огромен — в продаже можно найти уже готовые к использованию источники питания, а также сухозаряженные батареи, которые требуют осуществить приготовление электролита и его заливку до начала эксплуатации. Дальнейшее обслуживание аккумуляторов многие часто осуществляют в сервисах. По разным причинам может возникнуть необходимость самостоятельно приготовить раствор. Чтобы это мероприятие увенчалось успехом, следует знать, как сделать электролит в домашних условиях.
Что такое электролит?
Электролит — электропроводящий раствор, содержащий в своём составе дистиллированную воду и серную кислоту, едкий калий или натрий в зависимости от типа источника питания.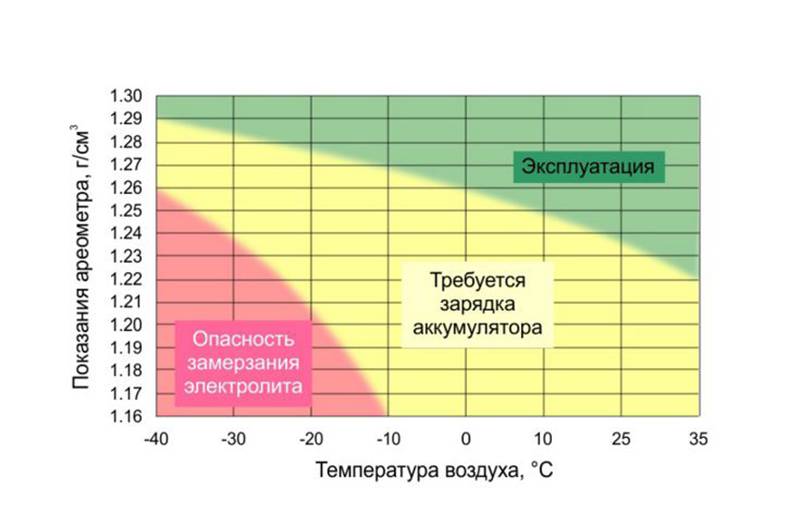
Концентрация серной кислоты в АКБ
Этот показатель кислотности напрямую зависит от необходимой плотности электролита. Изначально средняя концентрация этого раствора в автомобильном аккумуляторе — около 40% в зависимости от температуры и климата, в которых используется источник питания. Во время эксплуатации концентрация кислоты падает до 10–20%, что сказывается на работоспособности АКБ.
Вместе с тем стоит понимать, что аккумуляторная серная составляющая — наичистейшая жидкость, которая на 93% состоит непосредственно из кислоты остальные 7% — примеси. На территории России производство этого химиката строго регламентировано — продукция должна соответствовать требованиям ГОСТ.
Отличия электролитов для разных типов аккумуляторов
Несмотря на то что принцип работы раствора одинаков для разных источников питания, следует знать о некоторых различиях составов. В зависимости от состава принято выделять щелочной и кислотный электролиты.
Щелочные АКБ
Этот вид источников питания характеризуется наличием гидроокиси никеля, окиси бария и графита. Электролит в этом виде аккумуляторов представляет собой 20% раствор едкого калия. Традиционно используется добавка моногидрата лития, которая позволяет продлить срок эксплуатации АКБ.
Электролит в этом виде аккумуляторов представляет собой 20% раствор едкого калия. Традиционно используется добавка моногидрата лития, которая позволяет продлить срок эксплуатации АКБ.
Щелочные источники питания отличаются отсутствием взаимодействия калийного раствора с веществами, образуемыми во время работы аккумулятора, что способствует аксимальному уменьшению расхода.
Кислотные АКБ
Этот вид источников питания является одним из самых традиционных, поэтому и раствор в них знаком многим — смесь дистиллированной воды и серного раствора. Концентрат электролита для свинцово-кислотных аккумуляторов дешёво стоит и характеризуется способностью проводить ток большой величины. Плотность жидкости должна соответствовать климатическим показателям.
Таблица 1. Рекомендуемая плотность электролита
Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?
Отдельно хотелось бы обратить внимание на современные свинцово-кислотные источники питания — гелевые и AGM.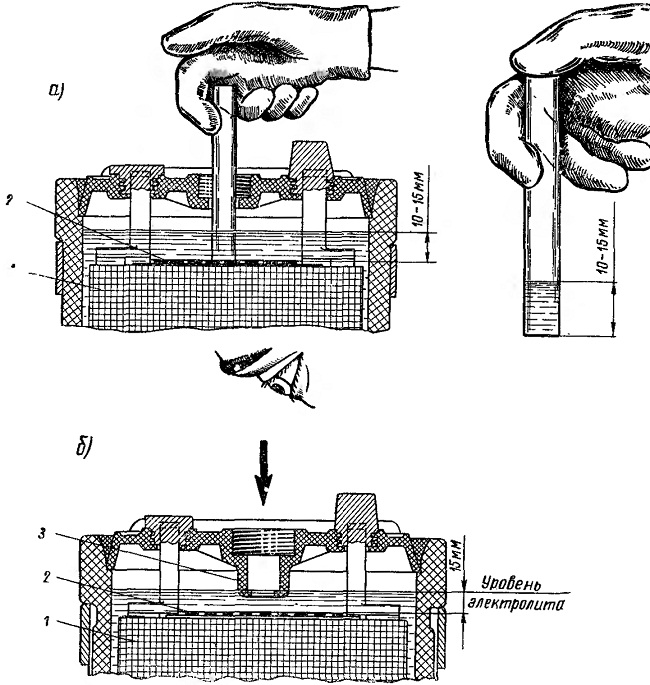 Они также могут быть заправлены собственноручно приготовленным раствором, который в них находится в специфической форме — в виде геля или внутри сепараторов. Для заправки гелевых аккумуляторов понадобится ещё один химический компонент — силикагель, который загустит кислотный раствор.
Они также могут быть заправлены собственноручно приготовленным раствором, который в них находится в специфической форме — в виде геля или внутри сепараторов. Для заправки гелевых аккумуляторов понадобится ещё один химический компонент — силикагель, который загустит кислотный раствор.
Кадмиевоникелевые и железоникелевые аккумуляторы
В отличие от свинцовых источников питания, кадмиево- и железоникелевые заливаются щелочным растовром, который является смесью дистиллированной воды и едкого калия или натрия. Гидроксид лития, входящий в состав этого раствора для определённых температурных режимов, позволяет увеличить срок службы АКБ.
Таблица 2. Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Железоникелевые источники питания рекомендуется эксплуатировать в тех же условиях, что и кадмиево-никелевые. Однако стоит отметить, что они более восприимчивы к низким температурам. Поэтому их следует использовать до минус 20 градусов.
Как правильно приготовить электролит в домашних условиях: техника безопасности
Приготовление раствора — работа с кислотами и щелочами, поэтому соблюдение мер предосторожности необходимо для самых опытных людей. Перед началом действия подготовьте средства защиты:
- резиновые перчатки
- одежду и фартук, устойчивый химическим веществам;
- защитные очки;
- нашатырный спирт, кальцинированную соду или борный раствор, чтобы нейтрализовать кислоту и щёлочь.
Оборудование
Для приготовления аккумуляторного электролита помимо самого источника питания потребуются следующие предметы:
- ёмкость и палочка, устойчивые к воздействию кислот и щелочей;
- дистиллированная вода;
- инструменты для измерения уровня, плотности и температуры раствора;
- аккумуляторная серная жидкость — для кислотной АКБ, твёрдые или жидкие щелочи, литий — для соответствующих видов АКБ, силикагель — для гелевых аккумуляторов.

Последовательность процесса: делаем электролит для кислотно-свинцового источника питания
Перед началом работ ознакомьтесь с информацией, приведённой в таблице 3. Она позволит выбрать необходимый объем жидкостей. В аккумуляторах залито от 2,6 до 3,7 литра кислотного раствора. Мы рекомендуем разводить примерно 4л электролита.
Таблица 3. Пропорции воды и серной кислоты.
- В ёмкость, устойчивую к едким веществам, налейте нужный объем воды.
- Разбавлять воду кислотой следует постепенно.
- По окончании процесса вливания замеряйте плотность получившегося электролита с помощью ареометра.
- Дайте составу отстояться около 12 часов.
Таблица 4. Плотность электролита для разных климатов.
Концентрация кислотного раствора должна соотноситься с минимальной температурой, при которой эксплуатируется аккумулятор. Если жидкость получилась слишком концентрированной, её необходимо разбавить дистиллированной водой.
Смотрите видео, как измерить плотность электролита.
Внимание! Вливать воду в кислоту нельзя! В результате этой химической реакции может возникнуть закипание состава, что приведёт к его расплескиванию и возможности получить кислотные ожоги!
Обращаем ваше внимание, что во время смешивания компонентов выделяется тепло. В подготовленный аккумулятор следует заливать остывший раствор.
Способ развести электролит для щелочного источника питания
Плотность и количество электролита в таких аккумуляторах указана в инструкции по эксплуатации источника питания или на сайте компании-производителя.
Необходимая плотность раствора | Количество твёрдой щелочи равняется количеству электролита, разделенному на |
1,17–1,19 г/см³ | 5 |
1,19–1,21 г/см³ | 3 |
1,25–1,27 г/см³ | 2 |
- Влейте в посуду дистиллированную воду.

- Добавьте щелочь.
- Смешайте раствор, герметично его закройте и дайте настояться в течение 6 часов.
- По истечении времени слейте образовавшийся светлый раствор — электролит готов.
При появлении осадка следует его перемешивать. Если к концу отстаивания он остаётся, слейте электролит так, чтобы осадок не попал в аккумулятор — это приведёт к уменьшению срока его эксплуатации.
Внимание! Во время работ температура щелочного раствора не должна превышать 25 градусов по Цельсию. Если жидкость чрезмерно нагревается, охладите её.
После приведения раствора к комнатной температуре и его заливке в аккумулятор, источник питания необходимо полностью зарядить током, составляющим 10% от ёмкости АКБ (60Ач — 6А).
Как видите, приготовление раствора электролита не такое сложное дело. Главное, следует чётко определиться с необходимым количеством ингредиентов и помнить о безопасности. Вы пробовали развести электролит своими руками? Поделитесь опытом с нашими читателями в комментариях.
Что такое электролит для аккумуляторов и как его приготовить?
Электролит – одна из основных составляющих аккумуляторных батарей, которые дают возможность запуска автомобиля. Он бывает нескольких видов, различающихся по своему составу. Своевременный контроль за количеством и качеством электролита в аккумуляторе позволит избежать преждевременный выход аккумулятора из строя и сэкономить на покупке нового устройства.
Содержание статьи
Виды, состав и особенности
На данный момент различают три вида электролитов для аккумуляторов, для щелочных аккумуляторов — щелочной, а для кислотных — кислотный, но так же выделяют и корректирующий электролит, необходимый при обслуживании батарей.
Как определить кислотный аккумулятор или щелочной? Проще всего это сделать по маркировке корпуса и по материалу, из которого он сделан. Корпус кислотных АКБ всегда изготавливается из специального пластика, тогда как щелочные батареи могут быть сделаны из металла.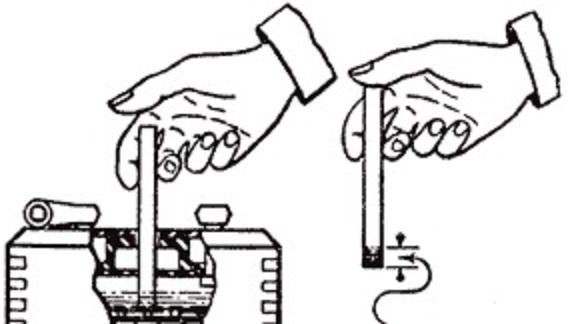 Так же можно определить протестировав каплю электролита из аккумулятора: кислотный электролит вступит в реакцию с содой или мелом.
Так же можно определить протестировав каплю электролита из аккумулятора: кислотный электролит вступит в реакцию с содой или мелом.
Кислотный
Представляет собой смесь серной кислоты, составляющей тридцать пять процентов всего состава, и дистиллированной воды, которая занимает оставшиеся шестьдесят пять. Данный состав в аккумуляторе находится в емкости со свинцовыми пластинами, при контакте этих элементов и происходит выработка тока.
Преимущества кислотного электролита:
- Высокий уровень КПД
- Слабая потеря заряда при бездействии
- Выдача высокого стартового тока
- Невысокая стоимость
Недостатки:
- Чувствительность к перепадам температур
- Неэкологичность
- Необходимость регулярного контроля плотности состава
Следует отметить, что кислотный электролит используется в большинстве моделей аккумуляторных батарей для автомобилей, так как только он способен давать достаточное количество тока для запуска двигателя. При этом аккумуляторы, изготовленные с использованием данного раствора, делятся на две группы:
При этом аккумуляторы, изготовленные с использованием данного раствора, делятся на две группы:
- Обслуживаемые
- Необслуживаемые
Первый вид обеспечивает легкий доступ к содержимому банок. В них можно замерять плотность электролита, при необходимости заливать дистиллированную воду и электролит, просто открутив крышки с банок.
В случае с необслуживаемыми моделями провести подобные действия также возможно, однако для этого нужно самостоятельно вскрыть устройство, провести нужные действия, а затем герметично их закрыть. В подобных случаях могут быть использованы дрель и сварочный аппарат.
Проводить замену электролита в необслуживаемых моделях стоит только в тех случаях, когда их гарантийный срок истек. Часто это производится исключительно для получения опыта проведения подобных операций.
Щелочной
Щелочной электролит состоит из гидроокиси калия, натрия, лития или всех этих составляющих в комплексе, разведенных в воде.
К достоинствам данного вида относятся:
- Длительный период службы
- Способность сохранять свойства при значительных перепадах температуры
- Гораздо меньшее выделение вредных газов в атмосферу
- Способность выдерживать встряски
- Неприхотливость в обслуживании
Недостатки:
- Меньшая величина электродвижущей силы по сравнению с кислотными
- Отсутствие способности подачи стартового тока для запуска двигателя
- Более высокая стоимость
Несмотря на долгий срок службы, неприхотливость и другие преимущества применение данного вида электролита в автомобильной промышленности ограничено. Виной тому неспособность выработки достаточного уровня стартового тока, необходимого для запуска двигателя. К минусам также относятся их внушительные габариты.
Однако устройства на щелочном электролите успешно применяются в обеспечении током тяговых и локомотивных составов.
Важно! Перед осуществлением замены следует убедиться, что аккумулятор именно щелочной.
В противном случае АКБ можно полностью вывести из строя.
Корректирующий
Данный электролит является специальным составом с высоким содержанием активных веществ, используемый для повышения плотности электролита аккумулятора. Он предназначен для повышения концентрации активных веществ в батарее.
В продаже можно встретить следующие виды корректирующего электролита:
- Твердый калиево-литиевый
- Жидкий калиево-литиевый с различной плотностью
- Жидкий кислотный
Корректирующий электролит можно изготовить самостоятельно, имея под рукой необходимые для этого составы, однако зачастую его проще купить, так как стоимость его более чем доступна.
Как пользоваться корректирующим электролитом:
- Удалить из банок немного электролита
- Долить в них такое же количество корректирующей жидкости
- Установить АКБ на заряд номинальным током для запуска процесса смешивания полученного состава на полчаса
- Оставить батарею на остывание на пару часов
- Произвести замер плотности и при необходимости отрегулировать его снова
При повторной коррекции количество заменяемого электролита следует уменьшить.
Как приготовить самостоятельно
Перед тем, как самостоятельно заменить электролит для аккумулятора, необходимо принять соответствующие меры безопасности и приготовить предметы индивидуальной защиты:
- Перчатки
- Фартук
- Защитные очки
- Раствор соды на случай попадания средства на кожу или предметы одежды
- Уксус или лимонную кислоту – для нейтрализации щелочи
Проводить действия следует в хорошо проветриваемом помещении с температурой воздуха не выше +25 C°. Следует заранее знать, какой объем готового электролита потребуется для заполнения батарей. В среднем, в современных АКБ количество раствора составляет от 2,6 до 3,7 литра. Поэтому стоит сразу ориентироваться на максимальное количество. За основу можно взять 4 литра конечного раствора.
Для приготовления электролита необходимо заранее приготовить следующие предметы:
- Посуду достаточной емкости, изготовленную из материала, устойчивого к воздействию кислоты и щелочи
- Небольшую палочку для перемешивания электролита
- Инструменты для проведения замеров плотности, температуры и уровня раствора
- Для кислотного электролита – серную жидкость, для щелочного – щелочь в твердом или жидком виде, литий или силикагель
Важно! Все используемые материалы должны быть химически нейтральными для исключения возникновения ненужных реакций при их соприкосновении. В качестве емкости вполне подойдут обычные стеклянные банки.
Процесс приготовления щелочного электролита
Ингредиенты для приготовления данного состава могут быть как в жидком виде, так и в твердом. Если с первым все понятно, то перед тем как залить, щелочной электролит из твердого вещества потребуется развести в дистиллированной воде.
Требуемая плотность указывается на сайте производителя аккумулятора, также информацию можно найти в прилагаемой инструкции по эксплуатации. Твердый электролит берется пропорционально нужному количеству окончательного жидкого раствора и составляет:
- 1/5 – для получения раствора плотностью 1,17-1,19 г/м³
- 1/3 – для раствора плотностью 1,19-1,21 г/м³
- 1/2 — для раствора плотностью 1,25-1,27 г/м³
Процесс приготовления состоит из следующих шагов:
- Налить в посуду дистиллированную воду
- Добавить нужное количество щелочи
- Перемешать раствор
- Плотно закрыть крышкой
- Настаивать в течение 6 часов
После того, как процесс настаивания будет завершен, необходимо слить светлый раствор. Если часть состава выпадает в осадок, нужно его регулярно перемешивать. При заливке нужно следить, чтобы он остался на дне, не попав в аккумулятор, в противном случае это грозит выходом АКБ из строя.
Приготовление раствора
для свинцовых аккумуляторовПеред тем, как разбавить кислотный электролит, необходимо определить нужные пропорции. Они зависят от климатических условий, в которых планируется эксплуатация устройства.
Для получения электролита плотностью 1,28 г/м³, что приемлемо для средних климатических условий, потребуется в один литр дистиллированной воды влить 0,36 л серной кислоты. Для жарких регионов количество серной кислоты уменьшается до 0,33 л на то же количество воды.
Как разводить аккумуляторную кислоту:
- Налить в подготовленную емкость дистиллированную воду
- Аккуратно тонкой струйкой влить в нее кислоту
- Измерить плотность полученного раствора
- Оставить раствор настаиваться на 12 часов
Важно! Нельзя вливать воду в кислоту! Правильно — вливать кислоту в воду. Не следует торопиться, вливая кислоту, давайте возможность ей постепенно раствориться в воде.
Инструкция по замене
Замена электролита производится в следующих случаях:
- Электролит в банках изменил цвет, стал мутным. Причиной тому может быть использование не дистиллированной воды для добавки, а обычно. Она может содержать примеси, вступающие в химическую реакцию с электролитом и образовывая твердые соединения, выпадающие в осадок
- После зарядки аккумулятора невозможно добиться нужной плотности
- Электролит вытек по неосторожности
- Новый аккумулятор быстро разряжается. Причиной тому может быть замерзание раствора
Замена электролита, независимо от того, является он щелочным или кислотным, производится в несколько шагов:
- Демонтаж аккумулятора из транспортного средства
- Очистка АКБ от загрязнений
- Выкачивание имеющейся жидкости с помощью груши или шприца
- Промывка банок дистиллированной водой
- Заливка электролита с помощью груши или аналогичных приспособлений
Уровень заливки определяется метками внутри банок. Если они отсутствуют, нужно руководствоваться правилом – электролит должен быть на уровне выше пластин на 5-7 миллиметров. При этом от его уровня до крышек банок должно оставаться не менее двух сантиметров.
Очень важно при сливе электролита не наклонять его в сторону и тем более не переворачивать. На дне сосудов могут оказаться твердые частицы, которые застрянут в пластинах, полностью выведя их из строя. Допускается легкое покачивание воды из стороны в сторону при промывании, такие же действия можно производить после заливки электролита в аккумулятор.
После этого АКБ устанавливается на зарядку, после чего следует проверить получившуюся плотность. Замеры должны производиться не арене, чем через пару часов после снятия устройства с зарядки, так как существует риск получить завышенные показания. Если плотность недостаточно высокая или, напротив, имеет излишние значения, ее следует отрегулировать добавлением кислоты, щелочи или дистиллированной воды.
Полезное видео
Видео инструкция о замене электролита
Заключение
Независимо от типа электролита, используемого в эксплуатируемой АКБ, можно самостоятельно произвести его полную замену, проверку плотности и других показателей. Однако стоит помнить о технике безопасности, так как электролит – опасный химический состав, способный значительно повредить кожные покровы и глаза.
Змена электролита в аккумуляторе и как приготовить пропорцию
Электролит является химическим раствором, и состоит из серной кислоты и дистиллированной воды. Состав способствует протеканию химических реакций между положительно и отрицательно заряженными свинцовыми пластинами в аккумуляторной батарее. При нормальных условиях эксплуатации АКБ требуется проводить только контроль уровня электролита и оценивать его плотность (около 1,27 г/см3).
В случае отдельных сбоев – понижение уровня, выкипание, несвоевременное обслуживание возможно изменение уровня и состояния химического раствора. Это значительно снижает срок эффективного использования АКБ, приводит к возникновению нештатных ситуаций.
Когда нужно доливать электролит в аккумулятор и как это делается
Следует учитывать, что замена электролита в АКБ не является частым процессом. В основном пользователи ограничиваются контролем уровня и состояния жидкости. Для понимания причин снижения плотности раствора следует вспомнить принцип работы электрохимической машины.
В процессе эксплуатации АКБ наиболее частой неисправностью является потеря электролитом плотности. После передачи батареей части энергии при запуске двигателя, питания других потребителей происходит последующая подзарядка. Ток поступает от генератора, или допустимо использовать внешний источник энергии. В случае недостаточного заряда возникает такой процесс, как сульфатация пластин. При разряде АКБ оксид свинца образуется в ускоренном режиме. В результате необходимые вещества изымаются из окружающего вещества, с учетом того, из чего состоит электролит для аккумуляторов. Как следствие – его плотность понижается.
Любой владелец авто без труда в состоянии при помощи ареометра проверить плотность раствора. Процесс намного более простой, чем замена электролита. При пониженном значении следует соотношение кислоты и воды за счет добавления раствора с начальным более высоким значением.
Для корректной оценки измерение плотности проводят на начально заряженной батарее. Возможны два варианта развития событий:
- Плотность находится в допустимых значениях – 1,25-1,27 г/см3. При малом уровне в отдельных банках следует только доливать дистиллированную воду в батарею.
- Плотность пониженная – значение от 1,20-1,25 г/см3 и ниже. Добавляют раствор с более высокой концентрацией (около 1,34 единиц).
Для повышения плотности применяют принцип замещения. Из банки с низкой плотностью грушей откачивают раствор из области над поверхностью пластин. На освободившееся место доливают раствор большей плотностью. Проводят последующий замер показателя плотности после отстоя источника тока в течение нескольких часов. После доливки уровень жидкости должен быть не выше меток, а если они отсутствуют – превышать на 5–7 мм верхнюю кромку свинцовых пластин.
Как поменять электролит в аккумуляторе автомобиля и когда это нужно
При контрольном осмотре могут быть обнаружены признаки, указывающие на то, что потребуется полная замена электролита:
1. Замутнение раствора, частичное изменение цвета. Для оценки состояния жидкости следует часть ее извлечь из каждой секции.
2. После частичной замены не удается добиться нужной плотности.
3. Раствор подвергался полной заморозке. К примеру, при плотности около 1,10 г/см3 (глубокий разряд) заморозка произойдет при 7–8 градусах мороза.
Кислотный состав нормальной плотности выдержит отрицательную температуру на уровне ниже -54 °С.
Полная замена электролита в аккумуляторе начинается с извлечения прежнего раствора. Ни в коем случае не следует сливать жидкость из банок путем наклона батареи. Стоит помнить, из чего состоит АКБ. Свинцовый осадок со дна с легкостью закоротит разно полярные пластины, попав между ними.
До начала замены электролита в автомобильном аккумуляторе следует приготовить подручные инструменты: емкость для старой жидкости, воронку, приспособления для откачки жидкости.
Поменять электролит легче, постепенно отсасывая грушей или шприцом прежний раствор из каждой секции. Предварительно корпус аккумулятора очищают от загрязнений. После откачки для замены электролита в АКБ выполняют последовательные действия:
- проводят промывку внутренней полости, заливая дистиллированную воду до необходимого уровня;
- заливают свежий раствор плотностью 1,27 единиц.
Для обретения второй жизни заменить электролит в аккумуляторе автомобиля недостаточно. Потребуется зарядка устройства с соблюдением режима.
После замены электролита сколько нужно заряжать аккумулятор
Прежде чем заряжать аккумулятор после замены электролита, дайте отстояться АКБ несколько часов. Разрешено покачать корпус с целью удаления пузырьков воздуха.
Режим зарядки АКБ предполагает использование малых зарядных токов – 0,1А. Процесс проводят по циклу – заряд-разряд, контролируя плотность. Не следует допускать излишнего кипячения раствора с учетом возможной потери концентрации воды.
При обнаружении излишней сульфатации свинцовых пластин допускается использовать присадку для растворения налета. На качество нового раствора этот процесс не повлияет. Время полного растворения оксида составляет около 2 суток.
Окончательный замер плотности и степени зарядки проводится не ранее чем через два часа после отключения батареи от зарядного устройства. При контроле тестером на полную зарядку укажет напряжение на клеммах на уровне 14–15 В. Но процесс следует продолжить в течение еще двух часов, чтобы убедиться на стабильность показателя плотности.
Как приготовить электролит для аккумулятора
Если с вопросом как заменить электролит в аккумуляторе все становится ясно, то остается приготовить химический раствор. На сегодняшний день приготовление электролита не является острой необходимостью. Кислотный состав плотностью 1,27 г/см3 доступен в свободной продаже.
В зависимости от размеров и электрической емкости батареи будет отличаться объем приготавливаемой жидкости. Для большинства легковых моделей не понадобится жидкости более 2,6-3,7 литра. Стоит заранее высчитать объем необходимых ингредиентов с учетом конечного объема с запасом — около 4 литров.
Теоретически, приготовление электролита для аккумуляторов плотностью 1,28 единиц включает в себя следующие пропорции:
- дистиллированная вода – 1 л;
- серная кислота – 0,33 л.
При смешивании важно помнить, как правильно вливать компоненты – в воду льют кислоту. Перемешивать не нужно, при постепенном добавлении процесс успешно протекает самостоятельно. По окончании приготовления раствора оставляют его на 12 часов, по истечении которых проводят замер плотности.
В случае самостоятельного приготовления следует учитывать, что серная кислота должна иметь отличную степень чистоты, что требуется стандартом. Допустимое содержание примесей – не более 7%.
Использование h4SO4 неизвестного происхождения не позволит заменить электролит в аккумуляторе автомобиля с успехом.
В случае использования щелочного аккумулятора процесс замены рабочей среды несколько отличается. Для приготовления щелочного электролита используют готовый сухой щелочной электролит – обычно Натрий-Литиевый. Этот состав смешивают в нужной пропорции с дистиллированной водой.
К примеру, для традиционной концентрации 1,27 г/см3 используют соотношение сухая смесь/готовый раствор как 1 к 2 частям. Более подробно следует прочитать инструкцию к смеси, а также изучить рекомендации производителя отдельной модели источника тока.
Следует внимательно отнестись к утилизации старого состава. Не экологично сливать его просто в канализацию или землю. Обратитесь в специальные службы по сбору кислоты.Проведенная работа не потребует значительных финансовых и временных затрат. В ответ владелец авто получит надежный запуск двигателя в любой сезон года.
Видео про замену электролита в аккумуляторе
Как приготовить электролит
Электролит можно приготовить только из дистиллированной воды и аккумуляторной серной кислоты.
Инструменты и материалы:
- электролит
- аккумуляторная батарея
- эбонитовая палочка
- сосуд, устойчивый к действие серной кислоты (керамический, эбонитовый, свинцовый) емкостью около 5 л.
Процесс:
1. Возьмите емкость, устойчивую к действию серной кислоты, залейте туда дистиллированную воду.
2. Затем в заполненную дистиллированной водой емкость, маленькими порциями влейте серную кислоту, помешивая эбонитовой палочкой.
3. Ни в коем случае не вливайте воду в серную кислоту, т.к. электролит будет разбрызгиваться с выделение большого количества тепла и в результате чего вы можете получить серьезные ожоги.
4. Электролит готовится исходя из климатических условий местности. Для районов с умеренным климатом плотность электролиты должна быть — 1,28 г/см, т.е. для его изготовления вам нужно смешать компоненты в пропорции 0,36 л серной кислоты на 1 л дистиллированной воды.
5. В теплых районах плотность электролита должна составлять 1,26 г/см, для подготовки берут 0,33 л серной кислоты и 1 литр дистиллированной воды.
6. Готовый электролит оставьте на 15–20 часов в закрытой емкости для его остывания, и чтобы произошло выпадение осадка на дно емкости.
кислотный, щелочной, корректирующий, состав и пропорции, как правильно приготовить и залить
Электролит – одна из основных составляющих аккумуляторных батарей, которые дают возможность запуска автомобиля. Он бывает нескольких видов, различающихся по своему составу. Своевременный контроль за количеством и качеством электролита в аккумуляторе позволит избежать преждевременный выход аккумулятора из строя и сэкономить на покупке нового устройства.
Виды, состав и особенности
На данный момент различают три вида электролитов для аккумуляторов, для щелочных аккумуляторов — щелочной, а для кислотных — кислотный, но так же выделяют и корректирующий электролит, необходимый при обслуживании батарей.
Как определить кислотный аккумулятор или щелочной? Проще всего это сделать по маркировке корпуса и по материалу, из которого он сделан. Корпус кислотных АКБ всегда изготавливается из специального пластика, тогда как щелочные батареи могут быть сделаны из металла. Так же можно определить протестировав каплю электролита из аккумулятора: кислотный электролит вступит в реакцию с содой или мелом.
Кислотный
Представляет собой смесь серной кислоты, составляющей тридцать пять процентов всего состава, и дистиллированной воды, которая занимает оставшиеся шестьдесят пять. Данный состав в аккумуляторе находится в емкости со свинцовыми пластинами, при контакте этих элементов и происходит выработка тока.
Преимущества кислотного электролита:
- Высокий уровень КПД
- Слабая потеря заряда при бездействии
- Выдача высокого стартового тока
- Невысокая стоимость
Недостатки:
- Чувствительность к перепадам температур
- Неэкологичность
- Необходимость регулярного контроля плотности состава
Следует отметить, что кислотный электролит используется в большинстве моделей аккумуляторных батарей для автомобилей, так как только он способен давать достаточное количество тока для запуска двигателя. При этом аккумуляторы, изготовленные с использованием данного раствора, делятся на две группы:
- Обслуживаемые
- Необслуживаемые
Первый вид обеспечивает легкий доступ к содержимому банок. В них можно замерять плотность электролита, при необходимости заливать дистиллированную воду и электролит, просто открутив крышки с банок.
В случае с необслуживаемыми моделями провести подобные действия также возможно, однако для этого нужно самостоятельно вскрыть устройство, провести нужные действия, а затем герметично их закрыть. В подобных случаях могут быть использованы дрель и сварочный аппарат.
Проводить замену электролита в необслуживаемых моделях стоит только в тех случаях, когда их гарантийный срок истек. Часто это производится исключительно для получения опыта проведения подобных операций.
Щелочной
Щелочной электролит состоит из гидроокиси калия, натрия, лития или всех этих составляющих в комплексе, разведенных в воде.
К достоинствам данного вида относятся:
- Длительный период службы
- Способность сохранять свойства при значительных перепадах температуры
- Гораздо меньшее выделение вредных газов в атмосферу
- Способность выдерживать встряски
- Неприхотливость в обслуживании
Недостатки:
- Меньшая величина электродвижущей силы по сравнению с кислотными
- Отсутствие способности подачи стартового тока для запуска двигателя
- Более высокая стоимость
Несмотря на долгий срок службы, неприхотливость и другие преимущества применение данного вида электролита в автомобильной промышленности ограничено. Виной тому неспособность выработки достаточного уровня стартового тока, необходимого для запуска двигателя. К минусам также относятся их внушительные габариты.
Однако устройства на щелочном электролите успешно применяются в обеспечении током тяговых и локомотивных составов.
Важно! Перед осуществлением замены следует убедиться, что аккумулятор именно щелочной. В противном случае АКБ можно полностью вывести из строя.
Корректирующий
Данный электролит является специальным составом с высоким содержанием активных веществ, используемый для повышения плотности электролита аккумулятора. Он предназначен для повышения концентрации активных веществ в батарее.
В продаже можно встретить следующие виды корректирующего электролита:
- Твердый калиево-литиевый
- Жидкий калиево-литиевый с различной плотностью
- Жидкий кислотный
Корректирующий электролит можно изготовить самостоятельно, имея под рукой необходимые для этого составы, однако зачастую его проще купить, так как стоимость его более чем доступна.
Как пользоваться корректирующим электролитом:
- Удалить из банок немного электролита
- Долить в них такое же количество корректирующей жидкости
- Установить АКБ на заряд номинальным током для запуска процесса смешивания полученного состава на полчаса
- Оставить батарею на остывание на пару часов
- Произвести замер плотности и при необходимости отрегулировать его снова
При повторной коррекции количество заменяемого электролита следует уменьшить.
Как приготовить самостоятельно
Перед тем, как самостоятельно заменить электролит для аккумулятора, необходимо принять соответствующие меры безопасности и приготовить предметы индивидуальной защиты:
- Перчатки
- Фартук
- Защитные очки
- Раствор соды на случай попадания средства на кожу или предметы одежды
- Уксус или лимонную кислоту – для нейтрализации щелочи
Проводить действия следует в хорошо проветриваемом помещении с температурой воздуха не выше +25 C°. Следует заранее знать, какой объем готового электролита потребуется для заполнения батарей. В среднем, в современных АКБ количество раствора составляет от 2,6 до 3,7 литра. Поэтому стоит сразу ориентироваться на максимальное количество. За основу можно взять 4 литра конечного раствора.
Для приготовления электролита необходимо заранее приготовить следующие предметы:
- Посуду достаточной емкости, изготовленную из материала, устойчивого к воздействию кислоты и щелочи
- Небольшую палочку для перемешивания электролита
- Инструменты для проведения замеров плотности, температуры и уровня раствора
- Для кислотного электролита – серную жидкость, для щелочного – щелочь в твердом или жидком виде, литий или силикагель
Важно! Все используемые материалы должны быть химически нейтральными для исключения возникновения ненужных реакций при их соприкосновении. В качестве емкости вполне подойдут обычные стеклянные банки.
Процесс приготовления щелочного электролита
Ингредиенты для приготовления данного состава могут быть как в жидком виде, так и в твердом. Если с первым все понятно, то перед тем как залить, щелочной электролит из твердого вещества потребуется развести в дистиллированной воде.
Требуемая плотность указывается на сайте производителя аккумулятора, также информацию можно найти в прилагаемой инструкции по эксплуатации. Твердый электролит берется пропорционально нужному количеству окончательного жидкого раствора и составляет:
- 1/5 – для получения раствора плотностью 1,17-1,19 г/м³
- 1/3 – для раствора плотностью 1,19-1,21 г/м³
- 1/2 — для раствора плотностью 1,25-1,27 г/м³
Процесс приготовления состоит из следующих шагов:
- Налить в посуду дистиллированную воду
- Добавить нужное количество щелочи
- Перемешать раствор
- Плотно закрыть крышкой
- Настаивать в течение 6 часов
После того, как процесс настаивания будет завершен, необходимо слить светлый раствор. Если часть состава выпадает в осадок, нужно его регулярно перемешивать. При заливке нужно следить, чтобы он остался на дне, не попав в аккумулятор, в противном случае это грозит выходом АКБ из строя.
Приготовление раствора
для свинцовых аккумуляторовПеред тем, как разбавить кислотный электролит, необходимо определить нужные пропорции. Они зависят от климатических условий, в которых планируется эксплуатация устройства.
Для получения электролита плотностью 1,28 г/м³, что приемлемо для средних климатических условий, потребуется в один литр дистиллированной воды влить 0,36 л серной кислоты. Для жарких регионов количество серной кислоты уменьшается до 0,33 л на то же количество воды.
Как разводить аккумуляторную кислоту:
- Налить в подготовленную емкость дистиллированную воду
- Аккуратно тонкой струйкой влить в нее кислоту
- Измерить плотность полученного раствора
- Оставить раствор настаиваться на 12 часов
Важно! Нельзя вливать воду в кислоту! Правильно — вливать кислоту в воду. Не следует торопиться, вливая кислоту, давайте возможность ей постепенно раствориться в воде.
Инструкция по замене
Замена электролита производится в следующих случаях:
- Электролит в банках изменил цвет, стал мутным. Причиной тому может быть использование не дистиллированной воды для добавки, а обычно. Она может содержать примеси, вступающие в химическую реакцию с электролитом и образовывая твердые соединения, выпадающие в осадок
- После зарядки аккумулятора невозможно добиться нужной плотности
- Электролит вытек по неосторожности
- Новый аккумулятор быстро разряжается. Причиной тому может быть замерзание раствора
Замена электролита, независимо от того, является он щелочным или кислотным, производится в несколько шагов:
- Демонтаж аккумулятора из транспортного средства
- Очистка АКБ от загрязнений
- Выкачивание имеющейся жидкости с помощью груши или шприца
- Промывка банок дистиллированной водой
- Заливка электролита с помощью груши или аналогичных приспособлений
Уровень заливки определяется метками внутри банок. Если они отсутствуют, нужно руководствоваться правилом – электролит должен быть на уровне выше пластин на 5-7 миллиметров. При этом от его уровня до крышек банок должно оставаться не менее двух сантиметров.
Очень важно при сливе электролита не наклонять его в сторону и тем более не переворачивать. На дне сосудов могут оказаться твердые частицы, которые застрянут в пластинах, полностью выведя их из строя. Допускается легкое покачивание воды из стороны в сторону при промывании, такие же действия можно производить после заливки электролита в аккумулятор.
После этого АКБ устанавливается на зарядку, после чего следует проверить получившуюся плотность. Замеры должны производиться не арене, чем через пару часов после снятия устройства с зарядки, так как существует риск получить завышенные показания. Если плотность недостаточно высокая или, напротив, имеет излишние значения, ее следует отрегулировать добавлением кислоты, щелочи или дистиллированной воды.
Полезное видео
Видео инструкция о замене электролита
Заключение
Независимо от типа электролита, используемого в эксплуатируемой АКБ, можно самостоятельно произвести его полную замену, проверку плотности и других показателей. Однако стоит помнить о технике безопасности, так как электролит – опасный химический состав, способный значительно повредить кожные покровы и глаза.
Вконтакте
Google+
Приготовление электролита для аккумуляторных батарей
Какова зависимость плотности электролита от климатической зоны?
Электролит приготовляется путём разведения аккумуляторной серной кислотыплотностью 1,83-1,84 г/см3 (ГОСТ 667–73) в дистиллированной воде с допустимыми примесями.
Химическая чистота электролита оказывает существенное влияние наработоспособность и срок службы батарей. Загрязнение электролита такими вредными примесями, как железо, марганец, хлор и другие, приводит к повышенному саморазряду батарей, снижению отдаваемой ёмкости, разрушению электродов ипреждевременному выходу батареи из строя. Поэтому для приготовления электролита запрещается применять техническую серную кислоту и загрязненную (недистиллированную) воду. При приготовлении электролита, приведении батарей в рабочее состояние и техническом обслуживании батарей в процессе эксплуатациинеобходимо пользоваться только специальной посудой (стойкой к действию серной кислоты) и соблюдать чистоту.
В исключительных случаях при отсутствии дистиллированной воды для приготовления электролита допускается использование снеговой или дождевой воды, предварительно профильтрованной через чистое полотно для очистки от механических загрязнений. Нельзя собирать воду с железных крыш и в железные сосуды.
Электролит следует готовить в стойкой к действию серной кислоты посуде (эбонитовой, фаянсовой, керамической и т.п.), соблюдая при этом особую осторожность и правила техники безопасности. Применение железной, медной или цинковой посуды категорически запрещается!
Аккумуляторные батареи в зависимости от климатической зоны заливаются электролитом, имеющим плотность, указанную в графе 4 таблицы №1: «Плотность электролита при приведении аккумуляторных батарей в рабочее состояние с учётом климатических зон». Электролит требуемой плотности может быть приготовлен непосредственно из кислоты плотностью 1,83-1,84 г/см3 и дистиллированной воды. Однако при непрерывном вливании кислоты в воду происходит сильный разогрев раствора (80-90°C) и требуется длительное время для его остывания. Поэтому для приготовления электролита требуемой плотности более удобно применять раствор кислоты промежуточной плотности 1,40 г/см3, так как в этом случае значительносокращается время охлаждения электролита.
Раствор серной кислоты плотностью 1,40 г/см3, приведённой к 25°C, должен готовиться заранее и после охлаждения храниться в стеклянной или полиэтиленовой посуде.
Количество воды, кислоты или её раствора плотностью 1,40 г/см3, необходимое для приготовления 1 л электролита, указано в таблице №2: «Количество дистиллированной воды, кислоты или её раствора плотностью 1,40 г/см3, необходимое для приготовления 1 л электролита требуемой плотности при температуре 25°C».
Таблица №1:
Плотность электролита при приведении аккумуляторных батарей
в рабочее состояние с учётом климатических зон
| Климатические зоны и районы | Средняя месячная температура воздуха в январе, °C | Время года | Плотность электролита, приведённая к 25°C, г/см3 | |
| заливаемого | полностью заряженной батареи | |||
| 1 | 2 | 3 | 4 | 5 |
| очень холодная | от –50 до –30 | зима | 1,28 | 1,30 |
| лето | 1,24 | 1,26 | ||
| холодная | от –30 до –15 | круглый год | 1,26 | 1,28 |
| умеренная | от –15 до –4 | круглый год | 1,24 | 1,26 |
| тёплая и влажная | от +4 до + 6 | круглый год | 1,20 | 1,22 |
| жаркая | от –15 до +4 | круглый год | 1,22 | 1,24 |
Расчёт проводится в такой последовательности: определяется общий объём электролита для заливки нужного числа батарей, затем подсчитывается количество дистиллированной воды и раствора кислоты плотностью 1,40 г/см3, нужное для приготовления электролита заданной плотности для заливки всех батарей.
Таблица №2:
Количество дистиллированной воды, кислоты или её раствора
плотностью 1,40 г/см3, необходимое для приготовления 1 л электролита
требуемой плотности при температуре 25°C
| Требуемая плотность электролита, г/см3 | Количество воды, л | Количество серной кислоты плотностью 1,83 г/см3 | Количество воды, л | Количество раствора серной кислоты плотностью 1,40 г/см3, л |
|
| л | кг | ||||
| 1,20 | 0,859 | 0,200 | 0,365 | 0,547 | 0,476 |
| 1,21 | 0,849 | 0,211 | 0,385 | 0,519 | 0,500 |
| 1,22 | 0,839 | 0,221 | 0,405 | 0,491 | 0,524 |
| 1,23 | 0,829 | 0,231 | 0,424 | 0,465 | 0,549 |
| 1,24 | 0,819 | 0,242 | 0,444 | 0,438 | 0,572 |
| 1,25 | 0,809 | 0,253 | 0,464 | 0,410 | 0,601 |
| 1,26 | 0,800 | 0,263 | 0,484 | 0,382 | 0,624 |
| 1,27 | 0,791 | 0,274 | 0,503 | 0,357 | 0,652 |
| 1,28 | 0,781 | 0,285 | 0,523 | 0,329 | 0,679 |
| 1,29 | 0,772 | 0,295 | 0,541 | 0,302 | 0,705 |
| 1,31 | 0,749 | 0,319 | 0,585 | 0,246 | 0,760 |
1). Если требуется приготовить электролита больше или меньше одного литра, необходимо взять количество воды и кислоты или раствора, кратное или долевое к указанному в таблице. Например, для приготовления 5 л электролита количество воды и кислоты, приведённое в таблице, нужно умножить на 5, а для приготовления 0,5 л – умножить на 0,5.
2). Аккумуляторная серная кислота учитывается на складах и выдаётся потребителям не в литрах, а в килограммах, поэтому при составлении заявки и получении кислоты со склада надо знать потребное её количество в килограммах. Можно также определить нужное количество кислоты в килограммах, умножив рассчитанное её количество в литрах на 1,83.
При возникновении сомнений относительно температуры замерзания электролита обратитесь к таблице №3
Таблица №3:
Температура замерзания электролита
| Плотность электролита при 25°C, г/см3 |
Температура замерзания, °C |
Плотность электролита при 25°C, г/см3 |
Температура замерзания, °C |
| 1,09 | –7 | 1,22 | –40 |
| 1,10 | –8 | 1,23 | –42 |
| 1,11 | –9 | 1,24 | –50 |
| 1,12 | –10 | 1,25 | –54 |
| 1,13 | –12 | 1,26 | –58 |
| 1,14 | –14 | 1,27 | –68 |
| 1,15 | –16 | 1,28 | –74 |
| 1,16 | –18 | 1,29 | –68 |
| 1,17 | –20 | 1,30 | –66 |
| 1,18 | –22 | 1,31 | –64 |
| 1,19 | –25 | 1,32 | –57 |
| 1,20 | –28 | 1,33 | –54 |
| 1,21 | –34 | 1,40 | –37 |
Заливка батарей электролитом
Температура электролита, заливаемого в аккумуляторные батареи, должна быть не выше 30°C и не ниже 15°C. Непосредственно перед заливкой электролита вывёртывают вентиляционные пробки и удаляют детали или элементы пробки, герметизирующие вентиляционные отверстия. Если в горловине под пробкой имеется герметизирующий диск, его необходимо удалить. Затем постепенно, небольшой струёй заливают электролит до тех пор, пока поверхность электролита не коснётся нижнего торца тубуса горловины крышки.
Завышенная плотность электролита приводит к снижению срока службы аккумулятора.Заниженная плотность электролита приводит к снижению ЭДС и затруднению пуска двигателя, а также к повышению опасности замерзания электролита в зимний период эксплуатации.
Как работает аккумулятор — Любопытно
Представьте себе мир без батарей. Все те портативные устройства, от которых мы так зависим, были бы настолько ограничены! Мы сможем доставить наши ноутбуки и телефоны так, чтобы их кабели были доступны только для того, чтобы сделать это новое работающее приложение, которое вы только что загрузили на свой телефон, практически бесполезным.
К счастью, батарейки у нас есть. Еще в 150 г. до н.э. в Месопотамии парфянская культура использовала устройство, известное как багдадская батарея, сделанное из медных и железных электродов с уксусом или лимонной кислотой.Археологи считают, что на самом деле это не батареи, а в основном они использовались для религиозных церемоний.
Изобретение батареи в том виде, в котором мы ее знаем, приписывают итальянскому ученому Алессандро Вольта, который собрал первую батарею, чтобы доказать свою точку зрения другому итальянскому ученому Луиджи Гальвани. В 1780 году Гальвани показал, что лапы лягушек, подвешенных на железных или латунных крючках, подергиваются при прикосновении к зонду из другого металла. Он считал, что это вызвано электричеством из тканей лягушек, и назвал это «животным электричеством».
Луиджи Гальвани обнаружил, что лапы лягушек, подвешенных на латунных крючках, дергались, когда их толкали зондом из другого металла. Он думал .Как сделать электролит
3. Подготовить электролизер и монеты для электролиза
1) Как сделать электролит
Сделать электролит для электролитической очистки монет легко: растворите одну столовую ложку пищевой соды (бикарбоната натрия) в одном галлоне (3,78 литра) дистиллированной воды. Некоторые консерваторы утверждают, что сода для стирки более полезна для электролитической очистки, чем пищевая сода, потому что сода для стирки обычно используется для удаления жира, масла и некоторых минералов.
Из своего опыта работы с электролизом я выяснил, что электролит пищевой соды так же эффективен, как и раствор стиральной соды, и безвреден — он не раздражает кожу, как стиральная сода. А мелкие загрязнения — масло, жир и минералы легко смываются с монет ацетоном.
Сода стиральная и пищевая
Соду для стирки можно купить в любом супермаркете или приготовить карбонат натрия дома самостоятельно. Выложите пищевую соду на противень и запекайте в духовке при температуре 149 ° C в течение часа.Тепло отгоняет углекислый газ (CO2) и молекулы воды; таким образом, делая стиральную соду.
НЕ ИСПОЛЬЗУЙТЕ ТАБЛИЧНУЮ СОЛЬ (хлорид натрия) в электролитическом растворе! Электролитический раствор, приготовленный из поваренной соли, будет генерировать ХЛОРИНОВЫЙ ГАЗ, который может быстро и быстро травмировать вас! Другая опасность может возникнуть, если хлор из соли объединяется с выделяющимся водородом, образуя соляную кислоту!
Кроме того, НЕ рекомендуется добавлять в электролит щелочь и / или очистители для сточных вод (содержащие загрязнения)! Доказано, что при использовании щелока или какой-либо другой вредной «добавки» не достигается заметного увеличения скорости процесса.На самом деле не стоит рисковать, связанными с использованием опасного материала и утилизацией щелочного раствора.
• Какая вода используется в электролите
Обычно рекомендуется использовать только дистиллированную воду (доступную в большинстве супермаркетов) или деионизированную воду для приготовления электролита. Водопроводная вода может содержать определенные минералы или химические вещества, которые могут загрязнить электролит, отложиться на монетах или помешать процессу.
• Как определить правильное количество пищевой соды для электролита
Если вы используете зарядное устройство с амперметром в качестве источника питания для электролиза, есть простой способ определить оптимальное количество пищевой соды, необходимое для приготовления электролита в чане любого объема; никаких расчетов и измерений не требуется.
После того, как вы поместили электрод и монету в банку и все соединили (все подробности приведены на следующих страницах), наполните емкость водой (разъемы электродов — зажимы типа «крокодил», нельзя погружать!), Установите ручку регулировки силы тока. в подходящем положении включите зарядное устройство и медленно добавьте в банку небольшое количество пищевой (или стиральной) соды, хорошо помешивая, чтобы вся сода быстро растворилась.
Теперь следите за стрелкой (или стрелкой) индикатора амперметра при добавлении соды: стрелка сначала будет двигаться медленно, но затем будет двигаться быстрее, так как концентрация соды в растворе увеличивается. Когда указатель останавливается (сила тока перестает быстро расти), количество соды в растворе является оптимальным, т. Е. Через электролит проходит не слишком большой ток для выполнения работы, поэтому источник питания — зарядное устройство для аккумулятора не будет «перегружен» «, и никакие соединительные провода не будут слишком горячими и сожженными.Ваш электролит готов! А ваш электролизный аппарат очистит монеты с максимальной эффективностью!
Необходимо сделать достаточный запас электролита не для добавления его в электролитическую ячейку во время электролиза, а для замены загрязненного и израсходованного раствора электролита. Когда слой электролита в процессе опустился, нужно добавить в него только ВОДУ!
2) Подготовка монет к электролизу: механическое удаление рыхлой грязи и корки нейлоновой щеткой
Перед электролитической очисткой монеты любая монета должна быть «подготовлена» к процессу, чтобы процесс можно было легко запустить и запустить без проблем и в более чистой среде внутри электролитической ячейки.
В случае недавно выкопанной монеты рекомендуется на некоторое время поместить ее в ванну с горячей водой, чтобы грязь, мусор и чрезмерная корка немного ослабли. Монету следует подвергнуть этой обработке несколько раз, и после каждого замачивания следует чистить монету нейлоновой щеткой до тех пор, пока большая часть грязи и рыхлой корки не исчезнет. Перед электролизом монеты постарайтесь удалить с монеты как можно больше грязи.
.Как работают батареи? | Живая наука
Батарейки везде. Современный мир зависит от этих портативных источников энергии, которые можно найти во всем: от мобильных устройств до слуховых аппаратов и автомобилей.
Но, несмотря на то, что они широко используются в повседневной жизни людей, батареям часто не уделяют должного внимания. Подумайте об этом: вы действительно знаете, как работает аккумулятор? Не могли бы вы объяснить это кому-нибудь другому?
Вот краткое изложение научных данных об источниках энергии для смартфонов, электромобилей, кардиостимуляторов и многого другого.[Тест: электрические и газовые автомобили]
Анатомия аккумулятора
Большинство аккумуляторов состоят из трех основных частей: электродов, электролита и сепаратора, по словам Энн Мари Састри, соучредителя и генерального директора Sakti3, базирующейся в Мичигане. запуск аккумуляторных технологий.
В каждой батарее по два электрода. Оба сделаны из токопроводящих материалов, но выполняют разные функции. Один электрод, известный как катод, подключается к положительному концу батареи и является местом, где электрический ток выходит (или электроны входят) в батарею во время разряда, то есть когда батарея используется для питания чего-либо.Другой электрод, известный как анод, подключается к отрицательному полюсу батареи и является местом, где электрический ток входит (или электроны покидают) батарею во время разряда.
Между этими электродами, а также внутри них находится электролит. Это жидкое или гелеобразное вещество, содержащее электрически заряженные частицы или ионы. Ионы соединяются с материалами, из которых состоят электроды, производя химические реакции, которые позволяют батарее генерировать электрический ток.[Взгляд изнутри на работу батарей (инфографика)]
Типичные батареи питаются за счет химической реакции. [См. Полную инфографику] (Изображение предоставлено Карлом Тейтом, художником по инфографике)Последняя часть батареи, разделитель, довольно проста. Роль сепаратора состоит в том, чтобы удерживать анод и катод отдельно друг от друга внутри батареи. По словам Састри, без разделителя два электрода соприкоснутся, что приведет к короткому замыканию и нарушит нормальную работу батареи.
Как это работает
Чтобы представить себе, как работает батарейка, представьте, как вы вставляете щелочные батарейки, такие как двойные AA, в фонарик. Когда вы вставляете эти батарейки в фонарик, а затем включаете его, на самом деле вы замыкаете цепь. Накопленная в батарее химическая энергия преобразуется в электрическую, которая выходит из батареи в основание лампы фонарика, заставляя ее загораться. Затем электрический ток снова входит в батарею, но на противоположном конце от того места, где он выходил изначально.
Все части батареи работают вместе, чтобы фонарик загорался. Электроды в батарее содержат атомы определенных проводящих материалов. Например, в щелочной батарее анод обычно изготавливается из цинка, а диоксид марганца действует как катод. Электролит между электродами и внутри них содержит ионы. Когда эти ионы встречаются с атомами электродов, между ионами и атомами электродов происходят определенные электрохимические реакции.
Серия химических реакций, протекающих в электродах, известна как окислительно-восстановительные (окислительно-восстановительные) реакции.В батарее катод известен как окислитель, потому что он принимает электроны от анода. Анод известен как восстановитель, потому что он теряет электроны.
В конечном итоге эти реакции приводят к потоку ионов между анодом и катодом, а также к освобождению электронов от атомов электрода, — сказал Састри.
Эти свободные электроны собираются внутри анода (нижняя плоская часть щелочной батареи). В результате два электрода имеют разные заряды: анод становится отрицательно заряженным, когда высвобождаются электроны, а катод становится положительно заряженным, поскольку электроны (которые заряжены отрицательно) поглощаются.Эта разница в заряде заставляет электроны двигаться к положительно заряженному катоду. Однако у них нет возможности попасть внутрь батареи, потому что разделитель не позволяет им сделать это.
Когда вы щелкаете выключателем на фонарике, все меняется. У электронов теперь есть путь к катоду. Но сначала они должны пройти через основание лампы фонарика. Схема замыкается, когда электрический ток снова входит в батарею через верхнюю часть батареи у катода.
Перезаряжаемые и неперезаряжаемые
Для первичных батарей, например, в фонарике, реакции, питающие батарею, в конечном итоге прекратятся, а это означает, что электроны, которые обеспечивают батарею ее зарядом, больше не будут создавать электрический ток. Когда это происходит, аккумулятор разряжен или «мертв», — сказал Састри.
Вы должны выбросить такие батареи, потому что электрохимические процессы, которые заставили батарею производить энергию, не могут быть обращены вспять, объяснил Састри.Однако электрохимические процессы, происходящие во вторичных или перезаряжаемых батареях, могут быть обращены вспять путем подачи электроэнергии в батарею. Например, это происходит, когда вы подключаете аккумулятор мобильного телефона к зарядному устройству, подключенному к источнику питания.
Некоторые из наиболее распространенных используемых сегодня вторичных батарей — это литий-ионные (литий-ионные) батареи, от которых питается большинство бытовых электронных устройств. Эти батареи обычно содержат угольный анод, катод из диоксида лития-кобальта и электролит, содержащий соль лития в органическом растворителе.Другие перезаряжаемые батареи включают никель-кадмиевые (NiCd) и никель-металл-гидридные (NiMH) батареи, которые можно использовать в таких вещах, как электромобили и аккумуляторные электроинструменты. Свинцово-кислотные (Pb-кислотные) батареи обычно используются в автомобилях и других транспортных средствах для запуска, освещения и зажигания.
По словам Састри, все эти аккумуляторные батареи работают по одному и тому же принципу: когда вы подключаете батарею к источнику питания, поток электронов меняет направление, и анод и катод возвращаются в исходное состояние.[10 лучших подрывных технологий]
Battery lingo
Хотя все батареи работают более или менее одинаково, разные типы батарей имеют разные характеристики. Вот несколько терминов, которые часто встречаются при любом обсуждении батарей:
Напряжение : Когда дело доходит до батарей, напряжение — также известное как номинальное напряжение ячейки — описывает величину электрической силы или давления, при которой свободные электроны — переходите от положительного полюса батареи к отрицательному, — пояснил Састри.В батареях с более низким напряжением ток выходит из батареи медленнее (с меньшей электрической силой), чем в батареях с более высоким напряжением (с большей электрической силой). Батареи в фонарике обычно имеют напряжение 1,5 В. Однако, если в фонарике используются две батареи последовательно, эти батареи или элементы имеют общее напряжение 3 вольта.
Свинцово-кислотные батареи, подобные тем, которые используются в большинстве неэлектрических автомобилей, обычно имеют напряжение 2,0 вольт. Но обычно в автомобильном аккумуляторе последовательно соединено шесть таких ячеек, поэтому вы, вероятно, слышали, что такие батареи называются 12-вольтовыми батареями.
Литий-кобальтооксидные батареи — наиболее распространенный тип литий-ионных батарей, используемых в бытовой электронике, — имеют номинальное напряжение около 3,7 вольт, сказал Састри.
Ампер : Ампер или ампер — это мера электрического тока или количества электронов, которые проходят через цепь в течение определенного периода времени.
Емкость : Емкость или емкость элемента измеряется в ампер-часах, то есть количество часов, в течение которых батарея может подавать определенное количество электрического тока, прежде чем ее напряжение упадет ниже определенного порога, согласно сообщению Райса. Кафедра электротехники и вычислительной техники университета.
9-вольтовая щелочная батарея, используемая в портативных радиоприемниках, рассчитана на 1 ампер-час, что означает, что эта батарея может непрерывно подавать один ампер тока в течение 1 часа, прежде чем она достигнет порогового значения напряжения и будет считаться разряженной.
Плотность мощности : Плотность мощности описывает количество энергии, которое батарея может выдать на единицу веса, сказал Састри. По словам Састри, для электромобилей важна плотность мощности, потому что она показывает, насколько быстро автомобиль может разогнаться от 0 до 60 миль в час (97 км / ч).Инженеры постоянно пытаются найти способы сделать батареи меньше, не уменьшая при этом их удельной мощности.
Плотность энергии : Плотность энергии описывает, сколько энергии способна отдавать батарея, деленное на объем или массу батареи, сказал Састри. Это число соответствует вещам, которые имеют большое влияние на пользователей, например, сколько времени вам нужно пройти до зарядки мобильного телефона или как далеко вы можете проехать на электромобиле, прежде чем остановиться, чтобы подключить его. techEpalermo .Следуйте за Live Science @livescience , Facebook и Google+ .
Дополнительные ресурсы
.Как ухаживать за свинцово-кислотными аккумуляторами
Знаете ли вы основную причину выхода свинцово-кислотных аккумуляторов из строя и потери емкости? Сульфатирование аккумулятора. Это причина этих проблем в 80% случаев. Но с правильными инструментами для обслуживания аккумуляторов и небольшими затратами времени вы вернете свои аккумуляторы к жизни и сохраните их надежную работу. Узнайте все, что вам нужно знать об обслуживании аккумулятора.
Стартерные аккумуляторы, полутяговые аккумуляторы, тяговые аккумуляторы и даже стационарные аккумуляторы — все они нуждаются в техническом обслуживании, чтобы полностью раскрыть свой потенциал.Регулярно выполняйте три основные задачи обслуживания, которые мы здесь описываем, чтобы оптимизировать производительность и надежность ваших свинцово-кислотных аккумуляторов.
Добавьте дистиллированную воду в свинцово-кислотную батарею
Жидкость в свинцово-кислотном аккумуляторе называется электролитом. На самом деле это смесь серной кислоты и воды. Когда аккумулятор заряжается, электролит нагревается, и часть воды испаряется. Во время процесса, называемого электролизом, вода распадается на газообразные водород и кислород, которые рассеиваются.Результат? Уровень электролита в батарее со временем снижается.
Если уровень электролита слишком низкий, пластины аккумуляторных элементов обнажатся и будут повреждены. Кроме того, серная кислота будет более концентрированной. Это означает, что вам необходимо заменить электролит. Вот как вы это делаете.
1. Проверить уровень воды в аккумуляторной батарее с помощью индикатора уровня
Как узнать, когда нужно добавить воды в аккумулятор? Это один из самых частых вопросов, которые нам задают.Вы можете постоянно проверять свою батарею или каждую батарею в каждой машине в вашем парке, но это ужасно трудоемко, и есть более простые подходы. Индикаторы специально разработаны для проверки уровня воды в аккумуляторе. Они уведомят вас, когда вам нужно зарядить аккумулятор.
Доступны разные системы. Один из них — Smartblinky. Вы устанавливаете его за вилкой аккумулятора. Есть ли зеленый свет? Ваш уровень электролита в порядке. Когда индикатор загорится красным, значит, пора добавить воды в аккумуляторные батареи.
Вы добавляете воду в аккумулятор до или после зарядки? Перед зарядкой всегда убедитесь, что электролит покрывает пластины аккумулятора. Если пластины закрыты, зарядите аккумулятор и при необходимости долейте. Это связано с тем, что электролит расширяется во время зарядки и, скорее всего, выльется через край, если вы уже долили его перед зарядкой.
2. Убедитесь, что у вас всегда под рукой дистиллированная вода.
Никогда не заливайте в аккумулятор обычную воду. Это повредит вашу батарею.Вам нужно использовать дистиллированную воду. Она также известна как деионизированная вода и деминерализованная вода. В основном это вода, прошедшая фильтрацию для удаления металлов и минералов, которые могут мешать процессам в вашей батарее.
Купите дистиллированную воду в строительном магазине или у специалиста по автомобильным запчастям. Также легко сделать самому. Вам нужна простая водопроводная вода и устройство для деминерализации, такое как Hydropure. Самые простые из этих устройств наполнены смолой. Вы впускаете водопроводную воду, смола отфильтровывает металлы и минералы из воды, и у вас остается деионизированная, деминерализованная, дистиллированная вода, которая подходит для использования с вашей батареей.
3. Установить автоматическую систему заливки воды в аккумуляторную батарею
Сколько дистиллированной воды вы добавляете в аккумулятор? Это еще один вопрос, который нам часто задают. Ответ варьируется от одной батареи к другой. Это одна из причин, по которой мы рекомендуем использовать систему наполнения аккумулятора водой.
В системе наполнения водой аккумуляторных батарей используются крышки заливных горловин с поплавками, которые соединяются друг с другом через водяные шланги. Они предохраняют аккумулятор от переполнения. И они экономят ваше время. Все, что вам нужно сделать, это налить в шланг дистиллированную воду.Все остальное сделает система розлива.
Свинцово-кислотная батарея выравнивания
Вторая задача в обслуживании аккумуляторов — зарядка. Очень важно, чтобы батареи заряжались равномерно.
Чем больше вы используете аккумулятор, тем больше может колебаться емкость разных элементов. Одна ячейка может быть полностью заряжена, а другая — наполовину. В этом случае аккумулятор заряжается не полностью.
Мы советуем использовать уравнительное зарядное устройство для выравнивающего заряда.Выравнивание батареи — это простой процесс, который предотвращает это. Зарядное устройство для аккумулятора обеспечивает более низкий ток в течение более длительного периода времени. В то время как типичный цикл зарядки длится около восьми часов, стабилизация занимает около одиннадцати часов. Поскольку он также требует более длительного времени охлаждения, чем обычный цикл зарядки, лучше всего выполнять выравнивающий заряд в выходные дни, чтобы у вас было достаточно времени для зарядки и охлаждения аккумулятора перед тем, как снова его использовать.
Что делать, если ваша батарея уже страдает от сульфатации? К счастью, сульфатирование можно контролировать и даже уменьшить.Просто пошлите через батарею большие кратковременные токи. Этот процесс называется восстановлением батареи.
Держите аккумулятор в чистоте
И последнее, но не менее важное: очень важно содержать аккумулятор в чистоте.
Кислота, грязь и пыль в аккумуляторной батарее, как известно, вызывают токи утечки, которые приводят к разрядке аккумулятора и выходу его из строя. Чистая батарея необходима. Как лучше это сделать? Используйте пароочиститель для батарей, например AQ steam или AQ steam pro.
У вас есть вопросы по любой из этих задач по обслуживанию аккумуляторов? Вы хотите знать, какие продукты лучше всего подходят для обслуживания свинцово-кислотных аккумуляторов? Вы найдете ответы — и все остальное, что вам нужно знать — в нашем профессиональном руководстве по обслуживанию аккумуляторов. Нажмите на кнопку, чтобы посмотреть его в Интернете.
Загрузите нашу инструкцию по обслуживанию аккумуляторной батареи
.Как восстановить батареи: пошаговое руководство
Батареи могут быть очень опасными при неправильном обращении, особенно если у вас нет соответствующих средств защиты. Крайне важно носить очки и перчатки, чтобы аккумуляторная кислота не вылилась и не обожгла кожу или что-либо еще, с чем она соприкасается. Батареи также могут взорваться при определенных условиях, особенно если с ними неправильно обращаться и обращаться с ними.
Если вы начинаете ремонтировать аккумулятор, но понимаете, что он треснутый, протекает или поврежден, очень важно утилизировать аккумулятор как можно скорее.В этот момент это небезопасный аккумулятор, и вам лучше утилизировать его, потому что вы больше не можете починить его в таком состоянии.
Наконец, не ремонтируйте аккумулятор более трех или четырех раз. Восстановление батареи может быть отличным способом продлить срок ее службы, но со временем она со временем изнашивается, и вы будете испытывать уменьшение отдачи каждый раз, когда восстанавливаете ее. Восстановленная батарея прослужит несколько лет, если вы продолжите работать с ней, но со временем ситуация ухудшится, и восстановление в конечном итоге скорее повредит батарее, чем поможет ей.
.Как правильно повысить плотность электролита в аккумуляторе
Пониженная или повышенная плотность электролита в аккумуляторе уменьшает эффективность работы батареи и ускоряет ее износ. Поэтому периодически необходимо измерять данный показатель и в случае отклонений от нормы проводить корректировку. Разберем детально, как это правильно сделать.
Содержание
- Чем и как проверять плотность электролита для аккумуляторов
- Как повысить плотность электролита в автомобильном аккумуляторе
- Резюме
Чем и как проверять плотность электролита для аккумуляторов
Нормой считается показатель в 1,27 грамма на кубический сантиметр. Измерения проводятся специальным диагностическим инструментом — ареометром. Важно, чтобы он был качественно изготовлен и показывал точные результаты. Хорошим и недорогим прибором является ареометр RedMark в тубе. Его можно использовать для проверки электролита и тосола.
Вот несколько правил, которые следует соблюдать:
- Измерения нужно проводить при полностью заряженной батарее.
- Проверять необходимо каждую банку.
- Температура воздуха должна быть 20–25 градусов тепла.
С учетом последнего пункта может возникнуть вопрос о том, как повысить плотность электролита в аккумуляторе зимой. Если автомобиль стоит не в теплом гараже, придется снять батарею и занести ее домой. Полностью зарядить и только потом проверить каждую банку.
Как повысить плотность электролита в автомобильном аккумуляторе
Прежде чем приступить к работе, подготавливаем все необходимое. Важно помнить, что данная жидкость представляет собой соединение, опасное для человека. Его попадание на открытые участки кожи может вызвать сильные химические ожоги. Поэтому работать необходимо в защитных резиновых перчатках. Кроме того, потребуются:
- ареометр;
- стеклянная емкость;
- корректирующий электролит;
- дистиллированная вода.
Суть работы заключается в том, чтобы откачать часть жидкости из аккумуляторной батареи и заместить ее корректирующим электролитом. Для откачки можно использовать ареометр. Набираем в него жидкость из батарейных банок и сливаем ее в заранее подготовленную емкость.
При откачивании важно помнить о том, что нельзя оголять аккумуляторные пластины. Необходимо, чтобы они все время были покрыты жидкостью.
Многие автовладельцы задаются вопросом, какой корректирующий электролит для аккумуляторов купить? Хорошим вариантом является «ДРЕКО», имеющий плотность 1,3 г/см3. С его помощью приводим показатели каждой банки в норму.
Вы спросите, а что будет, если переборщить? Параметры 1,28–1,29 г/см3 — это уже повышенная плотность электролита, которую в новом аккумуляторе нужно обязательно снизить. Просто добавляем дистиллированную воду. Использовать обычную, из-под крана, нельзя.
Резюме
Быстрый разряд и слабый пусковой ток далеко не всегда говорят о том, что батарею пора менять. Возможно, что причина неэффективной работы кроется именно в понизившейся плотности. Чтобы решить проблему, достаточно купить электролит для аккумуляторов, имеющий повышенную концентрацию, и с его помощью довести показатели до нормы.
Как восстановить гелевый аккумулятор самостоятельно в домашних условиях
Время прочтения: 5 мин
Дата публикации: 12-08-2020
Аккумуляторная батарея – это важный расходник в системах резервного электроснабжения, мотоциклах, скутерах, автомобилях и в прочих видах транспорта. Несмотря на то, что цена аккумулятора не является заоблачной, часто менять батареи никто не хочет. Чтобы АКБ прослужила долго и безотказно, следует придерживаться требований по эксплуатации. Тем не менее, из-за халатного отношения или невнимательности аккумуляторы часто значительно теряют свои первоначальные характеристики или, иными словами, выходят из строя.
Сперва определимся, что такое гелевая аккумуляторная батарея. Гелевым называют свинцово-кислотный аккумулятор с электролитом, свойства которого близки к сухому. Речь идет об АКБ класса GEL. В ней жидкий электролит абсорбирован гелевым наполнителем. Это наделяет батарею массой полезных свойств и преимуществ по сравнению с традиционными АКБ. Из-за схожести реализации и «маркетинговых трюков» гелевыми также называют аккумуляторы класса AGM. И действительно: принцип тот же, только вместо геля свободное пространство заполнено пористым стекловолоконным наполнителем.
Как GEL, так и AGM аккумуляторы являются необслуживаемыми. Речь идет об отсутствии необходимости доливать дистиллированную воду в связи с протеканием процесса рекомбинации. Многие трактуют это иначе и, например, не поддерживают высокий уровень заряда, хотя это необходимо для любой свинцово-кислотной АКБ. Гелевые аккумуляторы часто эксплуатируются в режимах с длительными периодами хранения. В таких условиях можно запросто упустить недопустимо низкий заряд батареи. Поэтому рекомендуется завести мультиметр и периодически проверять напряжение между клеммами. Только оно опустится ниже 10,5-11В – требуется осуществить обслуживание в виде заряда. Если же ситуацию запустить, возможно придется выполнить восстановление гелевого аккумулятора после глубокого разряда.
Что надо знать о сульфатации и десульфатации
В процессе разряда положительные пластины покрываются слоем сульфата свинца. Когда начинается заряд – образовавшийся слой мелкокристаллического сульфата растворяется и аккумулятор возвращается в первоначальное состояние. Условие необратимого образования крупнокристаллического сульфата свинца – это глубокий разряд. Такой налет не снимется полностью в процессе заряда, снижая активность протекающей между электролитом и электродами реакцию. Существуют различные способы очистки пластин:
- Способ №1. Самый простой и безопасный способ частично избавиться от налета в домашних условиях – это использование режима восстановления, который доступен во многих современных зарядных устройствах. Данный режим заключается в чередовании лавинообразных импульсов тока с периодами разряда, что позволяет добиться некоторого восстановления емкости. От крупнокристаллического сульфата, конечно же, такой способ не поможет.
- Способ №2. Существуют растворы, позволяющие растворить образовавшийся на пластинах сульфат свинца. Если первый способ можно назвать электрическим, то этот – химическим. Химическая очистка сульфата более эффективна и позволяет добиться очищения более крупного налета сульфата.
- Способ №3. Никуда не делся старый добрый механический способ удаления сульфата свинца. Это наиболее опасный способ, который ни в коем случае не рекомендуется использовать. Для этого придется необратимо повредить корпус и, возможно, сами пластины.
Осуществлять какие-либо физические и химические манипуляции над электродами с целью их очистки крайне не рекомендуются. Поэтому важно следить за уровнем заряда и не допускать глубокого разряда, способствующего сульфатации. Только так Вы можете обеспечить длительный срок службы аккумуляторной батареи.
Восстановления электролита
И все же, как восстановить гелевый аккумулятор, если манипуляции с электродами совершать не рекомендуется? Единственное, что Вы можете сделать, не навредив – это долить дистиллированной воды, если та все-таки испарилась. В гелевых аккумуляторах испарения возможны лишь при неправильной эксплуатации. Если ток заряда превышает допустимые значения, электролит может закипать, а образовавшиеся испарения – выходить через предохранительные клапаны.
Если требуется долив воды, необходимо снять крышку и колпачки с банок, после чего заливать дистиллированную воду мелкими порциями. Каждой порции воды следует дать впитаться в наполнитель. Испарение воды – это, повторимся, единственный случай, когда можно довольно безопасно восстановить характеристики гелевого аккумулятора. Во многих остальных случаях батарея не подлежит восстановлению.
Определить, можно ли что-то сделать с аккумулятором, можно визуально. Если аккумулятор потерял емкость, то первое, на что надо обратить внимание – это форма аккумулятора. Если различимо даже малейшее вздутие – эксплуатировать АКБ нельзя. В таком случае только замена. Если же аккумулятор не изменил свою форму, следует убедиться, что с пластинами все в порядке – вполне возможно они попросту начали рассыпаться. Для этого можно потрясти АКБ и постараться расслышать шум от движения трухи, которая отслоилась от электродов. Следующий шаг – это визуальный осмотр через отверстия банок. Снимите колпачки и посветите внутрь, стараясь рассмотреть очертания пластин. Если они рассыпались – пора покупать новый аккумулятор.
Проверяем емкость
Прежде чем делать выводы о состоянии свинцово-кислотной аккумуляторной батареи, надо узнать текущие показатели емкости. А как проверить емкость гелевого аккумулятора, когда вменяемых технических приспособлений для этого попросту нет? Здесь на помощь приходит классический контрольный разряд. Для «эксперимента» потребуется лишь потребитель с известной мощностью (в идеале лампочка) и мультиметр.
Зарядите гелевый аккумулятор до 100% и повесьте на него нагрузку. Следует засечь время, за которое аккумулятор потеряет половину заряда. Сколько осталось заряда, можно определить при помощи мультиметра, измеряя напряжение. Для гелевых аккумуляторов при 50% емкости напряжение будет составлять 12В. Проверять емкость аккумуляторной батареи путем разряда до нуля не рекомендуется по понятным причинам: Вы не только проверите емкость аккумулятора, но и сократите его срок службы глубоким разрядом.
Таким образом, мы приходим к одному важному выводу: практически любые проблемы, связанные с гелевым аккумулятором, вызваны нарушением требований по эксплуатации. Закипание электролита связано с неправильным зарядом, сульфатация пластин — с глубоким разрядом, а их осыпание – с эксплуатацией под высокой температурой.
Следовательно, единственный способ добиться максимально длительного срока службы – это вовремя заряжать аккумуляторную батарею качественным зарядным устройством, а также эксплуатировать АКБ в прохладном помещении. Банальным бережным обслуживанием батареи Вы добьетесь таких показателей длительности работы и срока службы АКБ, каких не добьетесь ни одним существующим способом восстановления.
Как ухаживать за свинцово-кислотными аккумуляторами
Знаете ли вы основную причину выхода свинцово-кислотных аккумуляторов из строя и потери емкости? Сульфатирование аккумулятора. Это причина этих проблем в 80% случаев. Но с правильными инструментами для обслуживания батарей и небольшими затратами времени вы вернете свои батареи к жизни и обеспечите их надежную работу. Узнайте все, что вам нужно знать об обслуживании аккумулятора.
Стартерные батареи, полутяговые батареи, тяговые батареи и даже стационарные батареи — все они нуждаются в техническом обслуживании, чтобы полностью раскрыть свой потенциал.Регулярно выполняйте три основные задачи по техническому обслуживанию, которые мы здесь описываем, чтобы оптимизировать производительность и надежность ваших свинцово-кислотных аккумуляторов.
Добавьте дистиллированную воду в свинцово-кислотную батарею
Жидкость в свинцово-кислотном аккумуляторе называется электролитом. На самом деле это смесь серной кислоты и воды. Когда аккумулятор заряжается, электролит нагревается, и часть воды испаряется. Во время процесса, называемого электролизом, вода распадается на газообразные водород и кислород, которые рассеиваются.Результат? Уровень электролита в аккумуляторе со временем снижается.
Если уровень электролита слишком низкий, пластины аккумуляторных элементов обнажатся и будут повреждены. Кроме того, серная кислота будет более концентрированной. Это означает, что вам необходимо заменить электролит. Вот как вы это делаете.
1. Проверить уровень воды в аккумуляторе с помощью индикатора уровня
Как узнать, когда нужно долить воду в аккумулятор? Это один из самых частых вопросов, которые нам задают.Вы можете постоянно проверять свою батарею или каждую батарею в каждой машине в вашем парке, но это ужасно трудоемко, и есть более простые подходы. Индикаторы специально разработаны для проверки уровня воды в аккумуляторе. Они уведомят вас, когда вам нужно зарядить аккумулятор.
Доступны разные системы. Один из них — Smartblinky. Вы устанавливаете его за вилкой аккумулятора. Есть ли зеленый свет? Ваш уровень электролита в порядке. Когда индикатор загорится красным, вы поймете, что пора добавить воды в аккумуляторные элементы.
Вы добавляете воду в аккумулятор до или после зарядки? Перед зарядкой всегда убедитесь, что электролит покрывает пластины аккумулятора. Если пластины закрыты, зарядите аккумулятор, а затем долейте при необходимости. Это связано с тем, что электролит расширяется во время зарядки и, скорее всего, выльется через край, если вы уже долили его перед зарядкой.
2. Убедитесь, что у вас всегда под рукой есть дистиллированная вода.
Никогда не заливайте в аккумулятор обычную воду. Это повредит вашу батарею.Вам нужно использовать дистиллированную воду. Она также известна как деионизированная вода и деминерализованная вода. По сути, это вода, прошедшая фильтрацию для удаления металлов и минералов, которые могут помешать процессам в вашей батарее.
Купите дистиллированную воду в строительном магазине или у специалиста по автомобильным запчастям. Также легко сделать самому. Вам нужна простая водопроводная вода и устройство для деминерализации, такое как Hydropure. Самые простые из этих устройств заполнены смолой. Вы впускаете водопроводную воду, смола отфильтровывает металлы и минералы из воды, и у вас остается деионизированная, деминерализованная, дистиллированная вода, подходящая для использования с вашей батареей.
3. Установить автоматическую систему заливки воды в аккумуляторную батарею
Сколько дистиллированной воды вы добавляете в аккумулятор? Это еще один вопрос, который нам часто задают. Ответ варьируется от одной батареи к другой. Это одна из причин, по которой мы рекомендуем использовать систему наполнения аккумулятора водой.
В системе заливки воды в аккумуляторной батарее используются крышки заливных горловин с поплавками, которые соединяются друг с другом с помощью водяных шлангов. Они предохраняют аккумулятор от переполнения. И они экономят ваше время. Все, что вам нужно сделать, это налить в шланг дистиллированную воду.Все остальное сделает система розлива.
Свинцово-кислотная батарея выравнивания
Вторая задача при обслуживании аккумуляторов — зарядка. Очень важно, чтобы батареи заряжались равномерно.
Чем больше вы используете аккумулятор, тем больше может колебаться емкость различных ячеек. Одна ячейка может быть полностью заряжена, а другая — наполовину. В этом случае аккумулятор не будет заряжаться полностью.
Мы советуем использовать уравнительное зарядное устройство для выравнивающего заряда.Выравнивание заряда батареи — это простой процесс, который предотвращает это. Зарядное устройство для аккумулятора обеспечивает более низкий ток в течение более длительного периода времени. В то время как типичный цикл зарядки длится около восьми часов, стабилизация занимает около одиннадцати часов. Поскольку он также требует более длительного времени охлаждения, чем обычный цикл зарядки, лучше всего выполнять выравнивающий заряд на выходных, чтобы у вас было достаточно времени для зарядки и охлаждения аккумулятора перед тем, как снова использовать его.
Что делать, если ваша батарея уже страдает от сульфатации? К счастью, сульфатирование можно контролировать и даже уменьшать.Просто пошлите через батарею большие кратковременные токи. Этот процесс называется восстановлением аккумуляторной батареи.
Держите аккумулятор в чистоте
И последнее, но не менее важное: очень важно содержать аккумулятор в чистоте.
Кислота, грязь и пыль в аккумуляторной батарее, как известно, вызывают токи утечки, которые приводят к разрядке аккумуляторной батареи и ее разбалансировке. Чистая батарея необходима. Как лучше это сделать? Используйте пароочиститель для аккумуляторов, например AQ steam или AQ steam pro.
У вас есть вопросы по любой из этих задач по обслуживанию аккумуляторных батарей? Хотите знать, какие продукты лучше всего подходят для обслуживания свинцово-кислотных аккумуляторов? Вы найдете ответы — и все остальное, что вам нужно знать — в нашем профессиональном руководстве по обслуживанию аккумуляторов. Нажмите на кнопку, чтобы посмотреть его в Интернете.
Загрузите нашу инструкцию по обслуживанию аккумуляторной батареи
У вас должен быть включен JavaScript, чтобы использовать эту форму.
Аккумуляторный электролит представляет собой смесь воды и- Введение, раствор и соотношение_Greenway аккумулятор
Аккумулятор вашего автомобиля не всегда может быть заполнен необходимым количеством электролита, который необходим для его правильного функционирования.Поэтому в некоторых случаях может потребоваться добавить электролит в аккумулятор вашего автомобиля. Это может показаться легкой задачей, но на самом деле это не так просто, потому что это довольно сложный предмет.
? Итак, если в вашем автомобильном аккумуляторе заканчивается электролит, и у вас мало информации о том, что такое электролит или каково соотношение кислоты и воды в аккумуляторе, то вы попали на соответствующий веб-сайт, потому что мы ‘ Мы предоставили вам ответы на все ваши вопросы, касающиеся электролита аккумулятора.
? Давайте начнем и разберемся в «Электролит батареи — это смесь воды и — введение, раствор и соотношение»!
Из чего сделан аккумуляторный электролит? Если вы не знаете, из чего сделан электролит, мы здесь, чтобы дать ответ! Большинство обычных батарей состоит из жидкости, известной как электролит. Этот электролит в батарее представляет собой смесь серной кислоты и воды. Пластины свинцово-кислотных аккумуляторов содержат активный материал, который всегда должен быть погружен в электролит, в то время как водород и газообразный кислород выделяются во время зарядки.Пока аккумулятор заряжается, плотность раствора электролита будет увеличиваться.
Электролиты в батарее служат катализатором, делающим батарею проводящей, инициируя движение ионов от катода к аноду при зарядке и наоборот при разряде. В зависимости от того, в какой степени электролит аккумулятора может выделять ионы, электролит может быть сильным или слабым. Сильные электролиты — это соединения, которые отлично ионизируют и проводят мощный электрический ток.С другой стороны, слабые электролиты — это соединения, которые ионизируются в минимальной и небольшой степени и проводят небольшой электрический ток.
Теперь, если мы говорим о составе электролитов, то вам важно отметить, что разные батареи используют разные химические соединения в качестве электролита. Некоторые из обычно используемых соединений включают хлорид натрия, серную кислоту, азотную кислоту, хлорную кислоту, ацетат натрия и т. Д. Таким образом, в зависимости от типа или марки батареи, состав электролита батареи будет меняться от одной батареи к другой.Но в большинстве случаев электролиты в свинцово-кислотных аккумуляторах состоят из серной кислоты и воды.
Что такое раствор электролита для аккумуляторов? Как вы прочитали выше, из чего состоит электролит, теперь давайте разберемся, что такое раствор электролита для аккумуляторов?
Каждая батарея состоит из катода, анода и электролита. Анод и катоды — это электроды, которые полностью погружены в раствор электролита и соединены снаружи с помощью проводящего провода.Когда анод и катод растворяются в растворителе, раствор электролита выделяет ионы. Разряженные электролитом ионы реагируют с анодом, высвобождая один или несколько электронов.
Проще говоря, мы можем сказать, что электролит — это среда, которая предлагает механизм переноса ионов между катодом и анодом ячейки. Электролит часто рассматривается как жидкая смесь воды и других растворителей с растворенными кислотами, солями или щелочами, которые необходимы для ионной проводимости.Электролит допускает движение только ионов. В качестве аккумуляторного электролита обычно используются материалы с высокой ионной проводимостью, так что ионы лития могут легко перемещаться вперед и назад. Полное движение ионов лития обычно зависит от типа электролита; поэтому всегда следует использовать электролит, отвечающий строгим требованиям.
Каково соотношение серной кислоты и воды в батарее? Когда дело доходит до электролита в батарее, большинство людей обычно не понимает, какое соотношение кислоты и воды в батарее! Если вы один из тех, кто запутался в одном и том же, то вам больше не нужно запутываться, потому что у нас есть для вас ответ!
Когда мы говорим об электролите, мы обычно говорим о растворе серной кислоты и воды.Этот раствор серной кислоты и воды заполняет элементы свинцово-кислотных аккумуляторов, а синергия между свинцовыми пластинами и электролитом позволяет аккумулятору вашего автомобиля накапливать и выделять энергию.
Итак, всякий раз, когда в аккумуляторе вашего автомобиля заканчивается электролит, может потребоваться добавить в него дополнительный электролит. Но для этого вы должны быть уверены в процентном соотношении кислоты к воде в батарее! Каждый раз, когда вы ищете ответ на этот вопрос в Интернете, вы можете не найти подходящих результатов ни на одном из веб-сайтов, но у нас есть соответствующий ответ на ваш запрос.?
Кислота, присутствующая в аккумуляторной батарее вашего автомобиля, обычно представляет собой серную кислоту, которая обычно разбавляется водой до уровня концентрации 37%. Этот уровень концентрации аккумулятора вашего автомобиля обычно варьируется от одного аккумулятора к другому, в зависимости от марки. Идеальное соотношение кислоты и воды в аккумуляторе составляет 30,1 см3 кислоты: 100 см3 дистиллированной воды. Если это соотношение кислоты и воды не поддерживается должным образом, весь механизм электрохимии в аккумуляторе может быть изменен.
Итог Здесь вы подошли к сути статьи «Аккумуляторный электролит представляет собой смесь воды и — введение, раствор и соотношение»! Мы надеемся, что у вас есть точное представление о том, что такое электролит, из чего он состоит, процентное соотношение кислоты к воде в электролите и многое другое. Вся приведенная выше информация верна, поэтому вы можете быть уверены в ее достоверности. Всегда помните, что электролит аккумулятора часто называют аккумуляторной кислотой, потому что он очень кислый по своей природе.Так что, если в следующий раз вы столкнетесь с чем-то связанным с электролитом аккумулятора, эта информативная статья обязательно поможет вам в этом!
литий-ионный аккумулятор аккумулятор для электровелосипеда литиевая батарея
6 шагов Проверка уровня электролита в батареях
Обслуживание аккумуляторов — это тема, о которой часто забывают, особенно когда речь идет об автомобильных аккумуляторах .
Чаще всего, если вы открываете капот автомобиля, вы видите аккумулятор, который называется мокрой батареей.Это означает, что в нем есть вода или электролит, который используется в качестве соединителя между электродами батареи.
Эта вода реагирует на окружающую среду так же, как и вода в любом другом месте: она испаряется.
Чтобы продлить срок службы влажной аккумуляторной батареи, важно проверять уровень электролита и пополнять его по мере его снижения. К сожалению, это не так просто, как может показаться. К счастью, эти шесть шагов помогут упростить задачу.
Шаг 1. Безопасность прежде всегоВы слышали это миллион раз, и это не потому, что мы любим это говорить.Это потому, что безопасность — это всегда первое, что вы должны учитывать при работе с аккумулятором.
Каждый раз, когда вы работаете с аккумулятором, вы должны принять некоторые меры предосторожности . Батарея может не только сильно встряхнуть, но и стать опасной при неправильном обращении.
Убедитесь, что у вас есть перчатки и защитные очки. Вы также можете отсоединить аккумулятор и вынуть его из машины, прежде чем начинать с ним возиться. Этот шаг — гораздо лучший вариант, чем создание потенциально опасной ситуации.
Шаг 2. ОчиститьЕсть много причин, по которым вы должны постоянно содержать верхнюю часть батареи в чистоте. Помимо нежелания загрязнять внутреннюю часть батареи после ее открытия, вы также уменьшите риск непреднамеренной разрядки.
Аккумулятор лучше всего чистить старой зубной щеткой или металлической щеткой, смоченной смесью пищевой соды и воды. Окуните кисть в смесь и удалите с нее любую грязь или коррозию.Протрите аккумулятор чистой тряпкой без ворса.
Шаг 3. Проверьте уровни электролитаПрежде чем вы просто начнете заливать аккумулятор дистиллированной водой, вам нужно проверить уровень электролита, чтобы увидеть, нужно ли вообще доливать аккумулятор.
Вы можете сделать это по:
- Сначала снимите пластиковые крышки, закрывающие порты элементов. Это может потребовать некоторого поддевания отверткой.
- После снятия крышек осторожно очистите всю грязь, которая могла скопиться под ними.
- Теперь, когда ячейки открыты, вы захотите проверить уровень электролита. Лучший способ узнать, нужно ли батарее больше электролита, — это обнажить пластины или приблизиться к ним. Другой способ узнать, не одинаковы ли уровни электролита в каждой ячейке.
В данном случае электролит означает просто дистиллированную воду. Вы не хотите добавлять воду в другой форме и уж точно не кислоту.Знание того, сколько добавить , также является важным отличием. Обычное практическое правило — добавлять достаточно воды, чтобы покрыть электроды или пластины.
Для новых полностью заряженных аккумуляторов можно безопасно добавить достаточное количество электролита, чтобы его уровень совпадал с нижней частью заливной трубки.
Шаг 5: Восстановите элементы, замените батареюТеперь, когда уровни электролита долиты, установите на место крышки портов ячейки. Убедитесь, что на дно крышек нет грязи или пыли, чтобы предотвратить возможное загрязнение.
После того, как крышки будут закреплены, можно безопасно заменить батарею и повторно подсоединить кабели.
Шаг 6: Используйте аккумуляторТеперь, когда аккумулятор очищен и электролиты пополнились, попробуйте завести машину и даже немного покататься на ней.
Обратите внимание на общую производительность аккумулятора. Легко ли было начать? Можете ли вы выключить машину и снова запустить ее без проблем? Если улучшения нет или аккумулятор не держит заряд, возможно, вам потребуется полностью заменить аккумулятор.
Правильное обслуживание аккумулятора может помочь сохранить максимальную производительность аккумулятора дольше. Вы даже можете сэкономить деньги, не заменяя батарею так часто. Попробуйте добавить уход за батареей в свой распорядок обслуживания. Это поможет вам отслеживать, как часто вам нужно будет пополнять уровень электролита, и подскажет, когда что-то только начинает идти не так.
границ | Стратегии производства твердого электролита в аккумуляторах
Введение
Популяризация коммерческих аккумуляторов — один из важнейших моментов современной цивилизации.В последние несколько десятилетий общество стало свидетелем изобретения медицинских имплантатов с автономным питанием, беспроводной электроники, электромобилей и многих других приложений, которые питаются от батарей различных форм и размеров. Традиционные батареи с использованием органических жидких электролитов продемонстрировали преимущества высокой ионной проводимости и отличной смачиваемости электродами (Zhang, 2007; He et al., 2019), но страдают от потенциальных проблем безопасности, таких как высокая воспламеняемость, плохая термическая стабильность и утечка жидкости. (Strauss et al., 2020; Инь и др., 2020; Юань и Лю, 2020). Для устранения недостатков безопасности, присущих традиционным батареям, при одновременном соблюдении высоких требований к электрохимическим характеристикам, батареи, в которых используется твердотельный электролит (SSE), продемонстрировали многообещающий выбор в качестве лучшей альтернативы.
Как правило, SSE можно разделить на твердые полимерные электролиты (SPE), неорганические твердые электролиты (ISE) и композитные твердые электролиты (CSE). SPE состоят из высокомолекулярной полимерной матрицы и растворенной соли лития, ISE состоят из всех неорганических материалов, таких как керамика и стекло, а CSE, состоящие как из твердого полимера, так и из неорганических веществ (Zhang H.et al., 2017; Чен В. и др., 2018; Chen Y. et al., 2020). Как один из ключевых компонентов для практического применения твердотельных аккумуляторов, SSE продемонстрировали многочисленные преимущества перед органическим жидким электролитом: (i) характеристики негорючести, высокотемпературной стабильности и нелетучей среды для исключения возгорания или взрыва. органических жидких электролитов (Fergus, 2010; Takada, 2013; Sun et al., 2020), (ii) широкое электрохимическое окно, обеспечивающее лучшую совместимость с катодом с более высоким потенциалом, что значительно улучшает плотность энергии (Judez et al., 2017; Wang et al., 2018), (iii) улучшенная механическая жесткость (особенно для ISE) для подавления роста дендритов из циклических металлических анодов (G динаф и Сингх, 2015; Kim JG et al., 2015), и (iv) настраиваемый модуль упругости (особенно для SPE и CSE), обеспечивающий более высокую степень технологичности и гибкости (Yue et al., 2016; Lau et al., 2018; Schnell et al., 2018; Zhou et al., 2018). Однако следует дополнительно изучить и решить несколько проблем: (i) низкая ионная проводимость (<10 –5 См см –1 для SPE и <10 –3 См см –1 для ISE) по сравнению с жидким электролитом (> 10 –3 См см –1 ), что приводит к низкой мощности, и (ii) трудностям в производстве миниатюрных / больших ИСЭ с высокой хрупкостью.В сочетании с новым дизайном материалов разработка передовых производственных стратегий обеспечит решения вышеуказанных проблем.
Развитие аккумуляторных технологий демонстрирует экспоненциальную тенденцию с 1800-х годов, и мы стали свидетелями мотивации разработки аккумуляторов к постепенному переходу от улучшения характеристик электрохимических элементов к удовлетворению требований конфигурации сложных приложений. На рисунке 1 показано несколько важных этапов развития производства аккумуляторов.В качестве самого раннего задокументированного изобретения батареи, гальваническая свая состояла из штабеля из меди, цинка и пропитанной соленой водой ткани в виде цилиндра для хранения электрохимической энергии (Abetti, 1952; Warner, 2015). Почти шесть десятилетий спустя Гастон Планте (Kurzweil, 2010) погрузил блоки параллельных свинцово-оксидных пластин в серную кислоту и создал первую аккумуляторную батарею. Как гальванические, так и свинцово-кислотные батареи основывались на наложении металлических пластин друг на друга для увеличения напряжения элементов (Warner, 2015).Поскольку развитие продолжается, в никель-кадмиевых батареях использовалась цилиндрическая ячейка, заполненная электродами из уплотненного металлического листа, свернутыми в катушку с увеличенной площадью поверхности, чтобы уменьшить сопротивление батареи. Эта цилиндрическая конструкция была принята в более поздних коммерческих щелочных батареях с электродными материалами, заполненными внутренним и внешним слоями (Furukawa et al., 1984). В 1971 году изобретение литий-йодных батарей внесло значительный вклад в промышленность медицинских устройств. В этом элементе батареи использовался металлический чехол с закругленными краями для предотвращения проблем с проникновением, которые могут возникнуть из-за острых углов при имплантации в человеческое тело в составе кардиостимуляторов (Greatbatch and Holmes, 1991; Ruetschi et al., 1995).
Рисунок 1. Развитие производства аккумуляторов.
С момента коммерциализации литий-ионных аккумуляторов (LIB) компанией Sony Co. в 1991 году (Yoshio et al., 2009) в LIB были применены многие традиционные и новые форм-факторы, позволяющие разрабатывать более совершенные продукты с точки зрения эстетики и качества. функциональность. В литий-ионных призматических элементах использовались уплотненные и свернутые электроды, которые ранее использовались в никель-кадмиевых батареях, и они были упакованы в контейнеры, форма которых визуально напоминала плоскую плитку шоколада (Cousseau et al., 2006). Литий-ионные карманные элементы достигли высокой эффективности упаковки 90–95% за счет сварки проводящих контактов с электродной фольгой и герметичного закрытия всех материалов внутри пакета (Buchmann, 2001). Изобретение как литий-ионных призматических, так и карманных ячеек является частью усилий по созданию более тонкой и легкой электроники. С прогрессом в технологической зрелости и сложности в последние годы, новые производственные стратегии могут быть применены к батареям в различных масштабах, которые подходят для различных приложений.Например, наноразмерные батареи, используемые в качестве источника питания в биомедицинских приложениях (Johannessen et al., 2006; Ruzmetov et al., 2012), гибкие батареи для складной / носимой электроники (Dudney, 2008; Leijonmarck et al., 2013; Deng et al., 2017) и потенциально крупномасштабные аккумуляторные сети для хранения возобновляемой энергии (Diouf and Pode, 2015). Однако традиционные стратегии производства аккумуляторов, такие как сухое прессование, литье, центрифугирование и рулон на рулон, неудовлетворительны при изготовлении аккумуляторов сложной формы или микро / нанометров, особенно для ISE (Manthiram et al., 2017; Schnell et al., 2018; Dirican et al., 2019). Поэтому существует потребность использовать новую производственную стратегию для решения вышеуказанных проблем.
Появление технологии 3D-печати предложило уникальный метод производства, позволяющий создавать детали с высокой сложностью и прекрасными характеристиками (Chen Z. et al., 2019; Santoliquido et al., 2019). Хотя использование технологии 3D-печати может быть многообещающей альтернативой в производстве SSE, первоначальная цель развития 3D-печати не была направлена на производство батарей.В результате существует огромный разрыв между возможностями современных технологий 3D-печати и требованиями к производству аккумуляторов. Этот обзор направлен на преодоление разрыва путем анализа существующих ограничений в производстве SSE и выявления будущих потребностей. Благодаря всестороннему обзору традиционных и новых производственных стратегий SSE, мы стремимся обеспечить руководство и просвещение в отношении потенциальных прорывов в производственных технологиях как для лабораторных исследований, так и для промышленного производства.
Традиционные производственные стратегии
Твердые полимерные / композитные электролиты
Твердые полимерные электролиты (ТПЭ) были тщательно изучены для складных и растягиваемых аккумуляторов (Commarieu et al., 2018; Liang et al., 2018; Chen Y. et al., 2020) благодаря нескольким преимуществам, таким как высокая гибкость, простота технологичность и хорошая смачиваемость. Для производства ТФЭ можно использовать три различных пути: обработка на основе порошка, влажная химическая обработка и обработка с высокой вязкостью.Для обработки на основе порошков сначала используется процесс сухого измельчения на высокой скорости для приготовления хорошо перемешанных мелких порошков, а затем ТФЭ могут быть получены путем сухого прессования (Li et al., 2018), горячего / холодного изостатического прессования ( Appetecchi et al., 2001) или процесс осаждения (Hafner et al., 2019). Преимуществами обработки на основе порошков являются простота эксплуатации, низкие требования к оборудованию и возможное исключение стадий уплотнения (Nguyen et al., 2019). Однако этот процесс требует больших затрат времени и энергии, и его сложно масштабировать.Для влажной химической обработки необработанные частицы сначала диспергируют с растворителем для получения суспензии с заданной вязкостью, а затем формируют SPE путем литья из раствора (Sun et al., 2019), электрофоретического осаждения (Blanga et al., 2015), или процесс нанесения покрытия (Park et al., 2006). Преимуществами мокрой химической обработки являются хорошая смачиваемость и высокая производительность (Liu et al., 2017). Однако недостатком является необходимость удаления растворителя. Для обработки с высокой вязкостью сначала готовят высоковязкую пасту, не содержащую растворителей, состоящую из полимеров, при повышенных температурах, а затем применяют процесс экструзии для создания SPE с желаемым форм-фактором (Li W.et al., 2017), которому в некоторых случаях помогает ультрафиолетовое (УФ) облучение для сшивания полимерных цепей. Преимуществами этого процесса являются обработка без использования растворителей и образование гибких мембран с низкой пористостью (Wang et al., 2005). Недостатками могут быть ограниченная производительность во время процесса экструзии и высокий процент дефектов в неравномерно нанесенных полимерных пленках. Основными проблемами SPE являются низкая ионная проводимость 10 –8 ∼10 –5 См см –1 при температуре окружающей среды (Liang et al., 2018) и высокое межфазное сопротивление за счет полимера изолирующего Li + (Wan et al., 2019).
CSE, состоящие из полимерных и неорганических частей, разработаны для достижения удовлетворительных комплексных свойств и исключительных синергетических эффектов по сравнению с однокомпонентным электролитом. Из-за присутствия полимера производственные стратегии CSE аналогичны таковым для SPE, о которых сообщалось в предыдущих обзорах (Commarieu et al., 2018; Liu et al., 2018; Tan et al., 2018; Ли и др., 2020). Одной из самых популярных технологий получения CSE является электроспиннинг, при котором образуются переплетенные и высокопористые нановолокна с большим отношением поверхности к объему и повышенной механической прочностью за счет эффектов переплетения и армирования (Cavaliere et al., 2011; Wootthikanokkhan et al. ., 2015; Carli et al., 2019). Общей проблемой, которую следует отметить при производстве CSE, является ограниченная массовая загрузка неорганических материалов, которые легко агломерируются и, таким образом, ухудшают ионную проводимость и механическую прочность батарей.В целом, SPE и CSE обладают высокой технологичностью из-за высокой гибкости полимерных материалов.
Неорганические твердые электролиты
Неорганические твердые электролиты можно разделить на группы кристаллических, стеклянных и стеклокерамических электролитов. Большинство кристаллических электролитов — это керамика, например, типа NASICON, типа перовскита и типа граната, которые стабильны в окружающем воздухе, что может упростить изготовление элементов и повысить безопасность. Керамический электролит обычно получают методом сухого прессования с последующим высокотемпературным спеканием (Li C.и др., 2019). Чтобы выполнить сухое прессование для получения плотного керамического электролита, тонкоизмельченные порошки необходимо предварительно смешать с ~ 5 мас.% Поливинилового спирта, который легко создает микро- / макропоры после обработки для удаления связующего. Кроме того, давление на порошок в разных положениях в осевом направлении неодинаково, что приводит к неравномерной плотности и составу образца, полученного методом сухого прессования (Suvacı, Messing, 2001; Tanaka et al., 2006; Schiavo et al., 2018). . В качестве альтернативы можно выбрать коллоидный процесс для приготовления керамических электролитов с высокой относительной плотностью и хорошей однородностью состава (Lewis, 2004; Franks et al., 2017). При коллоидном формовании приготовление суспензий с высоким содержанием твердых веществ (> 50 об.%) И низкой вязкостью [<1 Па⋅с при скорости сдвига 100 с –1 (Tallon and Franks, 2011; Chen AN et al. ., 2020)] является ключевым фактором для непористого литья и плотной керамической подготовки. Следует отметить, что керамические электролиты обычно требуют осторожности при выборе растворителей, поскольку они могут вызвать нежелательную диффузию компонентов или реакцию (Li B. et al., 2017; Lim et al., 2018; Hitz et al., 2019).Другой частью кристаллического электролита является тио-ЛИЗИКОН (система Li 2 SP 2 S 5 ), который может достигать высокой ионной проводимости 10 -3 ∼10 -2 См см -1 из-за более поляризуемого электронного облака серы (Zhang et al., 2019; Shan et al., 2020). Процесс производства электролита тиолизикон аналогичен керамическому электролиту, хотя обычно требуется контролируемая инертная атмосфера из-за его чувствительности к воздуху (Manthiram et al., 2017). Кроме того, кристаллический электролит также может быть изготовлен с помощью тонкопленочной обработки, такой как импульсное лазерное осаждение (Fujimoto et al., 2015), химическое осаждение из паровой фазы (Gelfond et al., 2009), напыление (Lethien et al., 2011). ), золь-гель осаждение (Jung et al., 2001) и др.
Стекловидные электролиты привлекли большое внимание из-за их нескольких преимуществ по сравнению с кристаллическими материалами: изотропная ионная проводимость, отсутствие сопротивления границ зерен, легкость изготовления пленки, легкость модификации состава и т. Д.В общем, существует четыре основных метода обработки для образования стеклообразных электролитов: закалка расплава, механическое измельчение, золь-гель синтез и влажная химическая реакция. Метод закалки в расплаве включает начальный предварительный нагрев / плавление исходных материалов до температуры выше 900 ° C и последующее прессование / отжиг (Pradel et al., 1985). Это наиболее часто используемый метод производства стеклообразных и стеклокерамических электролитов. Из-за сильной склонности к кристаллизации некоторых составов стекла используется закалочное устройство с двумя валками для достижения высокой скорости охлаждения за счет уменьшения объема расплавленного стекла (Pradel et al., 1985; Minami et al., 2006). Недостатком метода закалки в расплаве являются высокие температуры и довольно сложная установка, которая может быть потенциально опасной. Благодаря простоте производственных процедур и способности улучшать измельчение / однородность при температуре и давлении окружающей среды, метод механического измельчения может быть легко применен для производства больших количеств хорошо перемешанных тонкодисперсных порошков при низких затратах. Однако процесс аморфизации во время измельчения действительно сильно зависит от времени, и для наблюдения аморфного гало на рентгенограммах может потребоваться до 20 часов (Morimoto et al., 1999; Hayashi et al., 2002). Метод золь-гель синтеза для производства стеклообразных электролитов включает в себя процесс контролируемого гидролиза, поликонденсации, гелеобразования и дегидратации (Hench and West, 1990). В зависимости от состава стекла различные алкоксиды металлов или неорганические соединения используются в качестве предшественников для смешивания с подходящим растворителем на стадии гидролиза. Следующая реакция конденсации затем формирует связь и связь для основы стеклянной сети (Hench and West, 1990). Благодаря реакции и перемешиванию в жидком состоянии золь-гель синтез может достигать высокой однородности при относительно низких температурах (Hench and West, 1990; Venkatasubramanian et al., 1991; Данн и др., 1994). Подобно процедурам золь-гель-синтеза, метод влажной химической реакции позволяет получить желаемую композицию посредством перегруппировки молекулы / связывания во время реакции в жидком состоянии. Органические соединения обычно используются в качестве растворителя для растворения исходных химикатов (Teragawa et al., 2014; Phuc et al., 2016; Choi et al., 2017).
Стеклокерамические электролиты представляют собой класс материалов со смесью как аморфной, так и микрокристаллической микроструктуры, которую обычно получают путем контролируемой нуклеации и кристаллизационной обработки соответствующего стекломатериала при температуре выше температуры стеклования (Варшнея и Мауро, 2019).Подобно обычным технологиям производства стеклообразных электролитов, во многих предыдущих публикациях сообщалось о стеклокерамических электролитах, полученных закалкой в расплаве или механическим измельчением с последующей стадией отжига (Hayashi et al., 2003; Trevey et al., 2009; Tatsumisago and Хаяси, 2012). Однако температура и время отжига могут повлиять на структурное устройство кристаллических фаз и повлиять на ионную проводимость (Xie et al., 2009). Об использовании золь-гель-синтеза и методов влажной химической реакции для получения ИСЭ из стеклокерамики также сообщалось в нескольких недавних работах (Kotobuki et al., 2013; Teragawa et al., 2014; Ли и др., 2015; Ma et al., 2016; Phuc et al., 2016).
Хотя ISE предлагают многочисленные преимущества в технологии твердотельных аккумуляторов, их хрупкая природа создает многочисленные проблемы обработки и интеграции. После изготовления ISE обычно требуется дополнительная обработка, такая как шлифовка или резка, чтобы получить желаемые формы для объединения с электродными слоями. Однако многие материалы ISE неизбежно сталкиваются с дилеммой перекрестного химического загрязнения или структурного повреждения во время последующей обработки.Например, керамические электролиты могут разрушаться во время резки, а электролиты из стекла / стеклокерамики могут иметь побочные реакции, связанные с водой или повышенной температурой во время шлифования / полировки. Следовательно, последующая обработка может значительно увеличить производственные затраты и продлить производственный цикл. Краткое изложение традиционных технологий производства SSE представлено в схемах на рисунке 2, где эти общие методы представляют аналогичные ограничения в достижении сложных форм-факторов, необходимых для будущих приложений для аккумуляторов.В этих условиях исследования SSE для 3D-печати привлекают все большее внимание из-за их способности достигать одноэтапного производства SSE с желаемыми форм-факторами. В обход многих дополнительных шагов, требуемых традиционными методами, в будущем полностью интегрированное производство твердотельной батареи может быть достигнуто с помощью 3D-печати. Далее в этом обзоре будут обсуждаться существующие стратегии 3D-печати для SSE, а затем подчеркнуты перспективы и возможность повышения производительности 3D-печатных SSE.
Рис. 2. Схема традиционных производственных стратегий с (A) Оптическое изображение твердого полимерного электролита на основе полиэтиленоксида (ПЭО). Воспроизведено из Chen C. et al. (2019) по лицензии Creative Commons Attribution. (B) Схема твердого композитного электролита, объединяющего Li 6,75 La 3 Zr 1,75 Ta 0,25 O 12 (LLZTO) и поливинилиденфторид (PVDF). Воспроизведено с книги Чжан X.и другие. (2017) с разрешения John Wiley & Sons-Books. (C) Оптическое изображение пленки керамического электролита Li 0,34 La 0,56 TiO 3 (LLTO). Воспроизведено из Jiang et al. (2020) с разрешения John Wiley & Sons-Books.
Технологии 3D-печати
Аддитивное производство, то есть 3D-печать, относится к передовой технологии изготовления, при которой трехмерные объекты строятся послойно на основе файлов компьютерного проектирования (САПР) (Chen A.Н. и др., 2017; Мао и др., 2017). По сравнению с традиционным методом технология 3D-печати продемонстрировала уникальные преимущества в быстром создании прототипов очень сложных и точных структур. Это преимущество может значительно упростить процедуру изготовления и сократить отходы материала для снижения стоимости производства (Chen A.N. et al., 2018; Li M. et al., 2019). Кроме того, 3D-печать способна ослабить ограничения, присущие форм-фактору аккумуляторов, и преобразовать производство аккумуляторов от простого двухмерного к сложному трехмерному (Pang et al., 2019; Cheng et al., 2020; Ян и др., 2020). Учитывая вышеупомянутые преимущества, для производства SSE были применены несколько методов 3D-печати. Эти методы 3D-печати SSE можно разделить на следующие две категории: печать на основе прямой записи (DW) [например, прямая запись чернилами (DIW), струйная печать (IJP), аэрозольная струйная печать (AJP) и наплавленное нанесение. моделирование (FDM)] и печать на основе литографии [например, стереолитография (SL) и цифровая обработка света (DLP)]. Далее будут обсуждаться последние достижения в исследованиях стратегий 3D-печати SSE, начиная с аспектов выбора сырья, конверта сборки и разрешения печати.
3D-печать твердотельных электролитов на основе DW
Прямая рукопись чернилами
Прямая рукопись (DIW) является наиболее широко используемой техникой 3D-печати для производства SSE благодаря ее низкой стоимости, простоте в эксплуатации и широкому выбору сырья (металлы, полимеры и керамика) (Ambrosi and Pumera, 2016; Du et al. , 2017). Схема процесса DIW показана на рисунке 3A. В процессе печати вязкоупругие чернила на гелевой основе выдавливаются непосредственно из сопловой головки в виде непрерывной нити.Перемещая сопло вверх, можно создавать спроектированные трехмерные объекты путем последовательного послойного нанесения. После печати чернильные материалы быстро затвердевают под воздействием испарения растворителя, гелеобразования, фазовых изменений, вызванных температурой или растворителем (Naficy et al., 2014). Обычно разрешение печати объектов, напечатанных методом DIW, определяется диаметром сопла, который составляет от десятков до сотен микрометров. Для печати SSE с высоким разрешением (10–100 мкм) решающим фактором является высокопроизводительный состав краски.Печатная краска должна быть модулирована, чтобы обеспечить хорошее истончение при сдвиге, обеспечивающее плавный поток чернил через сопло, и требуется достаточно высокий предел текучести и модуль упругости, чтобы обеспечить сохранение формы экструдированных нитей (Chang et al., 2019 ).
Рисунок 3. Прямое рукописное письмо (DIW). (A) Схема и SEM-микроскопия гелевого электролита для Zn-MnO 2 микро-батареи. Воспроизведено из Ho et al. (2010) с разрешения IOP Publishing, Ltd. (B) Схематические и оптические изображения полимерного электролита для Li 4 Ti 5 O 12 -графеноксидная батарея. Воспроизведено из Fu et al. (2016) с разрешения John Wiley & Sons-Books. (C) Схема и СЭМ-микрофотография композитного твердого электролита (CSE) для гибких LIB (LiFePO 4 / CSE / Li 4 Ti 5 O 12 ). Воспроизведено из Blake et al. (2017) с разрешения John Wiley & Sons-Books. (D) СЭМ-микроскопия и оптическое изображение CSE для LIB с электродом MnO 2 . Воспроизведено из Cheng et al. (2018) с разрешения John Wiley & Sons-Books. (E) Схема и микрофотографии на сканирующем электронном микроскопе Li 7 La 3 Zr 2 O 12 (LLZ) керамический электролит для металлического Li-аккумулятора (Li / LLZ / Li). Воспроизведено Mcowen et al. (2018) с разрешения John Wiley & Sons-Books.
В 2010 году Ho et al.(2010). Как показано на рисунке 3A, SSE был зажат между электродами в микробатареи Zn-MnO 2 . Напечатанная ячейка показала емкость 0,98 мАч см –2 и плотность энергии 1,2 мВтч см –2 за более чем 70 циклов. Fu et al. (2016) печатные полимерные композитные электролитные чернила с регулируемой вязкостью для Li 4 Ti 5 O 12 -графеноксид (GO) встречно-штыревой батареи (Рисунок 3B). Отмечено, что хлопья GO регулировались для выравнивания вдоль направления экструзии в осажденных электродах, что могло улучшить электрическую проводимость и обеспечить достаточную площадь поверхности для размещения электролита.CSE были созданы для гибких LIB компанией DIW (рисунки 3C, D; Blake et al., 2017; Cheng et al., 2018). По сравнению с коммерческим полиолефиновым сепаратором напечатанные CSE продемонстрировали сопоставимые высокие электрохимические характеристики, лучшую термостабильность, смачиваемость электролитом и циклическую способность (Blake et al., 2017). Mcowen et al. (2018) подготовили керамический электролит Li 7 La 3 Zr 2 O 12 (LLZ) с различными микрометрическими характеристиками для металлической литиевой батареи (рис. 3E).Было доказано, что эти электролитные структуры обеспечивают батареи с хорошими механическими свойствами, более низким полным сопротивлением элементов и улучшенной энергией и удельной мощностью. О подобной работе DIW также сообщалось в других источниках (Braam et al., 2012; Wei et al., 2018; Ma and Devin Mackenzie, 2019). Основные преимущества DIW заключаются в широком выборе сырья и широком диапазоне размеров сборки (100 мкм – 10 см). Использование концентрированных вязкоупругих паст позволяет создавать трехмерные структуры без необходимости в опорах (например, порошковой подушке, емкости с жидкостью или печатных ручных опорах) (Chen Z.et al., 2019), что может упростить процесс печати, исключить процесс обработки поверхности и максимально использовать сырье. DIW хорошо изучен для производства индивидуальных пористых структур, обладающих периодическими характеристиками, с минимальным разрешением или без него. Однако приготовление вязкоупругих паст на гелевой основе для DIW является сложной задачей. Кроме того, особенности печати DIW ограничены структурами поленницы из-за форм экструдированного волокна, что свидетельствует о трудностях изготовления плотных структур.
Струйная печать
Струйная печать (IJP) — это метод бесконтактного нанесения материала на основе капель, который может напрямую выбрасывать микрокапли чернил через сопла на различных типах подложек для создания двумерных (2D) узоров (Dobrozhan et al., 2020). Схема процесса IJP показана на рисунке 4A. В качестве многообещающего метода был изучен IJP для печати на нескольких материалах, включая металл, полимеры, гелевые, белковые материалы и т. Д. (Fritzler and Prinz, 2017).Обычно чернила для IJP должны быть в разбавленной жидкой форме с достаточно низкой динамической вязкостью и поверхностным натяжением. Количественная характеристика, основанная на физических свойствах чернил, была предложена Дерби (2010) для оценки того, можно ли описать чернила как «пригодность для печати» для IJP: Z = 1/ Oh = ( γρα ) 1 / 2 / η , где Z — величина, обратная безразмерному числу, Oh — число Онезорге, α — характерная длина, представляющая радиус сопла, и ρ , η и γ — плотность, динамическая вязкость и поверхностное натяжение чернил соответственно.В случае 1 < Z <10 ожидается, что чернила будут производить стабильные капли, чтобы обеспечить процесс IJP.
Рисунок 4. Струйная печать (IJP). (A) Схема процесса IJP; (B) СЭМ поперечного сечения и картирование элементов пористого композитного LiFePO 4 электрода с печатными ионогелевыми электролитами; (C) Температурная ионная проводимость напечатанных ионогелей; (D) Гальваностатическое циклирование полуэлемента с использованием напечатанных ионогелей и LiFePO 4 и Li 4 Ti 5 O 12 пористых композитных электродов.Воспроизведено Delannoy et al. (2015) с разрешения Elsevier Science and Technology Journals.
Применение IJP для печати SSE было впервые описано в литературе Delannoy et al. (2015). Авторы нанесли ионогелевые чернила на основе диоксида кремния непосредственно на пористые композитные электроды, чтобы сформировать SSE для LIB (рис. 4A – D). Ионогель SSE показал высокую ионную проводимость, хорошее термическое сопротивление и отличную совместимость с пористыми электродами, что позволило изготавливать микро-LIB с высокой поверхностной емкостью и хорошими характеристиками электрохимического циклирования.Полная ячейка с использованием IJP-напечатанного ионогеля SSE с LiFePO 4 и Li 4 Ti 5 O 12 пористых композитных электродов продемонстрировала поверхностную емкость 300 мАч см –2 для более чем 100 циклов, что было более конкурентоспособны, чем у микроустройств, полученных с помощью дорогостоящего процесса физического осаждения из паровой фазы. В методе IJP диаметр сопла обычно меньше 5 мкм, что меньше, чем у DIW (от десятков до сотен микрометров).В этом случае IJP позволяет изготавливать спроектированные структуры с более высоким разрешением (5–20 мкм), что способствовало применению IJP в областях микроэлектроники и энергетических устройств. Однако объекты, напечатанные IJP, в основном ограничены двумерным пространством со строительной оболочкой от 50 мкм до 10 мм и не могут быть адаптированы для нанесения толстых рисунков из-за очень небольшого объема исходных чернил. Кроме того, IJP имеет ограниченную гибкость при изготовлении сложных структур (например, полых и выступающих) из-за трудностей при изготовлении подложки с использованием экструдированных разбавленных жидких чернил.Эти ограничения ограничили его дальнейшее применение.
Аэрозольная струйная печать
Аэрозольная струйная печать (AJP) — это относительно новый подход к бесконтактному нанесению, ориентированный в первую очередь на изготовление печатной электроники. Сырье (например, металлы, полимеры и керамика) для нанесения AJP должно быть в жидкой форме и распыляться с помощью пневматической или ультразвуковой аэрозоли в капли диаметром 1–5 мкм. Эти капли затем доставляются к субстрату потоком газа, чтобы сформировать желаемый узор (Mahajan et al., 2013). Схема процесса AJP показана на рисунке 5A. Разрешение печати AJP зависит не только от размера сопла, но и от плотности капель и их взаимодействия с подложкой (Hoey et al., 2012). AJP считается потенциальным конкурентом IJP в миллиметровом производстве, поскольку он позволяет бесконтактное нанесение на гибкие и трехмерные неплоские подложки, что невозможно для технологий IJP или DIW.
Рис. 5. Аэрозольная струйная печать (AJP). (A) Схема процесса AJP. Воспроизведено из Hoey et al. (2012) по лицензии Creative Commons Attribution. AJP для электролитов на основе полиэтиленоксида (PEO) в LIB с LiFePO 4 в качестве катода: (B) СЭМ микрофотография поперечного сечения электролитов на основе PEO; (C) Температурная проводимость электролитов на основе ПЭО; (D) Кривые разряда для аккумуляторов, созданных из печатного электролита на основе ПЭО при 45 ° C со вставкой для измерения при 75 ° C.Воспроизведено из Deiner et al. (2019) с разрешения John Wiley & Sons-Books.
Применение AJP для печати SSE было впервые описано в литературе Deiner et al. (2019). В этой работе представлен состав чернил, состоящий из ПЭО, дифтор (оксалат) бората лития и наночастиц Al 2 O 3 , подходящих для осаждения AJP (рисунки 5B – D). Результаты показали, что геометрия и транспортные свойства напечатанных SPE в основном чувствительны к химической идентичности аниона литиевой соли и соотношению EO: Li.LIB с нанесенными на AJP SPE могли быть разряжены при C / 15 с емкостью> 85 мАч g –1 при 45 ° C и 162 мАч g –1 при 75 ° C. По сравнению с IJP, AJP имеет следующие преимущества: (i) экструдированные чернила обеспечивают гораздо более высокую вязкость, больший размер частиц и содержание твердых частиц благодаря процессу распыления, который воспроизводит мелкие капли, (ii) он основан на непрерывном генерировании туман из капель диаметром 1–5 мкм, что указывает на более высокое разрешение печати (∼5 мкм) и скорость осаждения, чем в процессе IJP «капля по требованию», и (iii) непрерывный туман состоит из высокоплотных плотно сфокусированные капли демонстрируют прекрасную способность предотвращать засорение сопла.Однако масштабируемость системы осаждения, особенно для обработки больших площадей (с рабочей зоной> 3 мм), по-прежнему является сложной задачей для AJP из-за размера сопла и принадлежностей. Кроме того, стоимость дополнительных принадлежностей и сфокусированного потока газа в системе AJP обычно высока.
Моделирование наплавленного осаждения
Моделирование наплавленного осаждения (FDM) — это хорошо известный метод 3D-печати для создания сложных объектов как в промышленности, так и в академических кругах благодаря своей простоте и доступной машинной доступности (Bellini and Güçeri, 2003).Механизм формования FDM аналогичен механизму DIW, который основан на принципе экструдирования материала, в то время как их сырье и процесс подачи отличаются. Схема процесса FDM показана на рисунке 6A. Материалы для печати FDM должны быть твердыми и термопластичными в форме тонкой нити, которая может быть доставлена в экструзионную головку с помощью приводных колес. После экструзии из сопла термопластические материалы, нагретые до состояния стеклования, кристаллизуются и затвердевают, осаждаясь на подложке.Обычными термопластическими материалами, используемыми в технике FDM, являются нити из акрилонитрил-бутадиен-стирола и полимолочной кислоты (PLA), в которых PLA приобретает все большую популярность из-за своей экологически чистой природы. Несмотря на эти преимущества, метод FDM редко применялся для изготовления SSE из-за низкой ионной проводимости термопластов. Следовательно, разработка термопластичных материалов в форме нитей с высокой ионной проводимостью является ключом к производству SSE с помощью FDM.
Рисунок 6. Моделирование наплавленного осаждения (FDM). (A) Схема процесса FDM. Воспроизведено Klippstein et al. (2018) с разрешения John Wiley & Sons-Books. FDM для электролитов на основе полимолочной кислоты (PLA) в LIB (титанат лития / матрица PLA / оксид лития-марганца): (B) Отдельные компоненты монетного элемента, напечатанного на 3D-принтере; (C) Емкость и кулоновский КПД при плотности тока 20 мАg –1 для 100 циклов; (D) Оптическое изображение отпечатанной батареи, питающей светодиод; (E) SEM — поперечное сечение одной батареи для печати.Воспроизведено из Reyes et al. (2018) с разрешения Американского химического общества.
В 2018 году Reyes et al. (2018) впервые синтезировали филаменты электролита на основе PLA для печати методом FDM с наивысшей ионной проводимостью 0,031 мСм⋅см –1 путем вливания смеси этилметилкарбоната, пропиленкарбоната и LiClO 4 . Они также разработали материалы электродов из PLA для трехмерной печати полных LIB произвольной формы, таких как плоские элементы и встроенные батареи, используемые в носимых электронных устройствах, как показано на рисунках 6B – E.Однако напечатанная полная ячейка имеет более низкую кулоновскую эффективность (∼88,5% в течение первых 50 циклов) по сравнению с таковой у обычных LIB (∼95–99%) (Smith et al., 2010). FDM предлагает множество преимуществ, таких как низкая стоимость печати, возможности большого размера (максимальный размер сборки ~ 10 см) и, в частности, возможность печати структуры из нескольких исходных материалов. Тем не менее, все еще существует несколько ограничений на производство SSE с помощью FDM: (i) материалы для печати ограничены термопластами и должны быть сформированы в нити, (ii) термопластические нити должны быть нагреты до состояния стеклования при высокой температуре 150 ° C. –180 ° C, и (iii) разрешение печати FDM вместе с осью Z составляет от 50 до 200 мкм, что приводит к плохому качеству поверхности и управляемости структуры.
Трехмерная печать твердотельных электролитов на основе литографии
Стереолитография
Стереолитография (SL) считается наиболее известной и популярной техникой 3D-печати и применяется для изготовления деталей из полимеров, керамики и стекла (Eckel et al., 2016; Ngo et al., 2018; Santoliquido et al. , 2019). Схема процесса SL показана на рисунке 7A. SL позволяет изготавливать сложные трехмерные микрорешетки путем избирательной полимеризации и отверждения фотоотверждаемой смолы с использованием источника света определенной длины волны (обычно в УФ-диапазоне) (Chartrain et al., 2018). Процесс полимеризации обычно протекает на поверхности жидкости. После завершения одного слоя полимеризации чан или платформа, поддерживающая строительную часть, поднимается или опускается на толщину слоя. Иногда требуется лезвие, чтобы выровнять поверхность жидкости перед полимеризацией следующего слоя. Фотоотверждаемая смола SL состоит в основном из фотоактивных мономеров и других добавок в очень небольших количествах, особенно фотоинициатора (Manapat et al., 2017). По сравнению с техникой 3D-печати на основе DW (например.g., DIW, IJP, AJP и FDM), SL может изготавливать произвольную трехмерную геометрию, включая различные полые резные детали с высоким разрешением вплоть до микрометрового масштаба, и может устранить ограничения, связанные с траекторией инструмента и последовательной экструзией (Yang et al. ., 2016). Следовательно, SL имеет высокий потенциал для изготовления различных типов SSE, включая SPE, CSE и ISE.
Рисунок 7. Стереолитография (SL). (A) Схема процесса SL. Воспроизведено из Gross et al.(2014) с разрешения Американского химического общества. SL для твердотельных электролитов (SSE): (B) Процесс трафаретной печати с использованием УФ-отверждения твердых полимерных электролитов (SPE, = этоксилированный триметилолпропантриакрилатный мономер / высококипящий электролит / наночастицы Al 2 O 3 ) тонкий слой для LIB [LiFePO 4 (LFP) / SPE / Li 4 Ti 5 O 12 (LTO)]. Воспроизведено с книги Kim S.H. и другие. (2015) с разрешения Американского химического общества. (C) Оптическое изображение и трехмерная структура ТФЭ на основе полиэтиленгликоля для микро-LIB (LFP / SPE / LTO). Воспроизведено из Chen Q. et al. (2017) с разрешения IOP Publishing, Ltd. (D) Схематические и SEM-изображения 3D-печатных шаблонов с кубической, гироидной, алмазной и бижелевой микроархитектурой Li 1,4 Al 0,4 Ge 1,6 (PO 4 ) 3 (LAGP) -эпоксидные электролиты для литий-металлических аккумуляторов с симметричными литиевыми электродами.Воспроизведено Zekoll et al. (2018) с разрешения Королевского химического общества. (E) Оптическое изображение, изображения SEM и кривые зависимости напряжения / мощности-тока от манганита лантана-стронция (LSM-YSZ) / YSZ / Ni-YSZ твердооксидных элементов. Воспроизведено из Pesce et al. (2020) под непортированной лицензией Creative Commons Attribution 3.0, опубликованной Королевским химическим обществом.
В 2015 году Kim S.H. и другие. (2015) подготовили слой SPE и электроды, встроенные в матрицу SPE на произвольных объектах, а затем собрали в многослойные гибкие LIB в различных форм-факторах (рис. 7B).Напечатанные батареи продемонстрировали хорошую способность длительного хранения заряда и средний уровень объемной плотности энергии. Chen Q. et al. (2017) разработали УФ-отверждаемую смолу на основе полиэтиленгликоля для SL-печати гелевого полимерного электролита 3D для микро-LIB дешевым и высокопроизводительным способом. Как показано на рисунке 7C, напечатанный зигзагообразный GPE может увеличить площадь контакта с электродами, а улучшенная ионная проводимость 4,8 × 10 –3 См см –1 может быть получена при температуре окружающей среды, что сравнимо с что жидкого электролита.Zekoll et al. (2018) сообщили о SL-печатных CSE, содержащих трехмерный бинепрерывный Li 1,4 Al 0,4 Ge 1,6 (PO 4 ) 3 (LAGP) керамический электролит и изолирующий полимер (эпоксидный полимер, полипропилен) для Li металлический аккумулятор (рис. 7D). Этот метод может точно контролировать соотношение керамики и полимера, а также геометрию и размер разнообразных точных микроархитектур, таких как кубические, гироидные, алмазные и бижелевые структуры. Гироидный LAGP-эпоксидный электролит имел ионную проводимость 1.6 × 10 –4 См см –1 , что было того же порядка величины, что и таблетка LAGP, в то время как печатный электролит продемонстрировал на 28% более высокую прочность на сжатие и до пяти раз большую прочность на изгиб. Недавняя работа, опубликованная Pesce et al. (2020) разработали самоподдерживающиеся цельнокерамические электролиты из 8 мол.% Оксида циркония, стабилизированного оксидом иттрия (YSZ), для твердооксидного топливного элемента (SOFC), напечатанного SL (рис. 7E). Напечатанные плотные и не содержащие трещин электролиты 8YSZ достигли ионной проводимости до 3.0 × 10 –2 См –1 при 800 ° C в плоской и гофрированной геометриях. Гофрированные электролиты YSZ с печатью SL показали увеличение удельной мощности на 57% (410 мВт · см –2 при 900 ° C) по сравнению с традиционной технологией SOFC, что в основном было связано с геометрическими аспектами с высоким аспектным отношением. SL продемонстрировал множество преимуществ, таких как высокое разрешение печати (10–100 мкм) и качество поверхности. Кроме того, SL имеет большой потенциал в подготовке SSE для многомасштабных батарей, особенно для батарей микронного размера.Однако доступность светочувствительных смол или полимеров-предшественников для печати SL ограничена и является дорогостоящей (около 100 долл. США / кг для светочувствительных смол и более дорого для предшественников), а для печати полых или нависающих структур требуются ручные опоры.
Цифровая обработка света
Цифровая обработка света (DLP) — это метод SL на основе маски, использующий цифровое микрозеркальное устройство (DMD) для проецирования световой маски, которая служит для затвердевания всего слоя за несколько секунд (Chartrain et al., 2018). Механизм формования и сырье DLP аналогичны SL. Схема процесса DLP показана на рисунке 8A. В системе DLP DMD представляет собой массив из нескольких миллионов микроскопически маленьких зеркал на полупроводниковом кристалле, и каждое зеркало представляет один или несколько пикселей в проецируемом изображении (Han et al., 2019). В этом случае разрешение печати DLP связано с количеством зеркал в DMD. Слоистое затвердевание в DLP предлагает многочисленные преимущества по сравнению с процессом точечного сканирования SL: (i) время построения значительно сокращается, поскольку оно в основном зависит от толщины слоя и времени воздействия, и (ii) остаточное напряжение DLP образцов мало, поскольку не существует разницы между контуром и внутренней областью во время затвердевания слоя.Эти преимущества привлекли значительное внимание при изготовлении плотной керамики в различных областях, включая керамические электролиты для ТОТЭ.
Рисунок 8. Цифровая обработка света (DLP). (A) Схема процесса DLP. Воспроизведено из Luongo et al. (2020) с разрешения John Wiley & Sons-Books. DLP для полностью плотного электролита из диоксида циркония, стабилизированного оксидом иттрия (8YSZ), с концентрацией 8 мол.% В твердооксидном топливном элементе (NiO-8YSZ / 8YSZ / La 0,8 Sr 0.2 MnO 3 ): (B) SEM-изображения напечатанного YSZ под разными углами; (C) SEM-изображения волнообразного YSZ; (D) Кривые напряжения и плотности тока для полных волнообразных ячеек. Воспроизведено из Xing et al. (2020) с разрешения Elsevier Science & Technology Journals.
Самая последняя работа по производству керамического электролита методом DLP была проведена Xing et al. (2020). Чтобы улучшить характеристики ТОТЭ, был разработан полностью плотный электролит YSZ с концентрацией 8 моль% с волнообразной формой и приготовленный методом DLP с различными углами печати (0 °, 15 °, 30 °, 45 °) (Рисунки 8B, C).Этот напечатанный специальный электролит может увеличить границу раздела электрод-электролит на ~ 36% и, таким образом, повысить удельную мощность на ~ 32% при температуре испытания 800 ° C и на ~ 37% при 700 ° C по сравнению с эталонным электродом. ячейка (рис. 8D). Эта работа продемонстрировала потенциал для производства конкретных шаблонных SSE с помощью DLP для изготовления SOFC с улучшенными и предсказуемыми характеристиками. DLP имеет сопоставимое с SL разрешение печати (10–100 мкм) и качество поверхности, но значительно сокращает время сборки и меньшее остаточное напряжение, что позволяет изготавливать высоконадежные SSE с высокой эффективностью.Однако дорогостоящие светочувствительные смолы / прекурсоры и ручные опоры по-прежнему являются проблемами, с которыми сталкивается DLP.
В последние годы были разработаны различные методы трехмерной печати на основе литографии, такие как двухфотонная полимеризация (TPP) (Truby and Lewis, 2016), непрерывное производство поверхности раздела жидкостей (CLIP) (Tumbleston et al., 2015) и проектирование Микростереолитография (PμSL) (Park et al., 2012), все они могут обеспечить сопоставимое или более высокое разрешение печати, чем 10–100 мкм (рис. 9).CLIP имеет разрешение печати 50 ~ 100 мкм, в то время как детали могут быть извлечены непосредственно из смолы за считанные минуты с использованием проницаемого для кислорода окна (Tumbleston et al., 2015). PμSL может обеспечить разрешение печати 2-8,5 мкм, используя трехмерный полутоновый DMD в качестве динамической маски и уменьшающую линзу в качестве пространственного модулятора света (Sun et al., 2005). В частности, TPP позволяет создавать элементы размером менее 1 мкм за счет одновременного поглощения двух фотонов ближнего инфракрасного (780 нм) или зеленого (515 нм) лазера (Obata et al., 2013). Эта основанная на литографии технология 3D-печати имеет высокий потенциал для изготовления SSE с тонкими характеристиками от сотен нанометров до микрон.
Рис. 9. Сравнение разрешающей способности печати для метода 3D-печати на основе литографии [стереолитография (SL), цифровая обработка света (DLP), непрерывное создание интерфейса жидкости (CLIP), проекционная микростереолитография (PμSL) и двухфотонная полимеризация ( ТЭС)]. SL воспроизведен из Jansen et al.(2009) с разрешения Американского химического общества. DLP воспроизведен из Lee et al. (2007) с разрешения Американского химического общества. CLIP воспроизведен из Tumbleston et al. (2015) с разрешения Американской ассоциации развития науки. PμSL воспроизведен из Lee et al. (2008) с разрешения John Wiley & Sons-Books. TPP воспроизведено из Obata et al. (2013) по лицензии Creative Commons.
Заключение и перспективы
В этом обзоре мы сначала обсудили общие процессы и ограничения традиционных методов производства SSE.Затем, посредством всестороннего обзора двух больших групп методов 3D-печати, основанных либо на DW, либо на SL, мы указали на преимущества новых технологий 3D-печати по сравнению с традиционными методами производства SSE с точки зрения построения механизмов, выбора сырья, построения конверт, разрешение печати и приложение (наноразмерные, гибкие и крупномасштабные аккумуляторные решетки). Мы подчеркнули перспективы и осуществимость производства SSE с использованием трехмерной печати на основе литографии, чтобы преодолеть технические барьеры и улучшить совместимость интерфейсов твердое тело-твердое тело.Наконец, мы обсудили несколько существующих проблем, связанных с процессом 3D-печати, и соответствующие будущие перспективы для лучшего решения этих проблем, стремясь предоставить руководство, которое будет стимулировать развитие технологий 3D-печати, более тесно связанных с производством аккумуляторов. В целом, за эволюцией аккумуляторов устойчивой движущей силой всегда были постоянно совершенствующиеся и совершенствующиеся технологии производства.
Учитывая преимущества высокого разрешения печати, гибкого изготовления очень сложных структур и широкого выбора сырья, технология 3D-печати продемонстрировала свой большой потенциал для производства различных типов и форм-факторов SSE.Однако есть еще несколько проблем, которые следует решить, а именно: (i) проблемы при производстве SSE, чувствительных к воздуху / влаге. В большинстве технологий 3D-печати используется сырье в жидкой или чернильной форме, такое как DIW, IJP и AJP, (ii) ограничения при производстве с высоким разрешением (вплоть до наномасштаба). Например, нано-LIB для биомедицинских приложений и SSE в форме нанометрового гребня для снижения внутреннего сопротивления, (iii) проблемы при производстве SSE для приложений масштаба сети.Например, ТОТЭ и крупномасштабные аккумуляторные сети для хранения возобновляемой энергии и (iv) потенциальные проблемы при последующей обработке ISE. Например, напряжение, трещины, летучесть лития и побочные реакции легко вызываются во время длительного времени (удаления связующего или спекания) (Nyman et al., 2010; Pfenninger et al., 2019). Для решения вышеупомянутых проблем настоятельно рекомендуются дальнейшие усилия в следующих аспектах: (i) объединить технологию 3D-печати и традиционное производство аккумуляторов, чтобы способствовать разработке полупроводниковых аккумуляторов с высокой плотностью энергии, (ii) повысить разрешение печати. вплоть до нанометра с использованием новых нанотехнологий, (iii) разработка принтеров промышленного уровня или конвейерной печатной платформы для производства SSE для приложений в масштабе сетки и (iv) объединение некоторых инновационных технологий спекания, совместимых со сложными деталями, напечатанными на 3D-принтере.
Этот обзор продемонстрировал возможность производства SSE с помощью 3D-печати, но требуются дополнительные усилия, чтобы полностью преодолеть разрыв между текущими технологическими возможностями и будущими производственными требованиями. Хотя 3D-печать предлагает беспрецедентную гибкость в регулировке структурной размерности и сложности SSE по сравнению с традиционными методами, ее не следует ошибочно принимать за всемогущее решение многих неотъемлемых препятствий при производстве аккумуляторов. Чтобы реализовать больший потенциал применения 3D-печати в производстве аккумуляторов, требуются совместные междисциплинарные усилия.С точки зрения материаловедения, необходимы дальнейшие экспериментальные и вычислительные исследования для систематического изучения отношений состав-структура-свойство SSE. Это должно способствовать достижению более высоких плотностей тока и лучшей механической / химической стабильности аккумуляторного элемента. Углубляясь в механизмы реакции с электрохимической точки зрения, можно исследовать и оптимизировать кинетику переноса ионов на границах раздела электрод / электролит, чтобы повысить эффективность переноса проводящего иона.За счет более комплексного проектирования в машиностроении можно было бы интегрировать специальные приспособления для чувствительных к воздуху / влаге образцов в существующие инструментальные установки 3D-печати, чтобы обеспечить более широкий выбор материалов. В целом технология 3D-печати использовала многие преимущества традиционных методов производства на протяжении многих лет. Благодаря совместным усилиям междисциплинарных исследований, 3D-печать с оптимизмом надеется вскоре реализовать весь свой потенциал в производстве SSE. Мы считаем, что широкое распространение технологий 3D-печати должно быть сосредоточено не только на производственном процессе, но и в таких дисциплинах, как химия поверхности, материаловедение и машиностроение.Например, ограниченная доступность и высокая стоимость фоточувствительных смол или полимеров-предшественников для печати (выше 100 долларов за килограмм) для SL заставят нас разрабатывать новые материалы для печати SL с низкой стоимостью и широкой совместимостью с материалами. Плохая совместимость интерфейса твердое тело / твердое тело подтолкнет нас к исследованию модификации поверхности и структурного дизайна SSE с сильным межчастичным взаимодействием и низким импедансом интерфейса. Кроме того, некоторые особые требования (такие как инертная атмосфера и сухая среда) заставят нас разработать особую технику 3D-печати для производства батарей.Следовательно, применение 3D-печати SSE в будущем потребует совместной разработки нескольких дисциплин, таких как химия поверхности, материаловедение и машиностроение.
Авторские взносы
ФС и Ю.С.: концепция или дизайн работы и критическая доработка статьи. AC и CQ: подготовка статьи. Все авторы внесли свой вклад в статью и одобрили представленную версию.
Финансирование
FS выражает признательность за поддержку фонда запуска со стороны Департамента энергетики и разработки полезных ископаемых Университета штата Пенсильвания.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Сокращения
2D, двухмерный; AJP, аэрозольная печать; CLIP, непрерывное производство поверхности раздела жидкостей; CSE, композитные твердые электролиты; DIW, прямое рукописное письмо; DLP, цифровая обработка света; DMD, цифровое микрозеркальное устройство; DW, прямое письмо; FDM, моделирование наплавленного металла; GO, оксид графена; IJP, струйная печать; ISE, неорганический твердый электролит; ЛАГП, Ли 1.4 Al 0,4 Ge 1,6 (PO 4 ) 3 ; LFP, LiFePO 4 ; LIB, литий-ионные батареи; LLZ, Li 7 La 3 Zr 2 O 12 ; LTO, Li 4 Ti 5 O 12 ; P μ SL, проекционная микростереолитография; PLA, полимолочная кислота; SL, стереолитография; ТОТЭ, твердооксидный топливный элемент; ТПЭ, твердый полимерный электролит; SSE, твердотельный электролит; TPP, двухфотонная полимеризация; УФ, ультрафиолет; YSZ, оксид циркония, стабилизированный оксидом иттрия.
Список литературы
Appetecchi, G. B., Alessandrini, F., Carewska, M., Caruso, T., Prosini, P. P., Scaccia, S., et al. (2001). Исследование аккумуляторов с литий-полимерным электролитом. J. Источники энергии 97, 790–794.
Google Scholar
Беллини А. и Гючери С. (2003). Механические характеристики деталей, изготовленных с использованием моделирования наплавкой. Rapid Prototyp. J. 9, 252–264. DOI: 10.1108 / 13552540310489631
CrossRef Полный текст | Google Scholar
Блейк, А.J., Kohlmeyer, R.R., Hardin, J.O., Carmona, E.A., Maruyama, B., Berrigan, J.D., et al. (2017). Керамически-полимерные электролиты для 3D-печати для гибких высокопроизводительных литий-ионных аккумуляторов с повышенной термостойкостью. Adv. Energy Mater. 7: 1602920. DOI: 10.1002 / aenm.201602920
CrossRef Полный текст | Google Scholar
Бланга Р., Бурштейн Л., Берман М., Гринбаум С. Г., Голодницкий Д. (2015). Твердый полимер-керамический электролит, полученный электрофоретическим осаждением. J. Electrochem. Soc. 162, D3084 – D3089.
Google Scholar
Браам, К. Т., Фолькман, С. К., и Субраманиан, В. (2012). Определение характеристик и оптимизация печатной первичной серебряно-цинковой батареи. J. Источники энергии 199, 367–372. DOI: 10.1016 / j.jpowsour.2011.09.076
CrossRef Полный текст | Google Scholar
Бухманн, И. (2001). Батареи в портативном мире: Справочник по аккумуляторным батареям для не инженеров .Ричмонд: Cadex Electronics.
Google Scholar
Карли М. Д., Касо М. Ф., Аврора А., Сета Л. Д. и Просини П. П. (2019). «Электроформование нановолокон в качестве сепараторов для литий-ионных аккумуляторов», в: Труды 15-й Международной конференции по фотоэлектрическим системам концентраторов (CPV-15) Мелвилл, штат Нью-Йорк.
Google Scholar
Кавальер, С., Субианто, С., Савич, И., Джонс, Д. Дж., Розьер, Дж. Дж. Э., и Science, E. (2011). Электропрядение: разработанные архитектуры для устройств преобразования и хранения энергии. Energy Environ. Sci. 4, 4761–4785. DOI: 10.1039 / c1ee02201f
CrossRef Полный текст | Google Scholar
Чанг, П., Мэй, Х., Чжоу, С., Дассиос, К. Г., и Ченг, Л. (2019). Электрохимические накопители энергии, напечатанные на 3D-принтере. J. Mater. Chem. А 7, 4230–4258. DOI: 10.1039 / c8ta11860d
CrossRef Полный текст | Google Scholar
Чартрейн, Н. А., Уильямс, К. Б., и Уиттингтон, А. Р. (2018). Обзор изготовления тканевых каркасов с использованием фотополимеризации в ванне. Acta Biomater. 74, 90–111. DOI: 10.1016 / j.actbio.2018.05.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Chen, A.-N., Li, M., Wu, J.-M., Cheng, L.-J., Liu, R.-Z., Shi, Y.-S., et al. (2019). Механизм повышения механических характеристик высокопористой муллитовой керамики с бимодальной структурой пор, полученных методом селективного лазерного спекания. J. Alloys Compd. 776, 486–494. DOI: 10.1016 / j.jallcom.2018.10.337
CrossRef Полный текст | Google Scholar
Чен, А.-N., Li, M., Xu, J., Lou, C.-H., Wu, J.-M., Cheng, L.-J., et al. (2018). Пенопласт из муллитовой керамики с высокой пористостью, полученный методом селективного лазерного спекания с использованием полых сфер летучей золы в качестве сырья. J. Eur. Ceram. Soc. 38, 4553–4559. DOI: 10.1016 / j.jeurceramsoc.2018.05.031
CrossRef Полный текст | Google Scholar
Chen, A.-N., Wu, J.-M., Cheng, L.-J., Liu, S.-J., Ma, Y.-X., Li, H., et al. (2020). Повышенное уплотнение и диэлектрические свойства керамики CaTiO3-0,3NdAlO3, полученной методом прямого коагуляционного литья. J. Eur. Ceram. Soc. 40, 1174–1180. DOI: 10.1016 / j.jeurceramsoc.2019.12.033
CrossRef Полный текст | Google Scholar
Chen, A.-N., Wu, J.-M., Liu, K., Chen, J.-Y., Xiao, H., Chen, P., et al. (2017). Высокопроизводительные керамические детали сложной формы, полученные методом селективного лазерного спекания: обзор. Adv. Прил. Ceram. 117, 100–117. DOI: 10.1080 / 17436753.2017.1379586
CrossRef Полный текст | Google Scholar
Чен, К., Сюй, Р., Хэ, З., Чжао, К., и Пан, Л. (2017). Печать 3D гелевого полимерного электролита в литий-ионной микробатареи с использованием стереолитографии. J. Electrochem. Soc. 164, A1852 – A1857.
Google Scholar
Chen, W., Lei, T., Wu, C., Deng, M., Gong, C., Hu, K., et al. (2018). Разработка безопасных систем электролита для высокостабильной литий-серной батареи. Adv. Energy Mater. 8: 1702348. DOI: 10.1002 / aenm.201702348
CrossRef Полный текст | Google Scholar
Чен, Ю., Чжо, С., Ли, З., и Ван, К. (2020). Редокс-полимеры для аккумуляторных металло-ионных аккумуляторов. EnergyChem 2: 100030. DOI: 10.1016 / j.enchem.2020.100030
CrossRef Полный текст | Google Scholar
Chen, Z., Li, Z., Li, J., Liu, C., Lao, C., Fu, Y., et al. (2019). 3D-печать керамики: обзор. J. Eur. Ceram. Soc. 39, 661–687.
Google Scholar
Ченг, М., Дейванаягам, Р., и Шахбазян-Яссар, Р. (2020). 3D-печать электрохимических накопителей энергии: обзор методов печати и архитектур электродов / электролитов. Тесто. Supercaps 3, 130–146. DOI: 10.1002 / batt.201
0CrossRef Полный текст | Google Scholar
Cheng, M., Jiang, Y., Yao, W., Yuan, Y., Deivanayagam, R., Foroozan, T., et al. (2018). Трехмерная печать гибридного твердотельного электролита для литий-ионных аккумуляторов при повышенных температурах. Adv. Матер. 30: e1800615.
Google Scholar
Чой, Ю. Э., Пак, К. Х., Ким, Д. Х., О, Д. Й., Квак, Х. Р., Ли, Ю. Г. и др. (2017). Покрываемые твердые электролиты Li4SnS4, приготовленные из водных растворов, для полностью твердотельных литий-ионных аккумуляторов. ChemSusChem 10, 2605–2611. DOI: 10.1002 / cssc.201700409
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Commarieu, B., Paolella, A., Daigle, J.-C., and Zaghib, K. (2018). На пути к высокой литиевой проводимости в твердотельных полимерных и полимерно-керамических батареях. Curr. Opin. Электрохим. 9, 56–63. DOI: 10.1016 / j.coelec.2018.03.033
CrossRef Полный текст | Google Scholar
Cousseau, J.-F., Siret, C., Biensan, P., and Broussely, M.(2006). Последние разработки в литий-ионных призматических элементах. J. Источники энергии 162, 790–796. DOI: 10.1016 / j.jpowsour.2005.02.095
CrossRef Полный текст | Google Scholar
Дейнер, Л. Дж., Дженкинс, Т., Хауэлл, Т., и Роттмайер, М. (2019). Полимерные композитные электролиты с аэрозольной печатью для твердотельных литий-ионных аккумуляторов. Adv. Англ. Матер. 21: 1
2. DOI: 10.1002 / adem.2012CrossRef Полный текст | Google Scholar
Деланной, П.Э., Риу, Б., Лестриес, Б., Гийомар, Д., Брюсс, Т., и Ле Бидо, Дж. (2015). К быстрой и экономичной струйной печати твердого электролита для литиевых микробатареек. J. Источники энергии 274, 1085–1090. DOI: 10.1016 / j.jpowsour.2014.10.164
CrossRef Полный текст | Google Scholar
Deng, Z., Jiang, H., Hu, Y., Liu, Y., Zhang, L., Liu, H., et al. (2017). Трехмерная упорядоченная макропористая наноструктура MoS2 @ C для гибких литий-ионных аккумуляторов. Adv. Матер. 29: 1603020.DOI: 10.1002 / adma.201603020
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дерби, Б. (2010). Струйная печать функциональных и конструкционных материалов: требования к свойствам жидкости, стабильность характеристик и разрешение. Annu. Rev. Mater. Res. 40, 395–414. DOI: 10.1146 / annurev-matsci-070909-104502
CrossRef Полный текст | Google Scholar
Диуф Б. и Поде Р. (2015). Возможности литий-ионных аккумуляторов в возобновляемых источниках энергии. Обновить.Энергия 76, 375–380. DOI: 10.1016 / j.renene.2014.11.058
CrossRef Полный текст | Google Scholar
Дирикан, М., Янь, К., Чжу, П., и Чжан, X. (2019). Композитные твердые электролиты для твердотельных литиевых батарей. Mater. Sci. Англ. R Rep. 136, 27–46.
Google Scholar
Доброжан О., Пшеничный Р., Воробьев С., Курбатов Д., Команицкий В., Опанасюк А. (2020). Влияние термического отжига на морфологические и структурные свойства пленок ZnO, нанесенных на полиимидные подложки методом струйной печати. SN Прил. Sci. 2: 365.
Google Scholar
Ду, К.-Ф., Лян, К., Ло, Ю., Чжэн, Ю., и Янь, К. (2017). Последние достижения в области печати аккумуляторных батарей. J. Mater. Chem. А 5, 22442–22458. DOI: 10.1039 / c7ta07856k
CrossRef Полный текст | Google Scholar
Дадни, Н. Дж. (2008). Тонкопленочные микробатареи. Electrochem. Soc. Интерфейс 17, 44–48.
Google Scholar
Данн, Б., Фаррингтон, Г.К. и Кац Б. (1994). Золь-гель подходы для твердых электролитов и электродных материалов. Твердотельный ион. 70, 3–10. DOI: 10.1016 / 0167-2738 (94) -x
CrossRef Полный текст | Google Scholar
Экель, З. К., Чжоу, К., Мартин, Дж. Х., Якобсен, А. Дж., Картер, В. Б., и Шедлер, Т. А. Дж. С. (2016). Аддитивное производство керамики на основе полимеров. Наука 351, 58–62. DOI: 10.1126 / science.aad2688
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фергус, Дж.W. (2010). Керамические и полимерные твердые электролиты для литий-ионных аккумуляторов. J. Источники энергии 195, 4554–4569. DOI: 10.1016 / j.jpowsour.2010.01.076
CrossRef Полный текст | Google Scholar
Фрэнкс, Г. В., Таллон, К., Стударт, А. Р., Сессо, М. Л., и Лео, С. (2017). Коллоидная обработка: создание керамики сложной формы с уникальной многомасштабной структурой. J. Am. Ceram. Soc. 100, 458–490. DOI: 10.1111 / jace.14705
CrossRef Полный текст | Google Scholar
Фрицлер, К.Б., Принц В. Ю., Дж. П. У. (2017). Методы 3D-печати микро- и наноструктур. Phys. Успехи. 62, 54–69. DOI: 10.3367 / ufne.2017.11.038239
CrossRef Полный текст | Google Scholar
Fu, K., Wang, Y., Yan, C., Yao, Y., Chen, Y., Dai, J., et al. (2016). Электродные чернила на основе оксида графена для литий-ионных аккумуляторов, напечатанных на 3D-принтере. Adv. Матер. 28, 2587–2594. DOI: 10.1002 / adma.201505391
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фудзимото, Д., Кувата, Н., Мацуда, Ю., Кавамура, Дж., И Канг, Ф. (2015). Изготовление твердотельных тонкопленочных аккумуляторов с использованием тонких пленок LiMnPO 4, нанесенных методом импульсного лазерного осаждения. Тонкие твердые пленки 579, 81–88. DOI: 10.1016 / j.tsf.2015.02.041
CrossRef Полный текст | Google Scholar
Фурукава, Н., Иноуэ, К., и Мураками, С. (1984). Щелочная батарея. Google Patents.
Google Scholar
Гельфонд Н.В., Бобренок О.Ф., Предтеченский М.Р., Морозова, Н. Б., Жерикова, К. В., Игуменов, И. К. (2009). Химическое осаждение из газовой фазы тонких пленок электролитов на основе оксида циркония, стабилизированного оксидом иттрия. Inorg. Матер. 45, 659–665.
Google Scholar
Гуденаф, Дж. Б., и Сингх, П. (2015). Обзор — твердые электролиты в перезаряжаемых электрохимических элементах. J. Electrochem. Soc. 162, A2387 – A2392.
Google Scholar
Greatbatch, W., and Holmes, C.F. (1991). История имплантируемых устройств. IEEE Eng. Med. Биол. Mag. 10, 38–41.
Google Scholar
Гросс, Б. К., Эркал, Дж. Л., Локвуд, С. Ю., Чен, К., и Спенс, Д. М. Дж. А. С. (2014). Оценка 3D-печати и ее потенциального воздействия на биотехнологии и химические науки. 86, 3240–3253. DOI: 10.1021 / ac403397r
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хафнер, С., Гатри, Х., Ли, С.-Х., и Бан, К. (2019). Синхронизированная технология электроспиннинга и электрораспыления для производства твердотельных литий-ионных аккумуляторов. J. Источники энергии 431, 17–24. DOI: 10.1016 / j.jpowsour.2019.05.008
CrossRef Полный текст | Google Scholar
Хаяси А., Охтомо Т., Мидзуно Ф., Таданага К. и Тацумисаго М. (2003). Полностью твердотельные Li / S аккумуляторы с высокопроводящими стеклокерамическими электролитами. Electrochem. Commun. 5, 701–705. DOI: 10.1016 / s1388-2481 (03) 00167-x
CrossRef Полный текст | Google Scholar
Хаяси А., Ямасита Х., Тацумисаго М. и Минами Т.(2002). Характеристика аморфных твердых электролитов Li2S – SiS2 – LixMOy (M = Si, P, Ge), полученных закалкой расплава и механическим измельчением. Твердотельный ион. 148, 381–389. DOI: 10.1016 / s0167-2738 (02) 00077-2
CrossRef Полный текст | Google Scholar
He, P., Chen, Q., Yan, M., Xu, X., Zhou, L., Mai, L., et al. (2019). Создание лучших цинк-ионных аккумуляторов: перспективы материалов. EnergyChem 1: 100022. DOI: 10.1016 / j.enchem.2019.100022
CrossRef Полный текст | Google Scholar
Хенч, Л.Л. и Уэст Дж. К. (1990). Золь-гель процесс. Chem. Ред. 90, 33–72.
Google Scholar
Hitz, G. T., Mcowen, D. W., Zhang, L., Ma, Z., Fu, Z., Wen, Y., et al. (2019). Высокоскоростное циклирование лития в масштабируемой трехслойной архитектуре литий-гранат-электролит. Mater. Сегодня 22, 50–57. DOI: 10.1016 / j.mattod.2018.04.004
CrossRef Полный текст | Google Scholar
Хо, К. К., Эванс, Дж. У. и Райт, П. К. (2010). Прямая печать с диспенсером для цинковой микробатареи с ионным жидким гелевым электролитом. J. Micromech. Microeng. 20: 104009. DOI: 10.1088 / 0960-1317 / 20/10/104009
CrossRef Полный текст | Google Scholar
Хои, Дж. М., Лутфурахманов, А., Шульц, Д. Л., и Ахатов, И. С. (2012). Обзор прямой записи на основе аэрозолей и ее приложений для микроэлектроники. J. Nanotechnol. 2012, 1–22. DOI: 10.1155 / 2012/324380
CrossRef Полный текст | Google Scholar
Янсен, Дж., Мелчельс, Ф. П. У., Грийпма, Д. У., и Фейен, Дж.Дж. Б. (2009). Поли (D, L-лактид) / N-винил-2-пирролидон смолы, функционализированные моноэтиловым эфиром фумаровой кислоты, для получения каркасов тканевой инженерии с помощью стереолитографии. Биомакромолекулы 10, 214–220. DOI: 10.1021 / bm801001r
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Jiang, Z., Wang, S., Chen, X., Yang, W., Yao, X., Hu, X., et al. (2020). Ленточное литье пленок керамического электролита Li0,34La0,56TiO3 обеспечивает высокую плотность энергии литий-металлических батарей. Adv. Матер. 32: 11. DOI: 10.1002 / adma.2011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Йоханнесен, Э. А., Ван, Л., Вайз, К., Камминг, Д. Р., и Купер, Дж. М. (2006). Биосовместимость датчика «лаборатория на таблетке» в искусственных средах желудочно-кишечного тракта. IEEE Trans. Биомед. Англ. 53, 2333–2340. DOI: 10.1109 / tbme.2006.883698
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Иудез Х., Чжан Х., Ли, К., Эшету, Г. Г., Гонсалес-Маркос, Дж. А., Арманд, М., и др. (2017). Обзор — твердые электролиты для безопасных литий-серных батарей с высокой плотностью энергии: перспективы и проблемы. J. Electrochem. Soc. 165, A6008 – A6016.
Google Scholar
Юнг, Г. Б., Хуанг, Т., Хуанг, М. Х., и Чанг, К. Л. Дж. Дж. О. М. С. (2001). Получение легированного самарией оксида церия для твердооксидного электролита топливных элементов модифицированным золь-гель методом. J. Mater. Sci. 36, 5839–5844.
Google Scholar
Ким, Дж. Г., Сон, Б., Мукерджи, С., Шупперт, Н., Бейтс, А., Квон, О. и др. (2015). Обзор твердотельных батарей на литиевой и нелитиевой основе. J. Источники энергии 282, 299–322.
Google Scholar
Ким, С. Х., Чой, К. Х., Чо, С. Дж., Чой, С., Пак, С., и Ли, С. Ю. (2015). Печатные твердотельные литий-ионные батареи: новый путь к источникам питания соответствующей формы с эстетической универсальностью для гибкой электроники. Nano Lett. 15, 5168–5177. DOI: 10.1021 / acs.nanolett.5b01394
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Клиппштейн, Х., Диас де Серио Санчес, А., Хассанин, Х., Цвейри, Ю., и Сеневиратне, Л. (2018). Моделирование наплавленных отложений для беспилотных летательных аппаратов (БПЛА): обзор. Adv. Англ. Матер. 20: 1700552. DOI: 10.1002 / adem.201700552
CrossRef Полный текст | Google Scholar
Котобуки М., Койси М. и Като Ю.(2013). Приготовление твердого электролита Li1,5Al0,5Ti1,5 (PO4) 3 методом соосаждения. Ionics 19, 1945–1948. DOI: 10.1007 / s11581-013-1000-4
CrossRef Полный текст | Google Scholar
Курцвейл П. (2010). Гастон Планте и его изобретение свинцово-кислотной батареи — генезис первой практической аккумуляторной батареи. J. Источники энергии 195, 4424–4434. DOI: 10.1016 / j.jpowsour.2009.12.126
CrossRef Полный текст | Google Scholar
Лау, Дж., Деблок, Р. Х., Баттс, Д. М., Эшби, Д. С., Чой, С. С., Данн, Б. С. (2018). Сульфидные твердые электролиты для литиевых батарей. Adv. Energy Mater. 8: 1800933. DOI: 10.1002 / aenm.201800933
CrossRef Полный текст | Google Scholar
Ли, Дж. У., Лан, П. X., Ким, Б., Лим, Г., и Чо, Д. У. (2008). Изготовление и анализ характеристик каркаса из полипропиленфумарата с использованием технологии микростереолитографии. J. Biomed. Матер. Res. B Прил.Биоматер. 87, 1–9. DOI: 10.1002 / jbm.b.31057
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, К. В., Ван, С., Фокс, Б. К., Ритман, Э. Л., Яшемски, М. Дж., И Лу, Л. Дж. Б. (2007). Изготовление каркаса для инженерии костной ткани из поли (пропиленфумарата) с использованием стереолитографии: влияние составов смол и параметров лазера. Биомакромолекулы 8, 1077–1084. DOI: 10.1021 / bm060834v
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лейонмарк, С., Корнелл, А., Линдберг, Г., и Вогберг, Л. (2013). Однобумажные гибкие литий-ионные аккумуляторные элементы в процессе изготовления бумаги на основе нанофибриллированной целлюлозы. J. Mater. Chem. А 1, 4671–4677. DOI: 10.1039 / c3ta01532g
CrossRef Полный текст | Google Scholar
Летиен, К., Зегауи, М., Руссель, П., Тильман, П., Роллан, Н., и Роллан, П. А. (2011). Микро-узор из LiPON и литий-фосфата железа, нанесенного на массив кремниевых наностолбиков для литий-ионной твердотельной трехмерной микро-батареи. Microelectron. Англ. 88, 3172–3177. DOI: 10.1016 / j.mee.2011.06.022
CrossRef Полный текст | Google Scholar
Льюис, Дж. А. (2004). Коллоидная обработка керамики. J. Am. Ceram. Soc. 83, 2341–2359.
Google Scholar
Ли, Б., Гу, П., Фэн, Ю., Чжан, Г., Хуанг, К., Сюэ, Х. и др. (2017). Ультратонкие 2D нанолисты из никель-кобальтфосфата для электрохимического накопления энергии под водным / твердотельным электролитом. Adv. Funct.Матер. 27: 1605784. DOI: 10.1002 / adfm.201605784
CrossRef Полный текст | Google Scholar
Li, C., Liu, Y., Li, B., Zhang, F., Cheng, Z., He, P., et al. (2019). Встроенный твердый электролит с пористым катодом путем простого одностадийного спекания для полностью твердотельной батареи Li-O2. Нанотехнологии 30: 364003. DOI: 10.1088 / 1361-6528 / ab226f
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, М., Чен, А.-Н., Лин, X., Ву, Ж.-М., Chen, S., Cheng, L.-J., et al. (2019). Легкая муллитовая керамика с контролируемой пористостью и улучшенными свойствами, изготовленная методом SLS с использованием механически смешанных композитов FAHS / полиамид12. Ceram. Int. 45, 20803–20809. DOI: 10.1016 / j.ceramint.2019.07.067
CrossRef Полный текст | Google Scholar
Ли, С., Чжан, С.К., Шен, Л., Лю, К., Ма, Дж. Б., Львов, В. и др. (2020). Развитие и перспективы керамических / полимерных композитных твердых электролитов для литиевых батарей. Adv. Sci. 7: 18.
Google Scholar
Ли, В., Чен, Л., Сунь, Ю., Ван, К., Ван, Ю., и Ся, Ю. (2017). Полностью твердотельная вторичная литиевая батарея с твердым полимерным электролитом и антрахиноновым катодом. Твердотельный ион. 300, 114–119. DOI: 10.1016 / j.ssi.2016.12.013
CrossRef Полный текст | Google Scholar
Ли, X., Чжан, З., Инь, К., Ян, Л., Тачибана, К., и Хирано, С.-И. (2015). Квазитвердые электролиты из мезопористого кремнезема / ионной жидкости и их применение в литий-металлических батареях. J. Источники энергии 278, 128–132. DOI: 10.1016 / j.jpowsour.2014.12.053
CrossRef Полный текст | Google Scholar
Li, Y., Ding, F., Xu, Z., Sang, L., Ren, L., Ni, W., et al. (2018). Твердотельный литий-ионный аккумулятор, температура окружающей среды, на основе твердого полимерного электролита с высокой концентрацией солей. J. Источники энергии 397, 95–101. DOI: 10.1016 / j.jpowsour.2018.05.050
CrossRef Полный текст | Google Scholar
Лян, С., Янь, В., Ву, X., Чжан, Ю., Zhu, Y., Wang, H., et al. (2018). Гелевые полимерные электролиты для литий-ионных аккумуляторов: изготовление, характеристики и характеристики. Твердотельный ион. 318, 2–18. DOI: 10.1016 / j.ssi.2017.12.023
CrossRef Полный текст | Google Scholar
Lim, H.-D., Lim, H.-K., Xing, X., Lee, B.-S., Liu, H., Coaty, C., et al. (2018). Слои твердого электролита осаждением из раствора. Adv. Матер. Интерфейсы 5: 1701328. DOI: 10.1002 / admi.201701328
CrossRef Полный текст | Google Scholar
Лю В., Ли, С. В., Лин, Д., Ши, Ф., Ван, С., Сендек, А. Д. и др. (2017). Повышение ионной проводимости в композитных полимерных электролитах с помощью хорошо ориентированных керамических нанопроволок. Nat. Энергия 2: 17035.
Google Scholar
Луонго, А., Фальстер, В., Дуст, М. Э. Б., Рибо, М. М., Эйрикссон, Э. Р., Педерсен, Д. Б. и др. (2020). Контроль микроструктуры в 3D-печати с помощью цифровой обработки света. 39, 347–359.
Google Scholar
Ма, Ф., Чжао, Э., Zhu, S., Yan, W., Sun, D., Jin, Y., et al. (2016). Приготовление и оценка твердого электролита Li1.3Al0.3Ti1.7 (PO4) 3 с высокой ионно-литиевой проводимостью, полученного с использованием нового метода растворения. Твердотельный ион. 295, 7–12. DOI: 10.1016 / j.ssi.2016.07.010
CrossRef Полный текст | Google Scholar
Ма, Т., и Девин Маккензи, Дж. (2019). Полностью печатные гибкие воздушно-цинковые батареи с высокой плотностью энергии на основе твердых полимерных электролитов и иерархического каталитического токосъемника. Flex. Распечатать. Электрон. 4: 015010. DOI: 10.1088 / 2058-8585 / ab0b91
CrossRef Полный текст | Google Scholar
Махаджан А., Фрисби К. Д. и Фрэнсис Л. Ф. (2013). Оптимизация аэрозольной струйной печати для получения серебряных линий с высоким разрешением и высоким соотношением сторон. ACS Appl. Матер. Интерфейсы 5, 4856–4864. DOI: 10.1021 / am400606y
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Manapat, J. Z., Chen, Q., Ye, P., and Advincula, R.С. (2017). 3D-печать полимерных нанокомпозитов методом стереолитографии. Macromol. Матер. Англ. 302: 1600553. DOI: 10.1002 / mame.201600553
CrossRef Полный текст | Google Scholar
Manthiram, A., Yu, X., and Wang, S. (2017). Химический состав литиевых батарей обеспечивается твердотельными электролитами. Nat. Rev. Mater. 2: 16103.
Google Scholar
Мао, М., Хе, Дж., Ли, X., Чжан, Б., Лей, К., Лю, Ю. и др. (2017). Новые границы и области применения 3D-печати с высоким разрешением. Микромашины 8: 113. DOI: 10.3390 / mi8040113
CrossRef Полный текст | Google Scholar
Mcowen, D. W., Xu, S., Gong, Y., Wen, Y., Godbey, G. L., Gritton, J. E., et al. (2018). 3D-печать электролитов для твердотельных аккумуляторов. Adv. Матер. 30: 1707132.
Google Scholar
Минами Т., Хаяси А. и Тацумисаго М. (2006). Недавний прогресс стекла и стеклокерамики в качестве твердых электролитов для литиевых вторичных батарей. Твердотельный ион. 177, 2715–2720. DOI: 10.1016 / j.ssi.2006.07.017
CrossRef Полный текст | Google Scholar
Моримото, Х., Ямасита, Х., Тацумисаго, М., и Минами, Т. (1999). Механохимический синтез новых аморфных материалов 60Li2S⋅ 40SiS2 с высокой литиево-ионной проводимостью. J. Am. Ceram. Soc. 82, 1352–1354. DOI: 10.1111 / j.1151-2916.1999.tb01923.x
CrossRef Полный текст | Google Scholar
Нафиси, С., Джалили, Р., Обалеби, С. Х., Горкин И., Р.А., Константинов К., Иннис П. С. и др. (2014). Дисперсии оксида графена: настройка реологии для обеспечения возможности изготовления. Mater. Horiz. 1, 326–331. DOI: 10.1039 / c3mh00144j
CrossRef Полный текст | Google Scholar
Нго, Т. Д., Кашани, А., Имбальзано, Г., Нгуен, К. Т. К. и Хуэй, Д. (2018). Аддитивное производство (3D-печать): обзор материалов, методов, приложений и проблем. Compos. B Eng. 143, 172–196. DOI: 10.1016 / j.compositesb.2018.02.012
CrossRef Полный текст | Google Scholar
Nguyen, H., Banerjee, A., Wang, X., Tan, D., Wu, E.A., Doux, J., et al. (2019). Одностадийный синтез высокопроводящего твердого электролита Na3PS4 для всех натриевых твердотельных батарей. J. Источники энергии 435, 126623–126623. DOI: 10.1016 / j.jpowsour.2019.05.031
CrossRef Полный текст | Google Scholar
Найман, М., Алам, Т. М., Макинтайр, С. К., Блейер, Г. К., и Ингерсолл, Д. (2010). Альтернативный подход к увеличению подвижности Li в электролитах на гранате Li-La-Nb / Ta. Chem. Матер. 22, 5401–5410. DOI: 10,1021 / см 101438x
CrossRef Полный текст | Google Scholar
Обата, К., Эль-Тамер, А., Кох, Л., Хинце, У., Чичков, Б. Н. (2013). Высокоформатное трехмерное структурирование двухфотонной полимеризацией с расширенным рабочим диапазоном объектива (WOW-2PP). Light Sci. Прил. 2: e116. DOI: 10.1038 / lsa.2013.72
CrossRef Полный текст | Google Scholar
Pang, Y., Cao, Y., Chu, Y., Liu, M., Snyder, K., Mackenzie, D., et al.(2019). Аддитивное производство аккумуляторов. Adv. Funct. Матер. 30: 1
4.
Google Scholar
Park, C.-H., Park, M., Yoo, S.-I., and Joo, S.-K. (2006). Твердый полимерный электролит с центрифугированием для твердотельных перезаряжаемых тонкопленочных литий-полимерных батарей. J. Источники энергии 158, 1442–1446. DOI: 10.1016 / j.jpowsour.2005.10.022
CrossRef Полный текст | Google Scholar
Park, I.-B., Ha, Y.-M., Kim, M.-S., Kim, H.-C., and Lee, S.-ЧАС. (2012). Трехмерная шкала серого для улучшения качества поверхности в проекционной микростереолитографии. Внутр. J. Precis. Англ. Производство. 13, 291–298. DOI: 10.1007 / s12541-012-0036-0
CrossRef Полный текст | Google Scholar
Пеше А., Хорнес А., Нуньес М., Мората А., Торрелл М. и Таранкон А. (2020). 3D-печать нового поколения улучшенных твердооксидных топливных и электролизных ячеек. J. Mater. Chem. A. DOI: 10.1039 / d0ta02803g
CrossRef Полный текст | Google Scholar
Pfenninger, R., Струзик, М., Гарбайо, И., Стилп, Э., и Рупп, Дж. Л. М. (2019). Низкая рабочая температура для быстрой литиевой проводимости в гранатовых пленках твердотельных аккумуляторов. Nat. Энергия 4, 475–483. DOI: 10.1038 / s41560-019-0384-4
CrossRef Полный текст | Google Scholar
Фук Н. Х., Тотани М., Морикава К., Муто Х. и Мацуда А. (2016). Приготовление твердого электролита Li3PS4 с использованием этилацетата в качестве синтетической среды. Твердотельный ион. 288, 240–243.DOI: 10.1016 / j.ssi.2015.11.032
CrossRef Полный текст | Google Scholar
Pradel, A., Pagnier, T., and Ribes, M. (1985). Влияние быстрой закалки на электрические свойства литиевых проводящих стекол. Твердотельный ион. 17, 147–154. DOI: 10.1016 / 0167-2738 (85)
-5
CrossRef Полный текст | Google Scholar
Рейес, К., Сомоги, Р., Ниу, С., Круз, М. А., Янг, Ф., Катеначчи, М. Дж. И др. (2018). Трехмерная печать готовой литий-ионной батареи с изготовлением плавленой нити. ACS Appl. Energy Mater. 1, 5268–5279.
Google Scholar
Ruetschi, P., Meli, F., and Desilvestro, J. (1995). Никель-металлогидридные батареи. Предпочитаемые батареи будущего? J. Источники энергии 57, 85–91. DOI: 10.1016 / 0378-7753 (95) 02248-1
CrossRef Полный текст | Google Scholar
Рузметов Д., Олешко В. П., Хейни П. М., Лезец Х. Дж., Карки К., Белудж К. Х. и др. (2012). Стабильность электролита определяет пределы масштабирования для твердотельных литий-ионных аккумуляторов 3D. Nano Lett. 12, 505–511. DOI: 10.1021 / nl204047z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сантоликвидо, О., Коломбо, П., и Ортона, А. (2019). Аддитивное производство керамических компонентов с помощью цифровой обработки света: сравнение подходов «снизу вверх» и «сверху вниз». J. Eur. Ceram. Soc. 39, 2140–2148. DOI: 10.1016 / j.jeurceramsoc.2019.01.044
CrossRef Полный текст | Google Scholar
Скьяво, Л.С.А., Мантас, П.К., Сегадайнш, А.М., и Круз, Р.С.Д. (2018). От сухого прессования до пластического формования керамики: оценка окна технологичности. Констр. Строить. Матер. 189, 594–600. DOI: 10.1016 / j.conbuildmat.2018.09.015
CrossRef Полный текст | Google Scholar
Schnell, J., Günther, T., Knoche, T., Vieider, C., Köhler, L., Just, A., et al. (2018). Полностью твердотельные литий-ионные и литий-металлические батареи — путь к крупносерийному производству. Дж.Источники энергии 382, 160–175. DOI: 10.1016 / j.jpowsour.2018.02.062
CrossRef Полный текст | Google Scholar
Шань Ю., Ли Ю. и Панг Х. (2020). Применение материалов на основе сульфида олова в литий-ионных батареях и натрий-ионных батареях. Adv. Funct. Матер. 30: 2001298. DOI: 10.1002 / adfm.202001298
CrossRef Полный текст | Google Scholar
Смит, А. Дж., Бернс, Дж. К., Трасслер, С., и Дан, Дж. Р. (2010). Прецизионные измерения кулоновской эффективности литий-ионных аккумуляторов и материалов электродов для литий-ионных аккумуляторов. J. Electrochem. Soc. 157: A196.
Google Scholar
Штраус, Ф., Тео, Дж. Х., Шиле, А., Бартч, Т., Хацукаде, Т., Хартманн, П. и др. (2020). Выделение газа в литий-ионных батареях: твердый электролит по сравнению с жидким. ACS Appl. Матер. Интерфейсы 12, 20462–20468.
Google Scholar
Сунь К., Фанг Н., Ву Д. М. и Чжан X. (2005). Проекционная микростереолитография с использованием цифровой микрозеркальной динамической маски. Sens.Приводы A Phys. 121, 113–120. DOI: 10.1016 / j.sna.2004.12.011
CrossRef Полный текст | Google Scholar
Сунь, Дж., Ли, Ю., Чжан, К., Хоу, К., Ши, К., и Ван, Х. (2019). Композитный электролит на основе полиметилметакрилата с высокой ионной проводимостью и нанопроволоками типа граната Li6.75La3Zr1.75Nb0.25O12. Chem. Англ. J. 375: 121922. DOI: 10.1016 / j.cej.2019.121922
CrossRef Полный текст | Google Scholar
Сунь, Ю., Ши, П., Чен, Дж., Ву, К., Liang, X., Rui, X., et al. (2020). Разработка и вызов передовых неводных ионно-натриевых батарей. EnergyChem 2: 100031. DOI: 10.1016 / j.enchem.2020.100031
CrossRef Полный текст | Google Scholar
Суваджи Э., Мессинг Г. Л. (2001). Текстурированная керамика из оксида алюминия методом одноосного прессования. Ключ Eng. Матер. 206-213, 405–408. DOI: 10.4028 / www.scientific.net / kem.206-213.405
CrossRef Полный текст | Google Scholar
Такада, К.(2013). Развитие и перспективы твердотельных литиевых батарей. Acta Mater. 61, 759–770. DOI: 10.1016 / j.actamat.2012.10.034
CrossRef Полный текст | Google Scholar
Таллон, К., Фрэнкс, Г. В. (2011). Последние тенденции в формообразовании в результате коллоидной обработки: обзор. 119, 147–160. DOI: 10.2109 / jcersj2.119.147
CrossRef Полный текст | Google Scholar
Тан, С. Дж., Цзэн, X. X., Ма, К., Ву, X. W., и Го, Ю. Г. (2018). Последние достижения в области композитных электролитов на полимерной основе для литиевых аккумуляторных батарей. Electrochem. Energy Rev. 1, 113–138. DOI: 10.1007 / s41918-018-0011-2
CrossRef Полный текст | Google Scholar
Танака С., Пин К. С. и Уэмацу К. (2006). Влияние расслоения органического связующего на спеченную прочность глинозема сухого прессования. J. Am. Ceram. Soc. 89, 1903–1907. DOI: 10.1111 / j.1551-2916.2006.01057.x
CrossRef Полный текст | Google Scholar
Тацумисаго, М., Хаяси, А. (2012). Суперионные стекла и стеклокерамика в системе Li2S – P2S5 для твердотельных литиевых вторичных батарей. Твердотельный ион. 225, 342–345. DOI: 10.1016 / j.ssi.2012.03.013
CrossRef Полный текст | Google Scholar
Терагава, С., Асо, К., Таданага, К., Хаяси, А., Тацумисаго, М. (2014). Приготовление твердого электролита Li2S – P2S5 из раствора N-метилформамида и применение для твердотельных литиевых аккумуляторов. J. Источники энергии 248, 939–942. DOI: 10.1016 / j.jpowsour.2013.09.117
CrossRef Полный текст | Google Scholar
Треви, Дж., Джанг, Дж. С., Юнг, Ю. С., Штольд, К. Р., и Ли, С. Х. (2009). Стеклокерамические электролиты Li2S – P2S5, полученные с помощью одностадийного процесса шарового биллинга, и их применение для полностью твердотельных литий-ионных аккумуляторов. Electrochem. Commun. 11, 1830–1833. DOI: 10.1016 / j.elecom.2009.07.028
CrossRef Полный текст | Google Scholar
Тамблстон, Дж. Р., Ширванянц, Д., Ермошкин, Н., Янушевич, Р., Джонсон, А. Р., Келли, Д., и др. (2015). Непрерывное создание интерфейса жидкости для 3D-объектов. Science 347, 1349–1352. DOI: 10.1126 / science.aaa2397
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Варшнея, А. К., Мауро, Дж. К. (2019). Основы неорганических стекол . Амстердам: Эльзевир.
Google Scholar
Венкатасубраманян, Н., Уэйд, Б., Десаи, П., Абхираман, А., и Гельбаум, Л. (1991). Синтез и характеристика прядильных золь-гель производных полиборатов. J. Non Cryst. Твердые тела 130, 144–156.DOI: 10.1016 / 0022-3093 (91)
-к
CrossRef Полный текст | Google Scholar
Ван, Дж., Се, Дж., Конг, X., Лю, З., Лю, К., Ши, Ф. и др. (2019). Ультратонкий, гибкий, твердый полимерный композитный электролит с выровненным нанопористым основанием для литиевых батарей. Nat. Nanotechnol. 14, 705–711. DOI: 10.1038 / s41565-019-0465-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, Л., Е, Й., Чен, Н., Хуан, Ю., Ли, Л., Ву, Ф., и другие. (2018). Разработка и проблемы функциональных электролитов для высокопроизводительных литий-серных батарей. Adv. Funct. Матер. 28: 1800919. DOI: 10.1002 / adfm.201800919
CrossRef Полный текст | Google Scholar
Ван, X. Дж., Чжан, Х. П., Кан, Дж. Дж., Ву, Ю. П., и Фанг, С. Б. (2005). Новые композитные полимерные электролиты на основе поли (эфир-уретанового) сетчатого полимера и пирогенного кремнезема. J. Solid State Electrochem. 11, 21–26. DOI: 10.1007 / s10008-005-0029-3
CrossRef Полный текст | Google Scholar
Уорнер, Дж.Т. (2015). Справочник по проектированию литий-ионных аккумуляторных батарей: химия, компоненты, типы и терминология . Амстердам: Эльзевир.
Google Scholar
Wootthikanokkhan, J., Phiriyawirut, M., and Pongchumpon, O.J. (2015). Влияние параметров электропрядения и содержания нанонаполнителя на морфологию и свойства гелевого электролита композитных нановолокон на основе PVDF-HFP, наполненного La2O3. Внутр. J. Polym. Матер. Polym. Биоматер. 64, 416–426. DOI: 10.1080 / 00
7.2014.958830CrossRef Полный текст | Google Scholar
Се Дж., Иманиши Н., Чжан Т., Хирано А., Такеда Ю. и Ямамото О. (2009). Литий-ионный транспорт в твердотельных литиевых батареях с LiCoO2 с использованием стеклокерамических электролитов типа NASICON. J. Источники энергии 189, 365–370. DOI: 10.1016 / j.jpowsour.2008.08.015
CrossRef Полный текст | Google Scholar
Xing, B., Yao, Y., Meng, X., Zhao, W., Shen, M., Gao, S., et al. (2020). Самоподдерживающийся оксид циркония, стабилизированный оксидом иттрия, волнообразный электролит для применения в твердооксидных топливных элементах с помощью трехмерной печати с цифровой обработкой света. Scr. Матер. 181, 62–65. DOI: 10.1016 / j.scriptamat.2020.02.004
CrossRef Полный текст | Google Scholar
Янг, Ю., Чен, З., Сун, X., Чжу, Б., Сяй, Т., Ву, П.-И., и др. (2016). Трехмерная печать высокодиэлектрического конденсатора методом проекционной стереолитографии. Nano Energy 22, 414–421. DOI: 10.1016 / j.nanoen.2016.02.045
CrossRef Полный текст | Google Scholar
Янг Ю., Юань В., Чжан Х., Юань Ю., Wang, C., Ye, Y., et al. (2020). Обзор приложений трехмерной печати для литий-ионных аккумуляторов. Прил. Энергия 257: 14002.
Google Scholar
Инь, Ю. К., Ван, К., Ян, Дж. Т., Ли, Ф., Чжан, Г., Цзян, К. Х. и др. (2020). Межфазный слой на основе тонкой пленки хлорида металла на основе перовскита для защиты металлического лития от жидкого электролита. Nat. Commun. 11: 1761.
Google Scholar
Йошио, М., Бродд, Р. Дж., И Козава, А. (2009). Литий-ионные батареи . Нью-Йорк, штат Нью-Йорк: Спрингер.
Google Scholar
Юань, М., и Лю, К. (2020). Рациональная конструкция сепараторов и жидких электролитов для более безопасных литий-ионных батарей. J. Energy Chem. 43, 58–70. DOI: 10.1016 / j.jechem.2019.08.008
CrossRef Полный текст | Google Scholar
Yue, L., Ma, J., Zhang, J., Zhao, J., Dong, S., Liu, Z., et al. (2016). Все твердотельные полимерные электролиты для высокопроизводительных литий-ионных аккумуляторов. Energy Storage Mater. 5, 139–164.
Google Scholar
Зеколл, С., Марринер-Эдвардс, К., Хексельман, А. К. О., Касемчайнан, Дж., Кусс, К., Армстронг, Д. Е. Дж. И др. (2018). Гибридные электролиты с трехмерными бинепрерывными упорядоченными керамическими и полимерными микроканалами для полностью твердотельных батарей. Energy Environ. Sci. 11, 185–201. DOI: 10.1039 / c7ee02723k
CrossRef Полный текст | Google Scholar
Zhang, H., Li, C., Piszcz, M., Coya, E., Рохо, Т., Родригес-Мартинес, Л. М. и др. (2017). Одиночные литий-ионные проводящие твердые полимерные электролиты: достижения и перспективы. Chem. Soc. Ред. 46, 797–815.
Google Scholar
Чжан, К., Цао, Д., Ма, Ю., Натан, А., Аврора, П., и Чжу, Х. (2019). Твердотельные электролиты на основе сульфидов: синтез, стабильность и потенциал для полностью твердотельных аккумуляторов. Adv. Матер. 31: e1
1.Google Scholar
Чжан, С.С.(2007). Обзор сепараторов литий-ионных аккумуляторов с жидким электролитом. J. Источники энергии 164, 351–364. DOI: 10.1016 / j.jpowsour.2006.10.065
CrossRef Полный текст | Google Scholar
Zhang, X., Liu, T., Zhang, S., Huang, X., Xu, B., Lin, Y., et al. (2017). Синергетическое взаимодействие между Li6.75La3Zr1.75Ta0.25O12 и поливинилиденфторидом обеспечивает высокую ионную проводимость, механическую прочность и термическую стабильность твердых композитных электролитов. J. Am.Chem. Soc. 139, 13779–13785. DOI: 10.1021 / jacs.7b06364
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чжоу, К., Чжан, Дж., И Цуй, Г. (2018). Полимерные электролиты с жесткой и гибкой связью с литиевыми батареями высокой энергии. Macromol. Матер. Англ. 303: 1800337. DOI: 10.1002 / mame.201800337
CrossRef Полный текст | Google Scholar
границ | Последние достижения в области электролитов для цинково-воздушных батарей
Введение
Zn – воздушный аккумулятор имеет высокую удельную энергию (1,218 Вт · ч · кг −1 ).Между тем, присущие ему характеристики, в том числе безопасность и низкая стоимость, делают его одним из самых многообещающих аккумуляторов следующего поколения (Fu et al., 2017; Tan et al., 2017; Han et al., 2019). Роль электролитов упускается из виду по сравнению с горячими исследованиями бифункциональных воздушных электродов для Zn-воздушных батарей. Характеристики электролитов напрямую определяют ионную проводимость и межфазные свойства Zn-воздушной батареи в процессе эксплуатации. Кроме того, это дополнительно влияет на емкость, стабильность при циклической работе, а также эффективность зарядки и разрядки элемента (Pei et al., 2014). Zn-воздушные батареи развиваются в направлении высокой эффективности и долговечности, которые невозможно отделить от поддержки электролита с превосходными характеристиками во всех аспектах (R. Mainar et al., 2016). Таким образом, очень важно изучить работу электролитов в Zn-воздушных батареях (Mainar et al., 2018).
В настоящее время щелочной электролит все еще широко используется в батареях на основе цинка для удовлетворения требований низкой стоимости и высокой ионной проводимости и обеспечения стабильности цинкового электрода (R.Mainar et al., 2016; Сюй и др., 2020). Однако он чувствителен к воздействию CO 2 окружающей среды и относительной влажности. Zn-воздушная батарея в основном зависит от характеристик воздушного электрода. К сожалению, CO 2 может привести к образованию в электролите K 2 CO 3 , что отрицательно влияет на пустоту в воздушном электроде (Wang et al., 2014; Fu et al., 2017). Zn – воздушные батареи должны решать проблему испарения электролита или поглощения воды из внешней среды, чтобы хорошо работать в сложной внешней среде.Первый заставляет батарею расширяться, а второй влияет на перенос OH — (Chakkaravarthy et al., 1981; Mainar et al., 2018). Ионные жидкости комнатной температуры (RTIL) и твердые электролиты являются альтернативными и эффективными решениями для решения вышеуказанной проблемы. Однако их производительность была ограничена их низкой ионной проводимостью и неквалифицированным интерфейсом. Поэтому в следующих частях мы обсудим статус исследования щелочных электролитов и неводных электролитов в Zn-воздушных батареях.
Водный электролит
LiOH, NaOH и KOH — обычные электролиты для Zn-воздушных аккумуляторов. По сравнению с нейтральными и кислотными электролитами щелочные электролиты хорошо сочетаются с цинковыми электродами и материалами катализатора. Между тем, электролит КОН обладает высокой ионной проводимостью и низкой вязкостью. Когда Zn-воздушная батарея разряжается, внешний кислород входит в батарею и реагирует (Уравнение 1) (реакция восстановления кислорода) на границе раздела газ-жидкость-твердое тело (кислород, электролит, электрокатализатор).Цинковый электрод переносит электроны к воздушному электроду через внешнюю нагрузку, а OH — в месте реакции генерирует Zn (OH) 42- (уравнение 2). Когда концентрация Zn (OH) 42- достигает максимума, он далее разлагается на ZnO (уравнение 3). Полная реакция цинкового электрода показана в уравнении 4. Во время процесса зарядки происходит обратная реакция (уравнение 1) (реакция выделения кислорода) на границе раздела цинк-электролит, и электрическая энергия накапливается, в то время как цинк осаждается в результате обратной реакции. (Уравнение 3).
O2 + 2h3O + 4e-↔4OH-E = 0,40 В по сравнению с SHE (1) Zn + 4OH-↔Zn (OH) 42- + 2e-E = 1,26 В по сравнению с SHE (2) Zn (OH) 42-↔ZnO + h3O + 2OH- (3) Zn + 2OH-↔ZnO + h3O + 2e-E = 1,26 В по сравнению с SHE (4)Когда концентрация КОН составляет 6 М, плотность обмена током Zn / Zn 2+ достигает 0,21 А · см −2 , а растворимость ZnO увеличивается с увеличением концентрации КОН (See and White, 1997; Dyer и др., 2009). Следовательно, мы должны обратить внимание на неблагоприятное влияние электролита КОН с высокой концентрацией на цинковый электрод.Высокая концентрация ZnO производит избыток Zn (OH) 42- и осаждается после разряда, что увеличивает пассивирующее сопротивление цинкового электрода. Кроме того, кинетические параметры восстановления кислорода цинка были очень высокими, что приводило к растворению, миграции и переотложению цинка в различных условиях (R. Mainar et al., 2016).
Есть две основные стратегии решения этой проблемы. Один заключается в изменении состава и структуры цинкового электрода, а другой — в поиске подходящих добавок к электролиту.Известные методы, такие как создание трехмерной структуры цинкового электрода (Parker et al., 2014; Chamoun et al., 2015; Yan et al., 2015) или эффективная добавка для цинкового электрода (Fan et al., 2013; Masri and Mohamad, 2013; Huang et al., 2015) оказались эффективной стратегией решения. Актуальной задачей является точное измерение потенциала и концентрации ионов цинка на поверхности цинкового электрода, чтобы обеспечить адекватную теоретическую поддержку для улучшения условий жизни цинкового электрода в щелочном электролите.В таблице 1 мы суммировали последние работы по добавкам щелочных электролитов. Подходящие добавки в электролиты могут улучшить изменение формы цинкового электрода и производительность Zn-воздушной батареи. Если мы сможем снизить концентрацию КОН, насколько это возможно, не влияя на ионную проводимость электролита, мы полагаем, что производительность Zn-воздушной батареи будет еще больше улучшена. Добавляя K 2 CO 3 к высококонцентрированному раствору KOH и оптимизируя структуру батареи, Schröder et al.(2015) не только получили стабильный электрический потенциал, но также улучшили фактическую плотность энергии и долгосрочную стабильность Zn-воздушной батареи. Кроме того, ингибирование роста дендритов и выделения водорода из цинкового электрода также зарегистрировано в Zn-воздушной батарее с щелочными электролитами, использующими додецилбензолсульфонат натрия (SDBS) (Yang et al., 2004), полиэтиленгликоль (PEG) (Banik and Akolkar). , 2013), винной / янтарной / лимонной кислотами (Lee et al., 2006) и гидроксидами тетраалкиламмония (Lan et al., 2007).
Таблица 1 . Краткое изложение недавно опубликованной добавки к щелочному электролиту для Zn-воздушных батарей.
Zn – air аккумулятор представляет собой полуоткрытую систему, которой для участия в процессе реакции требуется богатый кислород из внешней среды. Углекислый газ (CO 2 ) трудно избежать во влажной атмосфере. CO 2 из внешней атмосферы попадает в батарею через воздушный электрод и вступает в реакцию с OH — в электролите (уравнения 5, 6).
СО2 + ОН- → HCO3- (5) HCO3− + OH − ↔CO32− + h3O (6)Ионная проводимость электролита ослабляется из-за образования HCO3- и CO32- и низкой растворимости K 2 CO 3 и KHCO 3 . Когда они осаждаются на воздушном электроде, перенос кислорода будет до некоторой степени заблокирован, что приведет к снижению производительности Zn-воздушной батареи. Оптимизация структуры Zn-воздушной батареи и состава слоя адсорбции газа, чтобы позволить кислороду проходить беспрепятственно, но препятствовать прохождению диоксида углерода и водяного пара, является идеальным решением.Для решения вышеуказанных проблем исследователи также предложили несколько решений. Pedicini et al. (1996) создали систему управления воздухом для рециркуляции реагирующего воздуха в металл-воздушной батарее. Goldstein et al. (1997) предложили скрубберную систему для удаления диоксида углерода из металл-воздушной батареи или батареи топливных элементов. Педикни (2002) предложил ограничивать выбросы углекислого газа и водяного пара, когда батарея не используется, путем загрузки воздушной заслонки для электрохимического элемента. Есть много решений для решения этих проблем, но ограничениями являются пороговые значения высокой стоимости и ограниченное использование пространства, что ограничивает развитие Zn-воздушных батарей в практических приложениях.
Система проточного электролита — очень эффективный метод для Zn-воздушных батарей. Электролит перекачивается и циркулирует через систему питания внешних труб и насосов. В дополнение к удалению осажденного карбоната и других побочных продуктов через внешние фильтры проточный электролит улучшает перенос OH — и снижает градиенты концентрации (Iacovangelo and Will, 1985; Cheng et al., 2007). По сравнению со статическим электролитом, Zn-воздушная батарея значительно улучшена, включая срок службы и рабочее напряжение с системой циркуляции электролита.Однако мощность циркуляции электролита должна поддерживаться внешней системой откачки и электрической энергией. Следовательно, если система циркуляции электролита применяется на практике, необходимо решить проблему, которую трудно применить к крупномасштабной сетевой системе хранения энергии со строгими требованиями к пространству и весу.
Ионная жидкость комнатной температуры
Ионная жидкость комнатной температуры представляет собой расплавленную соль, которая существует в виде жидкости при комнатной температуре или ниже.Он имеет широкое электрохимическое окно и нелегко воспламеняется (Balaish et al., 2014). Поэтому все больше внимания уделяется RTIL как заменителю щелочных электролитов. Присущая RTIL безопасность и стабильность в широком диапазоне электрохимических потенциалов привели к его применению в литиевых батареях (Chou et al., 2008; Xiang et al., 2010). Использование RTIL в Zn-воздушных батареях может эффективно решить проблемы повреждения цинкового электрода (Simons et al., 2012), повреждения CO 2 и испарения электролита (Harting et al., 2012) в щелочном электролите водяной системы, упомянутой выше, и позволяют батарее работать при высоких температурах. Более того, для апротонных RTIL отсутствие протонов может эффективно избежать коррозии цинкового электрода, вызванной выделением водорода. Поэтому RTIL как электролит для Zn-воздушных аккумуляторов в последние годы попали в список.
RTIL, используемый в качестве электролита для Zn-воздушной ячейки, цинк окисляется до Zn 2+ во время разряда, и обратимая электрохимическая реакция цинка в RTIL оказалась возможной (Xu et al., 2015). Здесь необходимо отметить, что неподходящие RTIL могут образовывать нерастворимые вещества с Zn 2+ и делать их неспособными эффективно восстанавливаться. Предложен механизм воздушного электрода в электролите RTIL (Kar et al., 2014).
Когда в электролите RTIL происходит восстановление кислорода, кислород приобретает электроны и образует супероксид (O2 · -) (уравнение 7). Эта реакция считается квазиобратимой (AlNashef et al., 2002). Для апротонных RTIL отсутствует дальнейший перенос электронов из-за присутствия супероксида.Напротив, для протонных RTIL супероксид является сильным нуклеофилом, который может далее реагировать с протонами в RTIL с образованием пер-гидроксирадикала (HO2 ·) (уравнение 8). Затем пер-гидрокси-радикал может также реагировать с супероксидом с образованием пероксида (HO2-) (уравнения 9, 10) и, наконец, завершить процесс восстановления (уравнение 11).
O2 + e− → O2⋅− (7) O2⋅− + H + → HO2⋅ (8) HO2⋅ + O2⋅− → HO2− + O2 (9) HO2⋅ + e− → HO2− (10) HO2− + H + → h3O2 (11)Что касается того, может ли перекись водорода далее разлагаться на H 2 O, Зеллер (2011) указывает, что это определяется используемым электродом.Согласно Kar et al. (2014) краткое изложение реакций восстановления кислорода и осаждения кислорода в RTIL, в реакции, как упоминалось выше, пути оказались обратимыми и относительно стабильными продуктами пероксида. Однако все еще есть некоторые связанные реакции диспропорционирования. Перекись водорода требует меньше энергии активации для производства кислорода, что делает ее эффективной поддержкой для восстановления кислорода и реакций выделения кислорода в RTIL.
Разработка RTIL в Zn-воздушной батарее все еще сталкивается с огромными проблемами.С одной стороны, высокая стоимость RTIL затрудняет использование в больших масштабах. С другой стороны, двухэлектронный реакционный механизм RTIL снижает удельную энергию батареи в сочетании с ее высокой вязкостью и низкой проводимостью, что означает, что Zn-воздушная батарея может работать только при низком токе. Используя Li 0,87 Na 0,63 K 0,50 CO 3 и NaOH в качестве электролита, Liu et al. (2017) исследовали Zn-воздушную батарею, способную заряжаться и разряжаться при 550 ° C в течение 100 циклов с кулоновской эффективностью 96.9%. Когда Ingale et al. (2017) применили ионную жидкость трифторметансульфонат диэтилметиламмония (DEATfO) к Zn-воздушной батарее, они обнаружили, что, хотя образования дендритов цинка не было, слабое поверхностное натяжение DEATfO привело к неудовлетворительной плотности энергии (Pozo-Gonzalo et al., 2014). Кроме того, Ghazvini et al. (2018) указали на положительное влияние добавления воды на ионное взаимодействие при использовании электролита RTIL в Zn-воздушных батареях. Вышеупомянутая работа представляет собой хорошую стратегию для улучшения характеристик Zn-воздушной батареи с RTIL в качестве электролита.
Кроме того, следует изучить применение большего количества типов RTIL в Zn-воздушных батареях, включая положительное влияние добавок в RTIL. Также необходимо разработать специальные бифункциональные катализаторы для снижения энергетического барьера реакции восстановления кислорода и реакции выделения кислорода. Хотя электролит RTIL требует дальнейшего изучения с точки зрения свойств интерфейса, механизма электрохимической реакции кислорода и пути миграции активных веществ, различные свидетельства указывают на то, что RTIL являются многообещающими электролитами для Zn-воздушных батарей.
Квазитвердый гибкий электролит
В связи с растущим спросом на гибкие носимые электронные устройства, исследования гибких батарей, особенно квазитвердых электролитов, выдвинули более высокие требования. По сравнению с другими металл-воздушными батареями, Zn-воздушные батареи с высокой объемной плотностью энергии обладают характеристиками низкой стоимости и высокой безопасности. Напротив, цинк в качестве электрода имеет более энергетические механические свойства и производительность в гибких батареях. Например, батареи Zn-MnO 2 , в которых используются полимерные электролиты, были коммерчески произведены с использованием технологии печати (MacKenzie and Ho, 2015).Следовательно, необходимо проводить научные исследования структуры и характеристик гибкой Zn-воздушной батареи, а производство этого типа батареи и соответствующего квазитвердого электролита необходимо постоянно оптимизировать.
Квазитвердый гибкий электролит обычно получают из щелочного водного раствора и полимеров, таких как поливиниловый спирт (ПВС) (Fan et al., 2019), полиакриловая кислота (PAA) (Wu et al., 2006; Zhu et al., 2018), желатин (Park et al., 2015) и родственный им привитой сополимер (Yu et al., 2017), которые необходимы для обеспечения стабильной конфигурации, разделения катода и анода и квалифицированной ионной проводимости. В процессе приготовления большинство квазитвердых гибких электролитов могут образовывать сшитую сеть с большим количеством гидрофильных функциональных групп (таких как гидроксильные группы), что обеспечивает более высокое удержание воды и ионную проводимость в квазитвердых гибких электролитах. В первичной Zn-воздушной ячейке щелочной гелевый электролит может эффективно уменьшить утечку и улетучивание электролита, и был применен (Hilder et al., 2009). Однако для перезаряжаемых гибких Zn-воздушных батарей из-за цинкового электрода в квазитвердом гибком электролите они могут нести лишь небольшое количество Zn (OH) 42-. Блокируется процесс восстановления ZnO до Zn (OH) 42- (Xu et al., 2015). Поэтому создание перезаряжаемых Zn-воздушных батарей для работы с большим током является большой проблемой.
Гибкая удельная мощность и циклическая производительность Zn-воздушной батареи были высоко оценены. Однако есть несколько важных аспектов бифункционального катализатора для электрохимических кислородных реакций, ионной проводимости квазитвердого гибкого электролита и характеристик границы раздела электролит-электрод.Ионная проводимость электролита зависит в основном от типа полимера и добавок к электролиту. Fan et al. (2019) приготовили пористый электролит ПВС + SiO 2 с высокой ионной проводимостью 57,3 мСм см −1 , отличными характеристиками циклирования и удельной мощностью. Ли и др. (2019) изготовили полимерный диэлектрик TEAOH-PVA, который по прошествии 2 недель все еще имел ионную проводимость 30 мСм см -1 , демонстрируя отличный срок службы и срок службы. Нетрудно обнаружить, что отдельный полимер вряд ли может стать гибким электролитом квазитвердого состояния с превосходными характеристиками.Однако небольшое количество добавок может значительно улучшить характеристики электролитов, что также является процессом функционализации полимера. Это происходит главным образом потому, что добавка оптимизирует структуру сшитой сетки полимерного электролита, увеличивает количество гидрофильных функциональных групп (таких как гидроксильные группы) и дополнительно улучшает способность электролита удерживать воду, что имеет большое влияние на ионную проводимость. Более того, помимо ионной проводимости и характеристик удержания воды квазитвердого гибкого электролита, следует уделять больше внимания скорости переноса OH — и Zn (OH) 42-, которой уделялось недостаточное внимание в настоящее время.Процесс их переноса также оказывает сильное влияние на плотность энергии и другие характеристики гибких Zn-воздушных батарей.
Перед гибкой Zn-воздушной батареей стоит задача улучшить характеристики границы раздела электролит – электрод (особенно границы электролит – воздух). Смачиваемость квазитвердого гибкого электролита была снижена, что значительно затрудняет выполнение катализатором своей функции, чем в щелочном электролите водной системы.При сборке аккумулятора Xu et al. (2019) прессовали батарею в течение 3 минут при давлении 3 МПа с помощью таблеточного пресса, чтобы сделать ламинированную структуру более полной, а гибкая Zn-воздушная батарея могла стабилизировать циркуляцию в течение 35 часов. По-прежнему необходимы дополнительные исследования для улучшения границы раздела электролит-электрод, приготовления электролита и метода упаковки батареи.
Гибкая Zn-воздушная батарея также выдвигает более высокие требования к характеристикам изгиба, растяжения и сжатия цинкового электрода, воздушного электрода и электролита в батарее.Гибкая Zn-воздушная батарея обычно подразделяется на 1D-структуру (линейный тип) и 2D-структуру (в форме сэндвича). Ma et al. (2019) подготовили гидрогелевый электролит с двойной сеткой (полиакрилатный гидрогель, сшитый цепями целлюлозы и N, N-метилен-бисакриламидными якорями) и оптимизировали структуру цинкового и воздушного электродов для сборки Zn-воздушной батареи с превосходными характеристиками растяжения. Pan et al. (2019) сконструировали губчатую сжимаемую Zn-воздушную батарею, которая хорошо себя показала после 60% деформации сжатия или 500 циклов повторных испытаний на сжатие.Ли и др. (2018) подготовили одномерную вязанную Zn-воздушную батарею с диаметром всего 1,03 мм по пути, которая имела отличные характеристики гибкости, заряда и разряда.
В Таблице 2 перечислены более сравниваемые характеристики, чтобы предоставить более значимые пути разработки квазитвердых гибких электролитов для Zn-воздушных батарей. Однако получить компетентную оценку сложно из-за различной конструкции батареи, катализатора и электролита, используемых в записанных работах. Следовательно, необходимо установить единый стандарт оценки для гибкой Zn-воздушной батареи, чтобы лучше оценивать характеристики соответствующего электролита.Кроме того, состав электролита в гибкой Zn-воздушной батарее в основном находится в режиме «полимер + раствор КОН», что приводит к преимуществам и недостаткам упомянутого выше водного электролита, действующего на квазитвердый электролит. В то же время комбинация RTIL с полимером может придать новый импульс безопасности и стабильности Zn-воздушных батарей, но ее практическая осуществимость должна быть проверена в ближайшем будущем.
Таблица 2 .Краткое изложение недавно опубликованной квазитвердой добавки к гибкому электролиту для Zn-воздушных батарей.
Сводка
Учитывая потребность в высокомощных, долговечных и гибких перезаряжаемых Zn-воздушных батареях, разработка электролитов отвечает возможностям и задачам. Электролит, как критическая часть Zn-воздушной батареи, оказывает сильное влияние на эффективность циркуляции, удельную мощность и характеристики емкости. До сих пор щелочные электролиты являются основным направлением из-за их превосходной ионной проводимости и межфазных свойств.Однако щелочные электролиты чувствительны к воздействию содержания углекислого газа и относительной влажности во внешней среде. С одной стороны, следует изучить подходящий тип и пропорцию добавок для улучшения свойств щелочного электролита. С другой стороны, RTIL, как электролит для Zn-воздушных батарей, имеют высокий порог старения, и его защита и безопасность для цинковых электродов очевидны. Более того, исследования квазитвердого гибкого электролита в большей степени способствуют созданию портативных и гибких Zn-воздушных батарей, которые обеспечивают устранение недостатков в характеристиках интерфейса и ионной проводимости.Подбор подходящих RTIL и полимеров имеет смысл улучшить характеристики электролита.
Кроме того, мы думаем, что три упомянутых выше электролита могут иметь разные характеристики. Подходящие добавки к электролиту могут также способствовать применению RTIL и квазитвердых электролитов в Zn-воздушных батареях, а комбинация RTIL и полимеров также может улучшить характеристики электролитов. Исследованиям электролитов следует уделять больше внимания, чтобы Zn-воздушные батареи удовлетворяли потребности в накопителях энергии нового поколения.
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее для публикации.
Финансирование
Работа выполнена при финансовой поддержке Китайского фонда естественных наук (U1832136, 21303038), Национальной программы обучения студентов инновациям и предпринимательству (201
9010) и Фонда естественных наук провинции Аньхой (1808085QE140).Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
АльНашеф И. М., Леонард М. Л., Мэтьюз М. А. и Вайднер Дж. У. (2002). Электрохимия супероксида в ионной жидкости. Ind. Eng. Chem. Res. 41, 4475–4478. DOI: 10.1021 / ie010787h
CrossRef Полный текст | Google Scholar
Баник, С. Дж., Аколкар, Р. (2013). Подавление роста дендритов при электроосаждении цинка добавкой ПЭГ-200. J. Electrochem. Soc. 160, D519 – D523. DOI: 10.1149 / 2.040311jes
CrossRef Полный текст | Google Scholar
Чаккараварти, К., Вахид А.А. и Удупа Х. (1981). Цинково-воздушные щелочные батареи — обзор. J. Источники энергии 6, 203–228. DOI: 10.1016 / 0378-7753 (81) 80027-4
CrossRef Полный текст | Google Scholar
Чамун М., Герцберг Б. Дж., Гупта Т., Дэвис Д., Бхадра С., Ван Тасселл Б. и др. (2015). Гипердендритные нанопористые аноды из цинковой пены. NPG Asia Mater. 7: e178. DOI: 10.1038 / am.2015.32
CrossRef Полный текст | Google Scholar
Чен, X., Лю, Б., Чжун, К., Лю, З., Лю, Дж., Ма, Л. и др. (2017). Ультратонкий Co 3 O 4 слоя с большой площадью контакта на углеродных волокнах в качестве высокоэффективного электрода для гибкой воздушно-цинковой батареи, интегрированной с гибким дисплеем. Adv. Energy Mater. 7: 1700779. DOI: 10.1002 / aenm.201700779
CrossRef Полный текст | Google Scholar
Cheng, J., Zhang, L., Yang, Y.-S., Wen, Y.-H., Cao, G.-P., and Wang, X.-D. (2007). Предварительные исследования однопоточной цинк-никелевой батареи. Electrochem. Commun. 9, 2639–2642. DOI: 10.1016 / j.elecom.2007.08.016
CrossRef Полный текст | Google Scholar
Chou, S.-L., Wang, J.-Z., Sun, J.-Z., Wexler, D., Forsyth, M., Liu, H.-K., et al. (2008). Высокая емкость, безопасность и улучшенная циклируемость литий-металлической батареи с использованием катода из наноматериала V 2 O 5 и ионно-жидкого электролита при комнатной температуре. Chem. Матер. 20, 7044–7051. DOI: 10,1021 / см801468q
CrossRef Полный текст | Google Scholar
Дайер, К.К., Мозли П. Т., Огуми З., Рэнд Д. А. и Скросати Б. (2009). Энциклопедия электрохимических источников энергии. (Newnes: Elsevier Science & Technology).
Google Scholar
Фан, X., Лю, Дж., Сун, З., Хан, X., Дэн, Ю., Чжун, К., и др. (2019). Пористый нанокомпозитный гелевый полимерный электролит с высокой ионной проводимостью и превосходной способностью удерживать электролит для гибких воздушно-цинковых батарей с длительным сроком службы. Nano Energy 56, 454–462.DOI: 10.1016 / j.nanoen.2018.11.057
CrossRef Полный текст | Google Scholar
Фань, X., Ян, Z., Xie, X., Long, W., Wang, R., and Hou, Z. (2013). Электрохимическое поведение Zn – Al – La-гидроталькита во вторичных ячейках Zn-Ni. J. Источники энергии 241, 404–409. DOI: 10.1016 / j.jpowsour.2013.04.136
CrossRef Полный текст | Google Scholar
Фу, Дж., Кано, З. П., Парк, М. Г., Ю, А., Фаулер, М., и Чен, З. (2017). Электрически перезаряжаемые воздушно-цинковые батареи: прогресс, проблемы и перспективы. Adv. Матер. 29: 1604685. DOI: 10.1002 / adma.201604685
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Fu, J., Lee, D. U., Hassan, F. M., Yang, L., Bai, Z., Park, M. G., et al. (2015). Гибкие высокоэнергетические перезаряжаемые воздушно-цинковые батареи на полимерно-электролитной основе. Adv. Матер. 27, 5617–5622. DOI: 10.1002 / adma.201502853
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Газвини, М.С., Пуллетикурти, Г., Цуй, Т., Кул, К., и Эндрес, Ф. (2018). Электроосаждение цинка из смесей ацетата 1-этил-3-метилимидазолия и воды: исследования применимости электролита для Zn-воздушных батарей. J. Electrochem. Soc. 165: D354. DOI: 10.1149 / 2.0181809jes
CrossRef Полный текст | Google Scholar
Гольдштейн, Дж. Р., Харац, Ю., Шарон, Ю., и Наймер, Н. (1997). Система скруббера для удаления углекислого газа из металлической батареи или батареи топливных элементов. Патент США №5,595,949. (Вашингтон, округ Колумбия: патентная заявка Управления США по патентам и товарным знакам).
Google Scholar
Гуань К., Сумбоджа А., Занг В., Цянь Ю., Чжан Х., Лю X. и др. (2019). Декорирование наночастиц Co / CoNx в углеродных наночастицах, легированных азотом, для гибких и перезаряжаемых воздушно-цинковых батарей. Energy Storage Mater. 16, 243–250. DOI: 10.1016 / j.ensm.2018.06.001
CrossRef Полный текст | Google Scholar
Хан, Дж., Мэн, X., Лу, Л., Биан, Дж., Ли, З., и Сан, К. (2019). Одноатомный Fe-Nx-C как эффективный электрокатализатор для цинково-воздушных аккумуляторов. Adv. Funct. Матер. 29: 1808872. DOI: 10.1002 / adfm.201808872
CrossRef Полный текст | Google Scholar
Хартинг, К., Кунц, У., Турек, Т. (2012). Цинково-воздушные батареи: перспективы и проблемы для дальнейшего совершенствования. Z. Phys. Chem. 226, 151–166. DOI: 10.1524 / zpch.2012.0152
CrossRef Полный текст | Google Scholar
Гильдер, М., Винтер-Йенсен, Б., и Кларк, Н. (2009). Цинково-воздушная батарея с печатью на бумажной основе. J. Источники энергии 194, 1135–1141. DOI: 10.1016 / j.jpowsour.2009.06.054
CrossRef Полный текст | Google Scholar
Хоссейни С., Аббаси А., Уджинет Л.-О., Хаустраэте Н., Прасертдам С., Йонезава Т. и др. (2019). Влияние диметилсульфоксида как добавки к электролиту на анодное растворение щелочной цинково-воздушной проточной батареи. Sci. Rep. 9: 14958. DOI: 10.1038 / s41598-019-51412-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хоссейни, С., Хан, С. Дж., Арпонвичаноп, А., Йонедзава, Т., и Кхеахом, С. (2018). Этанол в качестве добавки к электролиту для щелочных воздушно-цинковых батарей. Sci. Rep. 8: 11273. DOI: 10.1038 / s41598-018-29630-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хуанг, Дж., Ян, З., Ван, Р., Чжан, З., Фэн, З., и Се, X. (2015). Слоистые двойные оксиды Zn-Al в качестве высокоэффективных анодных материалов для вторичных батарей на основе цинка. J. Mater. Chem. А 3, 7429–7436.DOI: 10.1039 / C5TA00279F
CrossRef Полный текст | Google Scholar
Якованджело, К. Д., Уилл, Ф. Г. (1985). Параметрическое исследование осаждения цинка на пористом углероде в ячейке с проточным электролитом. J. Electrochem. Soc. 132: 851.
Google Scholar
Ингейл П., Сакхивел М. и Дриллет Дж. Ф. (2017). Испытание ионной жидкости трифторметансульфоната диэтилметиламмония в качестве электролита в электрически перезаряжаемой Zn / воздушной батарее. Дж.Электрохим. Soc. 164, H5224 – H5229. DOI: 10.1149 / 2.0351708jes
CrossRef Полный текст | Google Scholar
Кар, М., Саймонс, Т. Дж., Форсайт, М., и Макфарлейн, Д. Р. (2014). Ионные жидкие электролиты как платформа для перезаряжаемых металл-воздушных батарей: перспектива. Phys. Chem. Chem. Phys. 16, 18658–18674. DOI: 10.1039 / C4CP02533D
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кумар, К. К., Бринда, Р., Нандхини, М., Селвам, М., Саминатан, К., и Шактипанди, К. (2019). Взвешенный в воде графен в качестве добавки к электролиту в системе цинково-воздушных щелочных батарей. Ionics 25, 1699–1706. DOI: 10.1007 / s11581-019-02924-7
CrossRef Полный текст | Google Scholar
Лан, К., Ли, К., и Чин, Т. (2007). Гидроксиды тетраалкиламмония как ингибиторы дендрита цинка во вторичных батареях на основе цинка. Электрохим. Acta 52, 5407–5416. DOI: 10.1016 / j.electacta.2007.02.063
CrossRef Полный текст | Google Scholar
Ли, К.W., Sathiyanarayanan, K., Eom, S. W., Kim, H. S., and Yun, M. S. (2006). Новое электрохимическое поведение цинковых анодов в цинково-воздушных батареях в присутствии добавок. J. Источники энергии 159, 1474–1477. DOI: 10.1016 / j.jpowsour.2005.11.074
CrossRef Полный текст | Google Scholar
Li, M., Liu, B., Fan, X., Liu, X., Liu, J., Ding, J., et al. (2019). Полимерный электролит длительного хранения на основе гидроксида тетраэтиламмония для гибких воздушно-цинковых аккумуляторов. ACS Appl.Матер. Интерфейсы 11, 28909–28917. DOI: 10.1021 / acsami.9b09086
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, М., Ло, Ф., Чжан, К., Ян, З. и Сюй, З. (2020). Нанолисты атомарного слоя Co3O4-x как эффективный и стабильный электрокатализатор для аккумуляторных воздушно-цинковых батарей. Дж. Катал . 381, 395–401. DOI: 10.1016 / j.jcat.2019.11.020
CrossRef Полный текст | Google Scholar
Ли, Ю., Чжун, К., Лю, Дж., Цзэн, X., Цюй, С., Han, X., et al. (2018). Атомарно тонкий мезопористый слой Co 3 O 4 слоя, прочно связанные с нанолистами N-rGO в качестве высокоэффективных бифункциональных катализаторов для одномерных вязанных цинковоздушных батарей. Adv. Матер. 30, 1703657. doi: 10.1002 / adma.201703657
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лю С., Хань В., Цуй Б., Лю X., Чжао Ф., Стюарт Дж. И др. (2017). Новый перезаряжаемый воздушно-цинковый аккумулятор с расплавленным солевым электролитом. J. Источники энергии 342, 435–441. DOI: 10.1016 / j.jpowsour.2016.12.080
CrossRef Полный текст | Google Scholar
Ma, L., Chen, S., Wang, D., Yang, Q., Mo, F., Liang, G., et al. (2019). Суперэластичные воздушно-цинковые батареи на основе щелочно-толерантного двухсетевого гидрогелевого электролита. Adv. Energy Mater. 9: 1803046. DOI: 10.1002 / aenm.201803046
CrossRef Полный текст | Google Scholar
Маккензи, Дж. Д., и Хо, К. (2015). Перспективы накопления энергии для гибких электронных систем. P. IEEE 103, 535–553. DOI: 10.1109 / JPROC.2015.2406340
CrossRef Полный текст | Google Scholar
Майнар, А. Р., Ируин, Э., Кольменарес, Л. К., Кваша, А., де Меатза, И., Бенгоэча, М., и др. (2018). Обзор достижений электролитов для вторичных воздушно-цинковых батарей и других систем хранения на основе цинка. J. Хранение энергии 15, 304–328. DOI: 10.1016 / j.est.2017.12.004
CrossRef Полный текст | Google Scholar
Майнар, Р.А., Леонет, О., Бенгоэча, М., Бояно, И., де Меатза, И. и др. (2016). Водно-щелочные электролиты для вторичных цинково-воздушных аккумуляторов: обзор. Внутр. J. Energy Res. 40, 1032–1049. DOI: 10.1002 / er.3499
CrossRef Полный текст | Google Scholar
Масри, М. Н., и Мохамад, А. А. (2013). Эффект добавления технического углерода к пористому цинковому аноду в воздушно-цинковой батарее. J. Electrochem. Soc. 160, A715 – A721. DOI: 10.1149 / 2.007306jes
CrossRef Полный текст | Google Scholar
Мяо, Х., Chen, B., Li, S., Wu, X., Wang, Q., Zhang, C., et al. (2020). Полностью твердотельный гибкий воздушно-цинковый аккумулятор с полиакриламидным щелочно-гелевым электролитом. J. Источники энергии 450: 227653. DOI: 10.1016 / j.jpowsour.2019.227653
CrossRef Полный текст | Google Scholar
Пан, З., Янг, Дж., Занг, В., Коу, З., Ван, К., Дин, X., et al. (2019). Полностью твердотельный губчатый сжимаемый воздушно-цинковый аккумулятор. Energy Storage Mater. 23, 375–382. DOI: 10.1016 / j.ensm.2019.04.036
CrossRef Полный текст | Google Scholar
Парк, Дж., Парк, М., Нам, Г., Ли, Дж. С., и Чо, Дж. (2015). Полностью твердотельная гибкая воздушно-цинковая батарея кабельного типа. Adv. Матер. 27, 1396–1401. DOI: 10.1002 / adma.201404639
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Паркер, Дж. Ф., Червин, К. Н., Нельсон, Э. С., Ролисон, Д. Р., и Лонг, Дж. У. (2014). Трехмерная разводка цинка меняет характеристики батареи — цикл без дендритов. Energy Environ. Sci. 7, 1117–1124. DOI: 10.1039 / C3EE43754J
CrossRef Полный текст | Google Scholar
Pedicini, C., Sieminski, D. P., Skeggs, L. T., Young, J. E., and Cherry, E. C. (1996). Система управления воздухом для рециркуляции реагирующего воздуха в металло-воздушной батарее. Патент США № 5,560,999. Вашингтон, округ Колумбия: заявка на патент Управления по патентам и товарным знакам США.
Google Scholar
Pedicni, C. S. (2002). Воздушная заслонка, реагирующая на нагрузку, для электрохимической ячейки.Патент США №6,350,537. Вашингтон, округ Колумбия: заявка на патент в Ведомстве США по патентам и товарным знакам.
Google Scholar
Пей П., Ван К. и Ма З. (2014). Технологии продления срока службы воздушно-цинковых батарей: обзор. Прил. Энергия 128, 315–324. DOI: 10.1016 / j.apenergy.2014.04.095
CrossRef Полный текст | Google Scholar
Pozo-Gonzalo, C., Virgilio, C., Yan, Y., Howlett, P. C., Byrne, N., MacFarlane, D. R., et al. (2014). Повышенная эффективность ионных жидкостей на основе фосфония в отношении реакции восстановления кислорода с 4 электронами при добавлении слабого источника протонов. Electrochem. Commun. 38, 24–27. DOI: 10.1016 / j.elecom.2013.10.004
CrossRef Полный текст | Google Scholar
Шредер Д., Боркер Н. С., Кёниг М. и Кревер У. (2015). Характеристики воздушно-цинковых батарей с добавкой K 2 CO 3 в щелочном электролите. J. Appl. Электрохим. 45, 427–437. DOI: 10.1007 / s10800-015-0817-0
CrossRef Полный текст | Google Scholar
См. Д. М. и Уайт Р. Э. (1997).Температурная и концентрационная зависимость удельной проводимости концентрированных растворов гидроксида калия. J. Chem. Англ. Данные 42, 1266–1268. DOI: 10.1021 / je970140x
CrossRef Полный текст | Google Scholar
Шинде, С.С., Ли, К.Х., Юнг, Дж.-Й., Ваг, Н.К., Ким, С.-Х., Ким, Д.-Х., и др. (2019). Презентация двухзвенных металлоорганических каркасов из гексаиминобензола в 3D для создания долговечных усовершенствованных обратимых Zn-воздушных батарей. Energy Environ. Sci. 12, 727–738. DOI: 10.1039 / c8ee02679c
CrossRef Полный текст | Google Scholar
Саймонс, Т., Торриеро, А., Хоулетт, П., Макфарлейн, Д. Р., и Форсайт, М. (2012). Высокая плотность тока, эффективное циклирование Zn 2+ в ионной жидкости дицианамида 1-этил-3-метилимидазолия: влияние концентрации соли и воды Zn 2+ . Electrochem. Commun. 18, 119–122. DOI: 10.1016 / j.elecom.2012.02.034
CrossRef Полный текст | Google Scholar
Тан, П., Chen, B., Xu, H., Zhang, H., Cai, W., Ni, M., et al. (2017). Гибкие Zn- и Li-air аккумуляторы: последние достижения, проблемы и перспективы на будущее. Energy Environ. Sci. 10, 2056–2080. DOI: 10.1039 / c7ee01913k
CrossRef Полный текст | Google Scholar
Ван К., Пей П., Ма З., Сюй Х., Ли П. и Ван X. (2014). Контроль морфологии регенерации цинка для воздушно-цинковых топливных элементов и батарей. J. Источники энергии 271, 65–75. DOI: 10.1016 / j.jpowsour.2014.07.182
CrossRef Полный текст | Google Scholar
Ван, В., Тан, М., Чжэн, З., и Чен, С. (2019). Ультратонкий, гибкий и высокопроизводительный твердотельный Zn-воздушный аккумулятор на основе щелочно-полимерной мембраны. Adv. Energy Mater. 9, 1803628. doi: 10.1002 / aenm.201803628
CrossRef Полный текст | Google Scholar
Ван, X., Сунарсо, Дж., Лу, К., Чжоу, З., Дай, Дж., Гуань, Д., и др. (2020). Высокопроизводительный бифункциональный кислородный электрокатализатор из платино-перовскитового композитного материала для аккумуляторных Zn-воздушных батарей. Adv. Энергетика . 10: 11. DOI: 10.1002 / aenm.2011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ву Г., Линь С. и Ян К. (2006). Щелочные Zn-воздушные и Al-воздушные ячейки на основе новых твердотельных полимерных электролитных мембран ПВС / ПАА. J. Membr. Sci. 280, 802–808. DOI: 10.1016 / j.memsci.2006.02.037
CrossRef Полный текст | Google Scholar
Xiang, H., Yin, B., Wang, H., Lin, H., Ge, X., Xie, S., et al. (2010).Улучшение электрохимических свойств электролита на основе ионной жидкости комнатной температуры (RTIL) для литий-ионных аккумуляторов. Электрохим. Acta 55, 5204–5209. DOI: 10.1016 / j.electacta.2010.04.041
CrossRef Полный текст | Google Scholar
Xu, L., Liu, J., Chen, P., Wang, Z., Tang, D., Liu, X., et al. (2020). Мощные водные батареи Zn-h3O2 для широкого применения. Cell Rep. Phys. Sci . 1: 100027. DOI: 10.1016 / j.xcrp.2020.100027
CrossRef Полный текст | Google Scholar
Сюй, М., Айви, Д., Се, З., и Цюй, В. (2015). Перезаряжаемые Zn-воздушные батареи: прогресс в разработке электролитов и улучшении конфигурации элементов. J. Источники энергии 283, 358–371. DOI: 10.1016 / j.jpowsour.2015.02.114
CrossRef Полный текст | Google Scholar
Xu, N., Zhang, Y., Wang, M., Fan, X., Zhang, T., Peng, L., et al. (2019). Высокопроизводительные перезаряжаемые / гибкие воздушно-цинковые батареи с координированным иерархическим биметаллическим электрокатализатором и гетероструктурной анионообменной мембраной. Нано Энергия 65: 104021. DOI: 10.1016 / j.nanoen.2019.104021
CrossRef Полный текст | Google Scholar
Янь З., Ван Э., Цзян Л. и Сунь Г. (2015). Превосходная циклическая стабильность и высокая производительность трехмерных электродов из вспененного цинка / меди для щелочных батарей на основе цинка. RSC Adv. 5, 83781–83787. DOI: 10.1039 / C5RA16264E
CrossRef Полный текст | Google Scholar
Ян, Х., Цао, Й., Ай, X., и Сяо, Л. (2004). Повышенная разрядная способность и подавление пассивации поверхности цинкового анода в разбавленном щелочном растворе с использованием добавок поверхностно-активных веществ. J. Источники энергии 128, 97–101. DOI: 10.1016 / j.jpowsour.2003.09.050
CrossRef Полный текст | Google Scholar
Yu, M., Wang, Z., Hou, C., Wang, Z., Liang, C., Zhao, C., et al. (2017). Легированный азотом Co 3 O 4 массивы мезопористых нанопроволок в качестве воздушного катода без добавок для гибких твердотельных воздушно-цинковых батарей. Adv. Матер. 29: 1602868. DOI: 10.1002 / adma.201602868
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Целлер Р.А. (2011). Влияние внешней и внутренней активности протонов на механизм восстановления кислорода в ионных жидкостях . (Темп, Аризона: Государственный университет Аризоны, ProQuest Dissertations Publishing).
Google Scholar
Чжун, X., И, В., Цюй, Ю., Чжан, Л., Бай, Х., Чжу, Ю. и др. (2020). Одноатомный атом Co закреплен на Co3O4 и активированном угле, легированном азотом, в направлении бифункционального катализатора для воздушно-цинковых батарей. Прил. Catal., B 260, 118188. DOI: 10.1016 / j.apcatb.2019.118188
CrossRef Полный текст | Google Scholar
Zhu, L., Zheng, D., Wang, Z., Zheng, X., Fang, P., Zhu, J., et al. (2018). Стратегия ограничения для стабилизации бифункциональных катализаторов на основе ZIF в качестве эталонного катода гибких полностью твердотельных цинково-воздушных батарей. Adv. Матер. 30: e1805268. DOI: 10.1002 / adma.201805268
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Северо-восточная батарея | Блог | Основы водяного аккумулятора
Вода или электролиты — очень важная часть того, что заставляет вашу батарею работать.Количество воды в сочетании с размером пластин аккумулятора определяет количество заряда, которое сохранит ваша свинцово-кислотная аккумуляторная батарея . Знание того, как правильно управлять уровнем воды в вашей батарее, может продлить срок ее службы и помочь вам избежать катастрофического отказа батареи.
Основы
Когда аккумулятор заряжается и электричество течет через воду, оно превращается в исходные газы водорода и кислорода. Это выделение газов приводит к потере воды и является прямой причиной того, что вам необходимо время от времени пополнять запас воды в батарее.
Легковоспламеняющиеся газы являются причиной вентиляции многих корпусов батарей. Герметичные корпуса фактически позволяют газам рекомбинировать в воду, что компенсирует некоторую потерю воды, но не всю.
Когда пополнятьЛучший способ узнать, что пришло время долить воду, — это проверить уровень воды. Если уровень воды упадет ниже вершин пластин, вы можете повредить аккумулятор, не подлежащий ремонту. Следуйте этим нескольким практическим правилам:
- Ознакомьтесь с рекомендациями производителя .Обычно они предлагают рекомендации для вашей конкретной батареи.
- Чем чаще вы используете и перезаряжаете аккумулятор, тем больше потери воды вы испытываете, поэтому скорректируйте график технического обслуживания соответствующим образом.
- Температура является важным фактором потери воды. Если вы живете в более теплом климате, вам нужно чаще проверять уровень воды. Также полезно ознакомиться с , что вызывает утечку батареи.
Уровень воды должен быть примерно на ½ дюйма выше вершин пластин, чтобы считаться нормальным.При добавлении воды обязательно используйте дистиллированную воду. Водопроводная вода содержит минералы, которые могут снизить производительность аккумулятора и увеличить скорость их саморазряда. Перед добавлением воды убедитесь, что аккумулятор полностью заряжен.
Ловушки, которых следует остерегаться— Новые батареи иногда могут иметь низкий уровень электролита. Обязательно зарядите аккумулятор и при необходимости долейте воды.Если вы добавите еще воды до полной зарядки аккумулятора, существует риск перелива электролита.
— Избыточный полив может привести к разбавлению электролитов. , и вы испытаете снижение уровня производительности. Если уровень воды в пределах нормы, не доливайте воду.
— Подвод воды может привести к сульфатации . Сульфатирование — это когда кристаллы сульфата начинают накапливаться на пластинах батареи. Сульфатирование приводит к увеличению времени зарядки, потере мощности и является основной причиной преждевременного выхода из строя.
Остерегайтесь срезания угловМногие люди спрашивают, могут ли они уменьшить потребность в добавлении воды в батарею, если уменьшат напряжение зарядки. Хотя это правда, чем ниже напряжение зарядки, тем меньше будет потеря воды, но у этого процесса есть и другие последствия. Расслоение батареи — наиболее частый побочный эффект зарядки с более низким напряжением.
Расслоение — это когда кислота в электролите начинает отделяться и оседает на дне батареи.Эта концентрация кислоты приводит к сульфатированию, о котором упоминалось выше. Сульфатирование — враг вашей батареи, и необходимо соблюдать надлежащее обслуживание, если вы хотите продлить срок службы и возможности вашей батареи.
Полив свинцово-кислотного аккумулятора: основы
Так же, как нельзя обойтись без воды, нельзя обойтись и аккумулятором. Полив свинцово-кислотного аккумулятора — важный этап обслуживания, который нельзя пропустить. Это сохраняет вашу батарею в оптимальном состоянии и безопасно для ее использования.Несвоевременный полив свинцово-кислотной батареи может привести к серьезным повреждениям, но не всегда легко понять, когда лучше поливать батарею. Следуйте этим инструкциям по поливу свинцово-кислотной батареи.
Почему батареи нужно поливать
Свинцово-кислотные батареи состоят из плоских свинцовых пластин, погруженных в бассейн с электролитом. Электролит состоит из воды и серной кислоты. Размер пластин аккумулятора и количество электролита определяют количество заряда, которое может сохранить свинцово-кислотный аккумулятор, или количество часов использования.Вода — ключевая часть функционирования свинцовой батареи.
Кроме того, во время процесса перезарядки, когда электричество проходит через водную часть электролита, вода превращается в свои исходные элементы, водород и кислород. Эти газы очень легко воспламеняются, и поэтому из вашего жилого автофургона или морских аккумуляторов необходимо выпускать воздух наружу. Выделение газов приводит к потере воды, поэтому в свинцово-кислотные батареи необходимо периодически добавлять воду. Батареи, не требующие особого обслуживания, такие как батареи AGM, являются исключением, поскольку они способны компенсировать потерю воды.
Чрезмерный полив и недостаточный полив могут повредить аккумулятор. Чтобы свинцовый аккумулятор работал на максимальном уровне, следуйте этим рекомендациям по поливу.
Первое — начните с безопасностиДля начала обязательно используйте средства индивидуальной защиты, такие как защитные очки и перчатки, при работе с аккумуляторами. Кроме того, очень важно понимать, что некоторые батареи требуют регулярного полива, в то время как другие батареи не требуют обслуживания.
Обязательно найдите информацию на этикетке аккумулятора, которая указывает, можно ли открыть аккумулятор и отремонтировать. В зависимости от типа батареи, которую вы используете, предупреждающие надписи на батарее должны направлять вас «НЕ ОТКРЫВАТЬ» батарею или «ЗАДЕРЖИВАЙТЕ ВЕНТИЛЯЦИОННЫЕ КОЛПАЧКИ ПОСЛЕ ПОЛИВА». Обязательно следуйте инструкциям на этикетке с предупреждением.
Как полить аккумулятор
Хотя аккумулятор следует заряжать только после того, как он полностью зарядится, вам также следует проверить уровень воды перед зарядкой, чтобы убедиться, что воды достаточно, чтобы покрыть все открытые пластины.После зарядки добавьте достаточно воды, чтобы довести уровень до дна вентиляционного отверстия, примерно на ¾ ниже верха элемента.
Важно отметить, что владельцы аккумуляторов никогда не должны добавлять в аккумуляторы серную кислоту. При нормальной работе батареи потребляют только воду, а не серную кислоту. Когда уровень электролита в вашей батарее низкий, заполнение батареи водой сохранит батарею здоровой и безопасной для использования.
Не над водойВо время зарядки аккумулятора плотность раствора электролита увеличивается.Если перед зарядкой было добавлено слишком много воды, уровень электролита увеличится, что приведет к переполнению аккумулятора и повреждению аккумулятора. Кроме того, чрезмерное увлажнение аккумулятора может привести к дополнительному разбавлению электролита, что приведет к снижению производительности аккумулятора.
Когда следует поливать аккумулятор
Как часто вы добавляете воду в аккумулятор, зависит от того, как часто вы им пользуетесь. Аккумулятор для тележки для гольфа, который используется только по выходным, может потребовать полива только один раз в месяц.Вилочный погрузчик, который используется весь день, каждый день, может нуждаться в поливе аккумулятора каждую неделю. В жаркую погоду увеличивается потребность в поливе. Важно регулярно проверять уровень жидкости в аккумуляторе — лучше всего это делать после того, как аккумулятор зарядится.
Какую воду следует использоватьИзбегайте использования водопроводной воды. При заправке аккумулятора обычная водопроводная вода не подойдет. Водопроводная вода содержит минералы, которые вредны для аккумуляторов, даже если их добавляют в небольших количествах.Это особенно верно для воды, умягченной с помощью умягчителей, содержащих хлориды. На всякий случай лучше всего подойдет дистиллированная вода, которая требует гораздо меньших вложений, чем новая батарея.
Помните, что вода будет находиться поверх раствора кислоты в вашей батарее, пока он не смешается с пузырьками, возникающими при зарядке. Если вы снимаете показания ареометра электролита, лучше всего снимать их после завершения зарядки.




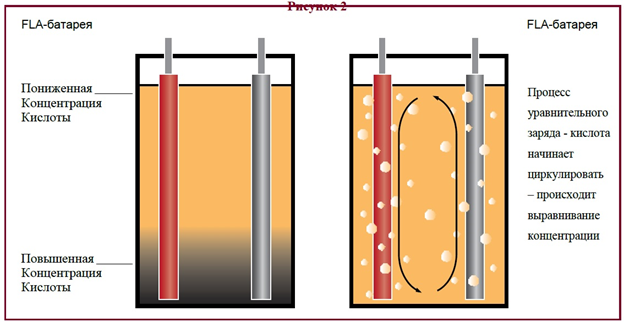 п.
п.
 Это значит, что далее раствор нужно разбавлять дистиллированной водой. В самом начале будет достаточно придерживаться приблизительных показателей, так как до нормы плотность доводится уже после заряда АКБ.
Это значит, что далее раствор нужно разбавлять дистиллированной водой. В самом начале будет достаточно придерживаться приблизительных показателей, так как до нормы плотность доводится уже после заряда АКБ.

 В противном случае АКБ можно полностью вывести из строя.
В противном случае АКБ можно полностью вывести из строя.